
【題目】如圖是s能級和p能級的原子軌道圖,試回答下列問題:
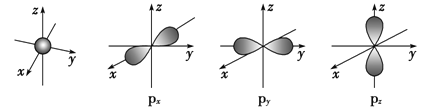
(1)s電子的原子軌道呈______形,每個s能級有______個原子軌道;p電子的原子軌道呈________形,每個p能級有________個原子軌道。
(2)元素X的原子最外層電子排布式為nsnnpn+1,原子中能量最高的是________電子,其電子云在空間有________方向;元素X的名稱是_______,它的氫化物的電子式是____________。若元素X的原子最外層電子排布式為nsn-1npn+1,那么X的元素符號為________,原子的電子排布圖為___________。
【答案】球 1 啞鈴 3 2p 三個互相垂直的伸展 氮 ![]() S
S ![]()
【解析】
(1)s電子的原子軌道都是球形的,每個s能級有1個原子軌道;p電子的原子軌道都是啞鈴形的,每個p能級有3個原子軌道,它們相互垂直,分別以px、py、pz表示。
(2)因為元素X的原子最外層電子排布式為nsnnn+1,np軌道已排上電子,說明ns軌道已排滿電子,即n=2,則元素X的原子核外電子排布式為1s22s22p3,是氮元素,其中原子中能量最高的是2p電子,其電子云在空間有三個互相垂直的伸展方向;氮元素的氫化物是氨氣,含有極性鍵,其電子式是![]() ;當元素X的原子最外層電子排布式為nsn-1npn+1時,根據上述分析,有n-1=2,則n=3,所以X元素的原子核外電子排布式為1s22s22p63s23p4,是硫元素;硫元素的元素符號為S,其原子的電子排布圖為
;當元素X的原子最外層電子排布式為nsn-1npn+1時,根據上述分析,有n-1=2,則n=3,所以X元素的原子核外電子排布式為1s22s22p63s23p4,是硫元素;硫元素的元素符號為S,其原子的電子排布圖為![]() 。
。


 名牌學校分層周周測系列答案
名牌學校分層周周測系列答案 黃岡海淀全程培優測試卷系列答案
黃岡海淀全程培優測試卷系列答案科目:高中化學 來源: 題型:
【題目】柔紅酮是一種醫藥中間體,其結構簡式如圖所示。下列說法正確的是( )
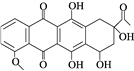
A. 每個柔紅酮分子中含有2個手性碳原子
B. 柔紅酮分子中所有的碳原子都在同一個平面上
C. 1 mol柔紅酮最多可與2 mol Br2發生取代反應
D. 一定條件下柔紅酮可發生氧化、加成、消去反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知在柑橘、檸檬等水果中含有檸檬酸,且已知檸檬酸中只含C、H、O三種元素。取檸檬酸19.2g,在氧氣中完全燃燒,產生CO2和H2O分別為26.4g和7.2g,現對該物質進行質譜分析,可獲得檸檬酸的相對分子質量為192,利用紅外光譜分析可知檸檬酸分子中含有﹣COOH和﹣OH。請回答:
(1)通過計算,可獲得檸檬酸的分子式為_____。
(2)再利用核磁共振氫譜分析發現有4個吸收峰,其峰面積之比為4:2:1:1.綜合以上信息,寫出檸檬酸的結構簡式_____。
(3)檸檬酸與有機物C在一定條件下發生酯化反應可生成一種相對分子質量為220的酯類物質。寫出C所有可能的結構簡式_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫時,用0.200molL-1鹽酸滴定 20.00mL 0.200 molL-1 的 NaY 溶液,溶液中水的電離程度隨所加鹽酸的體積變化如圖所示(忽略滴定過程中溶液體積變化),則下列有關說法正確的是[已知 Ka(HY)=5.0×10-11]

A.可選取酚酞作為滴定指示劑B.M 點溶液的 pH>7
C.Q 點水的電離程度最小,Kw<l0-14D.M點,c(Na+)=c (HY)+c (Y-)+c (Cl-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新型材料 AIN 應用前景廣泛,對其制備過程的研究成為熱點。
(1)將物質的量均為a mol 的 Al2O3與N2 充入恒溫恒容密閉容器中,控制溫度發生反應:2Al2O3(s)+2N2(g) ![]() 4AlN(s) +3O2(g) △H>0。
4AlN(s) +3O2(g) △H>0。
①下列可作為反應達到平衡的判據是_________(填序號)。
A.固體的質量不再改變
B.2v正(N2)=3v逆(O 2)
C.△H 不變
D.容器內氣體的壓強不變
E.N2分子數與 O2 分子數比為 2:3
②在起始壓強為p的反應體系中,平衡時 N2的轉化率為α,則上述反應的平衡常數 Kp__________(對于氣相反應,用某組分 B 的平衡壓強 p(B)代替物質的量濃度c(B)也可表示平衡常數,記作Kp,如p(B) =p總·x(B) ,p總為平衡總壓強,x(B)為平衡系統中B的物質的量分數)。
③為促進反應的進行,實際生產中需加入焦炭,其原因是____________。
(2)鋁粉與 N2 在一定溫度下可直接生成 AlN, 加入少量 NH4Cl 固體可促進反應。將等質量的A1粉與不同量的 NH4Cl混合均勻后置于充 N2的密閉容器中,電火花引燃,產品中 AlN的質量分數[ω(AlN)] 隨原料中ω(NH4Cl)的變化如圖1所示,燃燒過程中溫度隨時間變化如圖2所示。則:
①固體混合物中,ω(NH4Cl)的最佳選擇是__________。
②結合圖2解釋當ω(NH4Cl)超過一定值后,ω(AlN)明顯減少的原因__________。

(3)AIN粉末會緩慢發生水解反應,粒徑為100 nm 的 AlN 粉末水解時溶液 pH的變化如圖3 所示。

①AlN 粉末水解的化學方程式是______________。
②相同條件下,請在圖3中畫出粒徑為40 nm 的AlN粉末水解的變化曲線____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋰輝石(主要成分為LiAl(SiO3)2,還含有Fe2O3、MgO、Al2O3等雜質)是最重要的提鋰礦石原料,工業上以α-鋰輝石為原料制備碳酸鋰,其工藝流程如圖:

已知:①α-鋰輝石化學惰性大,除HF外,幾乎不與任何酸堿反應,α-鋰輝石在高溫下可轉化為β-鋰輝石,β-鋰輝石具有更高的化學活性。
②β-鋰輝石可與濃硫酸發生反應:2β-LiAl(SiO3)2+H2SO4(濃) ![]() Li2SO4+Al2O3·4SiO2·H2O。
Li2SO4+Al2O3·4SiO2·H2O。
③部分金屬氫氧化物開始沉淀和完全沉淀的pH如下表:
氫氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
開始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
請回答下列問題:
(1)將LiAl(SiO3)2改寫成氧化物的形式為___,1000℃焙燒α-鋰輝石的目的為___。
(2)濾渣2的主要成分為___,調節pH值的范圍為___。
(3)“除大部分Mg”步驟的離子方程式為___。
(4)實驗室蒸發濃縮操作中所需的儀器為酒精燈、鐵架臺(帶鐵圈)、___。
(5)洗滌過程中檢驗沉淀是否洗滌干凈的操作為___。
(6)碳酸鋰是制備鋰離子電池的原料之一,某鋰離子電池以CoP3作為負極材料,以LiMn1.5Ni0.5O4作為正極材料,以可傳導放電Li+的無機固體電解質c-LATP作為電解液,其工作時電池反應為Li1-xMn1.5N0.5O4+Lix(CoP3)n![]() LiMn1.5Ni0.5O4+(CoP3)n,則該電池放電時負極的電極反應式為___,充電時陽極的電極反應式為___。
LiMn1.5Ni0.5O4+(CoP3)n,則該電池放電時負極的電極反應式為___,充電時陽極的電極反應式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳酸鈉與工農業生產、日常生活緊密相關。工業上碳酸鈉大多采用侯氏制堿法制取,所得碳酸鈉樣品往往含有少量的NaCl,現欲測定碳酸鈉樣品中Na2CO3的質量分數,某探究性學習小組分別設計了如下實驗方案。
方案一:沉淀分析法
(1)把一定質量的樣品溶解后加入過量的CaCl2溶液,將所得沉淀________(填操作名稱)、洗滌、烘干、稱量。洗滌沉淀的操作是________________________________________.
方案二:氣體分析法
(2)用如圖所示裝置,將一定質量的樣品與足量鹽酸反應,并測定產生CO2氣體的體積,為了使測量結果準確,B中的溶液最好采用________(填字母)。
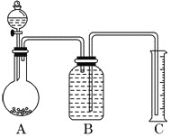
a.飽和碳酸鈉溶液 b.飽和碳酸氫鈉溶液
c.飽和氫氧化鈉溶液 d.氯化鈉溶液
但選用該溶液后實驗結果仍然不夠準確,原因是________________________________
方案三:質量差分析法
(3)采用如圖所示裝置,將一定質量的樣品與足量的稀硫酸反應,通過稱量反應前后盛有堿石灰的干燥管的質量,利用其質量差計算樣品的純度。
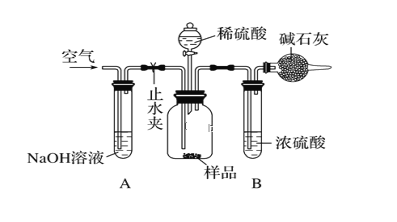
該實驗的操作步驟:
①在干燥管內裝滿堿石灰,質量為m1g ②取ng樣品裝入廣口瓶中 ③檢查裝置的氣密性 ④緩慢鼓入空氣數分鐘,再稱量干燥管質量為m2g ⑤關閉止水夾 ⑥打開止水夾 ⑦緩慢加入稀硫酸至不再產生氣體為止 ⑧緩慢鼓入空氣數分鐘
Ⅰ.正確的操作順序是(填序號):③→_____→⑥→_____→⑤→________→⑦→________→④。
Ⅱ.在操作④中,要緩慢鼓入空氣數分鐘,鼓入空氣的作用是________________;裝置 B的作用是__________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某科學家利用二氧化鈰(CeO2)在太陽能作用下將H2O、CO2轉變成H2、CO,其過程如下:mCeO2 (m-x)CeO2·xCe+xO2;(m-x)CeO2·xCe+xH2O+xCO2
(m-x)CeO2·xCe+xO2;(m-x)CeO2·xCe+xH2O+xCO2![]() mCeO2+xH2+xCO
mCeO2+xH2+xCO

下列說法不正確的是( )
A.該過程中CeO2沒有消耗B.該過程實現了太陽能向化學能的轉化
C.圖中ΔH1=ΔH2+ΔH3D.H2(g)+O2(g)=H2O(g)的反應熱大于ΔH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將一定量的CO2氣體通入2L的NaOH溶液中,在所得溶液中逐滴加入稀鹽酸至過量,并將溶液加熱,產生的氣體與消耗的HC1物質的量關系如圖所示(忽略氣體的溶解和HC1的揮發).下列說法不正確的是
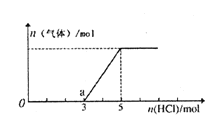
A. 0點溶液中所含溶質的化學式為NaOH、Na2CO3
B. 0到a點發生反應的離子方程式:H++OH-=H2O、CO32-+H+=HCO3-
C. 通入CO2氣體的體積在標準狀況下為22.4L
D. NaOH溶液的物質的量濃度為2.5mol/L
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com