
如右圖所示的裝置,通電一段時間后,測得甲池中某電極質量增加2.16g,乙池中某電極上析出0.24g某金屬,下列說 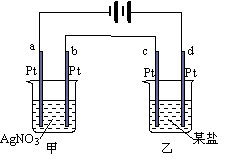 法正確的是
法正確的是
A.甲池是b極上析出金屬銀,乙池是c極上析出某金屬
B.甲池是a極上析出金屬銀,乙池是d極上析出某金屬
C.某鹽溶液可能是CuSO4溶液
D.某鹽溶液可能是Mg(NO3)2溶液
科目:高中化學 來源: 題型:
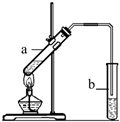 “酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯.回答下列問題:
“酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯.回答下列問題: CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O查看答案和解析>>
科目:高中化學 來源: 題型:
 “酒是陳的香”,就是因為酒在儲存過程中生成了有香 味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯.
“酒是陳的香”,就是因為酒在儲存過程中生成了有香 味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯.| 濃硫酸 |
| △ |
| 濃硫酸 |
| △ |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
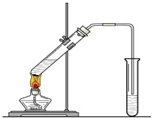 “酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯.回答下列問題:
“酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯.回答下列問題:| 濃硫酸 |
| △ |
| 濃硫酸 |
| △ |
查看答案和解析>>
科目:高中化學 來源:2015屆云南省高一下學期期中考試化學文科卷(本部)(解析版) 題型:填空題
“酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯。回答下列問題:
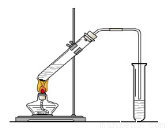
(1)寫出制取乙酸乙酯的化學反應方程式: 。
(2)在大試管中配制一定比例的乙醇、乙酸和濃硫酸的混合液的方法(加入試劑順序)是: 。
(3)濃硫酸的作用是:① ;② 。
(4)飽和碳酸鈉溶液的主要作用是
。
(5)裝置中通蒸氣的導管要插在飽和碳酸鈉溶液的液面上,不能插入溶液中,目的是防止 。
(6)若要把制得的乙酸乙酯分離出來,應采用的實驗操作是
查看答案和解析>>
科目:高中化學 來源:09-10年湛江一中高一下學期期末考試化學卷 題型:實驗題
(20分) “酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯。回答下列問題:

(1).寫出制取乙酸乙酯的化學反應方程式
(2).在大試管中配制一定比例的乙醇、乙酸和濃硫酸的混合液的方法是: 。
(3).濃硫酸的作用是:① ;② 。
(4).飽和碳酸鈉溶液的主要作用是 。
(5).裝置中通蒸氣的導管要插在飽和碳酸鈉溶液的液面上,不能插入溶液中,目的是防止 。
(6).若要把制得的乙酸乙酯分離出來,應采用的實驗操作的名稱是 。
(7).做此實驗時,有時還向盛乙酸和乙醇的試管里加入幾塊碎瓷片,其目的是 。
(8).生成乙酸乙酯的反應是可逆反應,反應物不能完全變成生成物,反應一段時間后,就達到了該反應的限度,也即達到化學平衡狀態。下列描述能說明乙醇與乙酸的酯化反應已達到化學平衡狀態的有(填序號) 。
①單位時間里,生成1mol乙酸乙酯,同時生成1mol水
②單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸
③單位時間里,消耗1mol乙醇,同時消耗1mol乙酸
④正反應的速率與逆反應的速率相等
⑤混合物中各物質的濃度不再變化
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com