
【題目】(1)請用下列4種物質的序號填空:①O2 ②NH4NO3 ③K2O2 ④NH3,既有離子鍵又有極性鍵的是___________。(填序號)
(2)氯化鋁的物理性質非常特殊,如:氯化鋁的熔點為190 ℃(2.02×105 Pa),但在180 ℃就開始升華。據此判斷,氯化鋁是___________(填“共價化合物”或“離子化合物”),設計實驗證明你的判斷正確的實驗依據是________________。
(3)現有a~g7種短周期元素,它們在周期表中的位置如下,請據此回答下列問題:
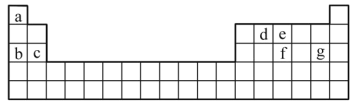
①元素的原子間反應最容易形成離子鍵的是___________。
A.c和f B.b和g C.d和g D.b和e
②d與g元素形成的分子中所有原子___________(填“是”或“不是”)都滿足最外層為8電子結構。
(4)A、B、C、D四種短周期元素,它們的原子序數依次增大,其中A與C,B與D分別是同主族元素,已知B、D兩元素間可形成DB2和DB3兩種化合物,兩者相對分子質量相差16;又如A、C兩元素原子序數之和是B、D兩元素原子序數之和的1/2。請回答下列問題:
①寫出由B、C兩種元素形成的原子個數比為1:1的化合物的電子式:________,其晶體中所含化學鍵的類型有________。
②A2B與A2D的沸點:A2B________A2D(填“高于”或“低于”),其原因是____________。
③由A、B、C、D四種元素形成的物質X,與鹽酸反應能夠生成具有刺激性氣味的氣體,寫出X與鹽酸反應的離子方程式:____________________________。
④碳元素的一種同位素可測定文物年代,這種同位素的符號是________。
【答案】 ② 共價化合物 氯化鋁在熔融狀態下不能導電 B 是 ![]() 離子鍵、共價鍵(非極性共價鍵) 高于 水分子間存在氫鍵,硫化氫分子間沒有氫鍵 HSO3-+H+=SO2↑+H2O
離子鍵、共價鍵(非極性共價鍵) 高于 水分子間存在氫鍵,硫化氫分子間沒有氫鍵 HSO3-+H+=SO2↑+H2O ![]()
【解析】(1)一般活潑的金屬和活潑的非金屬容易形成離子鍵,非金屬元素的原子間容易形成共價鍵,同種非金屬形成非極性鍵,不同非金屬形成極性鍵,據此判斷;
(2)氯化鋁的熔點為190℃(2.02×105 Pa),但在180℃就開始升華,可知熔沸點低,與分子晶體的性質相似;
(3)由元素的位置可知,a為H,b為Na,c為Mg,d為C,e為N,f為P,g為Cl。
(4)由B、D兩元素間可形成DB2和DB3兩種化合物,兩者相對分子質量相差16,可知B為O元素,B與D分別是同主族元素,所以D為S元素,B和D形成的化合物為SO2、SO3,S和O元素原子序數之和為24,則A、C元素原子序數之和為12,因A、C同主族,所以A為H元素,C為Na元素,根據元素對應的單質、化合物的性質結合元素周期律解答。
(1)①O2分子中含有非極性鍵;②NH4NO3中含有離子鍵和極性鍵;③K2O2中含有離子鍵,氧原子和氧原子之間還有非極性鍵;④NH3分子中只有極性鍵,則既有離子鍵又有極性鍵的是過氧化鉀,答案選②。
(2)氯化鋁的熔點為190℃(2.02×105 Pa),在180℃就開始升華,可知熔沸點低,與分子晶體的性質相似,可知由共價鍵形成的共價化合物,實驗依據是氯化鋁在熔融狀態下不能導電。
(3)由元素的位置可知,a為H,b為Na,c為Mg,d為C,e為N,f為P,g為Cl。則
①活潑的金屬與活潑的非金屬容易形成離子鍵,則元素的原子間反應最容易形成離子鍵的是b和g(NaCl),答案為B;
②d與g元素形成的CCl4分子中所有原子都滿足最外層為8電子結構;
(4)根據以上分析可知A、B、C、D分別是H、O、Na、S。則
①由B、C兩種元素形成的原子個數比為1:1的化合物是過氧化鈉,電子式為![]() ,其晶體中所含化學鍵的類型有離子鍵和共價鍵。
,其晶體中所含化學鍵的類型有離子鍵和共價鍵。
②H2O和H2S都是氫化物,其固體都屬于分子晶體,分子晶體中物質的沸點與其相對分子質量成正比,但水中含有氫鍵,硫化氫中不含氫鍵,所以二者沸點較高的是H2O。
③A、B、C、D四種元素形成的物質X為NaHSO3,NaHSO3和鹽酸反應生成的二氧化硫具有刺激性氣味,反應的離子方程式為HSO3-+H+=SO2↑+H2O。
④碳元素的一種同位素可測定文物年代,這種同位素的符號是![]() 。
。


科目:高中化學 來源: 題型:
【題目】有下列六種物質的溶液:①NaCl ②NH4Cl ③Na2CO3 ④Al2(SO4)3 ⑤CH3COOH ⑥NaHCO3。
(1)25℃時,0.1mol·L-1②溶液的pH________7(填“>”、“=”或“<”);其原因是______________________________________(用離子方程式表示);
(2)常溫下,濃度均為0.1mol/L的③和⑥的溶液中離子種類________(填“相同”或是“不相同”);
(3)將④溶液加熱蒸干并灼燒最終得到的物質是____________(填化學式);
(4)常溫下0.1 mol/L的⑤溶液加水稀釋過程中,下列表達式的數據一定變大的是_________。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定的溫度、壓強和釩催化劑存在的條件下,SO2被空氣中的O2氧化為SO3。V2O5是釩催化劑的活性成分,郭汗賢等提出:V2O5在對反應I的催化循環過程中,經歷了Ⅱ、Ⅲ兩個反應階段,圖示如圖1:
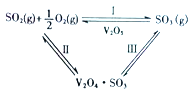
圖1
(1)①已知有關氣體分子中1mol化學鍵斷裂時需要吸收的能量數據如下:
化學鍵 | S=O(SO2) | O=O(O2) | S=O(SO3) |
能量/kJ | 535 | 496 | 472 |
由此計算反應Ⅰ的△H=_________kJ·mol-1。
②寫出反應Ⅱ的化學方程式_________。
(2)不能說明反應Ⅰ達到平衡狀態的是_________。
A.恒容密閉容器中混合氣體的壓強不再變化
B.恒容密團容器中混合氣體的密度不再變化
C.混合氣體的總物質的量不再變化
D.混合氣體的平均相對分子質量不再變化
E.n(SO2)∶n(O2)∶n(SO3)=2∶1∶2
F.SO2氣體的百分含量不再變化
(3)在保持體系總壓為105Pa的條件下進行反應SO2+1/2O2![]() SO3,原料氣中SO2和O2的物質的量之比m(m=
SO3,原料氣中SO2和O2的物質的量之比m(m=![]() )不同時,SO2的平衡轉化率與溫度(t)的關系如下圖所示:
)不同時,SO2的平衡轉化率與溫度(t)的關系如下圖所示:
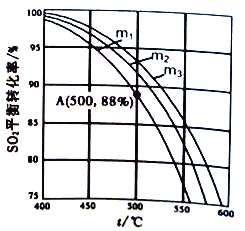
①圖中m1、m2、m3的大小順序為_________,理由是_________。
②反應I的化學平衡常數Kp表達式為_________(用平衡分壓代替平衡濃度表示)。圖中A點原料氣的成分是:n(SO2)=10mol,n(O2)=24.4mol,n(N2)=70mol,達平衡時SO2的分壓p(SO2)為_________Pa。(分壓=總壓×物質的量分數)。
③近年,有人研發出用氧氣代替空氣的新工藝,使SO2趨于全部轉化。此工藝的優點除了能充分利用含硫的原料外,主要還有_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎢有“光明使者”的美譽,在自然界中主要以鎢(+6價)酸鹽的形式存在,黑鎢礦的主要成分是鐵和錳的鎢酸鹽,化學式常寫成(Fe、Mn)WO4,鎢酸(B)酸性很弱,難溶于水,黑鎢礦傳統冶煉工藝的第一階段是堿熔法,第二階段則是用還原劑還原出金屬鎢。化合物A、B、C含有同一元素。請回答下列問題:
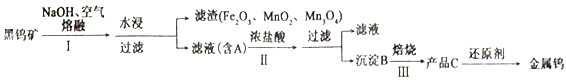
(1)為提高水浸速率,采取的措施為___________________(寫兩種)。
(2)用還原劑還原出金屬鎢。
①碳和氫氣均可還原化合物C得鎢,用氫氣比用碳更具有優點,其理由是___________。
②如果用金屬鋁與化合物C反應,還原出1mol鎢至少需要鋁的質量為___________。
(3)利用“化學蒸氣轉移法”提純金屬鎢的反應原理為:W(s)+I2(g)![]() WI2(g) △H<0。
WI2(g) △H<0。
①一定溫度下,向某恒容密閉容器中加入2molI2(g)和足量W(s)達平衡后,I2(g)的轉化率為20%,則平衡時c[I2(g)]∶c[WI2(g)]=___________;相同條件下,若開始加入I2(g)的物質的量變為原來2倍,則下列數值是原來2倍的有___________(填標號)。
A.平衡常數 B.達到平衡的時間
C.I2(g)的物質的量濃度 D.平衡時WI2(g)的體積分數
②工業上利用上述反應原理提純金屬鎢的示意圖如右:
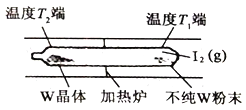
反應在真空石英管中進行,先在溫度為T1端放入不純W粉末和少量I2(g),一段時間后,在溫度為T2的一端得到純凈的晶體,則溫度T1___________T2(填:“>”、“<”或“=”)。
(4)寫出黑鎢礦中FeWO4在步驟Ⅰ中反應的化學方程式__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面有關試劑的保存正確的是
A.液氯通常保存在干燥的鋼瓶中
B.金屬鈉通常保存在四氯化碳中
C.鐵片通常保存在無色細口瓶中
D.硅酸鈉溶液通常保存在磨口玻璃塞的試劑瓶中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各物質的分類、名稱(或俗名)、化學式都正確的是( )
A.酸性氧化物 干冰 CO2
B.堿 純堿 Na2CO3
C.酸 硫酸 H2SO3
D.單質 氯水 Cl2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】香草醛是一種食品添加劑,可由愈創木酚作原料合成,合成路線如下:
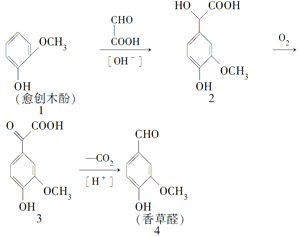
下列說法中正確的是( )
A. 反應1→2中原子利用率為90%
B. 檢驗制得的香草醛中是否混有化合物3,可用氯化鐵溶液
C. 化合物2在一定條件下可發生酯化反應
D. 等物質的量的四種化合物分別與足量NaOH溶液反應,消耗NaOH物質的量之比為1∶4∶3∶2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用工業冶煉硫酸銅(含有Fe2+、AsO2-、Ca2+等雜質)提純制備電鍍硫酸銅的生產流程如下:

已知:①Fe3+、Cu2+開始沉淀的pH分別2.7、5.4,完全沉淀的pH分別為3.7、6.4。
②Ksp[Cu(OH)2]=2×10-20
③AsO2-+H2O2+H+=H3AsO4, H3AsO4+Fe3+=FeAsO4↓+3H+
(1)溶解操作中需要配制含銅32 g·L-1的硫酸銅溶液1.0 L,需要稱量冶煉級硫酸銅的質量至少為___________g。
(2)測定溶解液中的Fe2+的濃度,可用KMnO4標準溶液滴定,取用KMnO4溶液應使用
________(“酸式”或“堿式”)滴定管,其中反應離子方程式為:______________________。若要檢驗調節pH后溶液中的Fe3+已除盡的方法是___________________________。
(3)氧化后需要將溶液進行稀釋及調節溶液的pH=5,則稀釋后的溶液中銅離子濃度最大不能超過____________mol·L-1。
(4)固體Ⅰ的主要成分除 FeAsO4 、Fe(OH)3外還有__________________,由溶液Ⅰ獲得CuSO4·H2O,需要經過________ 、____________、過濾、洗滌、干燥操作。
(5)利用以上電鍍級硫酸銅作為電解質溶液,電解粗銅(含鋅、銀、鉑雜質)制備純銅,寫出陽極發生的電極反應式:________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com