
【題目】銅是生活中常見的金屬,請回答下列問題:
(1)Cu不活潑,通常情況下不與稀硫酸反應,但向Cu和稀硫酸的混合物中滴入H2O2溶液后,溶液很快變藍色,試寫出該反應的離子方程式__________________________。
(2)將硫酸銅溶液和碳酸鈉溶液混合,會析出Cu2(OH)2CO3綠色固體,試寫出該反應的離子方程式_________________________________。
(3)火法煉銅的原理:Cu2S+O2![]() 2Cu+SO2,在該反應中每生成1 mol Cu,轉移________ mol e-。
2Cu+SO2,在該反應中每生成1 mol Cu,轉移________ mol e-。
(4)據報道,有一種細菌在有氧氣存在的酸性溶液中,可將黃銅礦CuFeS2氧化成硫酸鹽:4CuFeS2+2H2SO4+17O2===4CuSO4+2Fe2(SO4)3+2H2O。利用反應后的溶液,按如下流程可制備膽礬(CuSO4·5H2O):

①檢驗溶液B中Fe3+是否被除盡的實驗方法_____________________。
②在實驗室中,設計方案,從溶液B中提煉金屬銅(要求:方案只用一個反應來完成)。寫出方案中的化學方程式:___________________________。
③從溶液B中獲取膽礬的操作b是___________,____________,過濾,洗滌,干燥。
【答案】 Cu+H2O2+2H+=Cu2++2H2O 2Cu2++2CO32-+H2O=Cu2(OH)2CO3↓+CO2↑ 3 取樣,加KSCN,若變紅則含Fe3+,未被除盡;若不變紅,則除盡 CuSO4+Fe=Cu+FeSO4 蒸發濃縮 冷卻結晶
【解析】考查化學工藝流程,(1)滴入H2O2溶液后,溶液很快變藍色,說明Cu→Cu2+,H2O2作氧化劑,離子反應方程式為Cu+H2O2+2H+=Cu2++2H2O;(2)生成Cu2(OH)2CO3,部分Cu2+與CO32-發生雙水解反應,產生CO2,其離子反應方程式為:2Cu2++2CO32-+H2O=Cu2(OH)2CO3↓+CO2↑;(3)根據反應方程式,Cu2S中Cu的價態由+1→0價,化合價降低,S的價態由-2價→+4價,化合價升高,O的價態由0價→-2價,化合價降低,計算轉移電子物質的量,可以通過S進行計算,生成1molCu,則消耗0.5molCu2S,即轉移電子物質的量為0.5×6mol=3mol;(4)①檢驗是否Fe3+被除盡,一般用KSCN檢驗,如果溶液變紅,說明含有Fe3+,否則不含有,操作是:取樣,加KSCN,若變紅則含Fe3+,未被除盡;若不變紅,則除盡;②根據流程,溶液B中含有Cu2+,制備Cu,需要加入Fe,發生Fe+Cu2+=Cu+Fe2+;③得到膽礬,膽礬中含有結晶水,采用的是蒸發濃縮、冷卻結晶、過濾、干燥的方法。


科目:高中化學 來源: 題型:
【題目】對于反應中的能量變化,表述正確的是:
A. 氧化反應均為吸熱反應
B. 斷開化學鍵的過程會放出能量
C. 加熱才能發生的反應一定是吸熱反應
D. 放熱反應中,反應物的總能量大于生成物的總能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 1mol的硫蒸汽和硫固體分別完全燃燒,前者△H比后者小
B. 在101kPa時,1mol碳燃燒所放出的熱量為碳的燃燒熱
C. 由C(s,石墨)═C(s,金剛石);△H=+1.9kJmol-1 可知,金剛石比石墨穩定
D. 反應熱就是反應中放出的能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在常溫下,Fe與水并不起反應,但在高溫下,Fe與水蒸氣可發生反應用下列裝置,在硬質玻璃管中放入還原鐵粉和石棉絨的混合物,加熱,并通入水蒸氣,就可以完成高溫下“Fe與水蒸氣的反應實驗”.
請回答該實驗中的問題.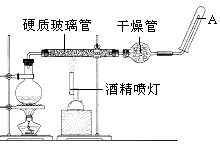
(1)寫出該反應的反應方程式:
(2)如何檢驗該裝置的氣密性
(3)圓底燒瓶中盛裝的水,該裝置受熱后的主要作用是;燒瓶底部放置了幾片碎瓷片,碎瓷片的作用是 .
(4)酒精燈和酒精噴燈點燃的順序是 , 為什么
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下反應最符合綠色化學原子經濟性要求的是( )
A. 用SiO2制備高純硅 B. 乙烯聚合為聚乙烯高分子材料
C. 工業煅燒石灰石制CaO D. 以銅和濃硝酸為原料生產硝酸銅
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是( )
A. 發酵粉中主要含有氫氧化鈉,能使焙制出的糕點疏松多孔
B. 碘鹽中的碘可以直接用淀粉檢驗
C. 硫酸氫鈉屬于鹽類,其水溶液顯中性
D. 碳酸氫鈉可以用于治療胃酸過多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素X、Y、Z、W的原子序數依次增大,X原子核外最外層電子數是其電子層數的2倍,X、Y的核電荷數之比為3:4。W-的最外層為8電子結構。金屬單質Z在空氣中燃燒生成的化合物可與水發生氧化還原反應。下列說法正確的是
A. 元素Y、Z的簡單離子的電子層結構不同
B. 原子半徑大小:r(X)<r(Y),r(Z)>r(W)
C. 化合物Z2Y和Z2XY3中都只存在離子鍵
D. 常溫下,W的單質與Z的最高價氧化物水化物的溶液反應生成兩種鹽
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com