
(1)對(duì)于下列反應(yīng):2SO2 + O2 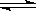 2SO3,如果2min內(nèi)SO2的濃度由6 mol/L下降為2 mol/L,那么,用SO2濃度變化來(lái)表示的化學(xué)反應(yīng)速率為_(kāi)___________,用O2濃度變化來(lái)表示的反應(yīng)速率為_(kāi)____________。
2SO3,如果2min內(nèi)SO2的濃度由6 mol/L下降為2 mol/L,那么,用SO2濃度變化來(lái)表示的化學(xué)反應(yīng)速率為_(kāi)___________,用O2濃度變化來(lái)表示的反應(yīng)速率為_(kāi)____________。
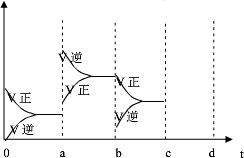
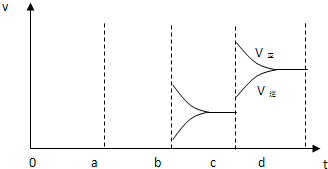
(2)右圖表示在密閉容器中反應(yīng):2SO2+O2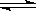 2SO3 △H<0達(dá)到平衡時(shí),由于條件改變而引起反應(yīng)速度和化學(xué)平衡的變化情況,
2SO3 △H<0達(dá)到平衡時(shí),由于條件改變而引起反應(yīng)速度和化學(xué)平衡的變化情況,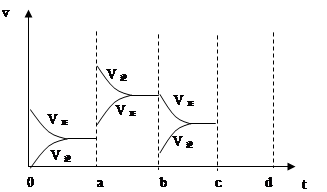
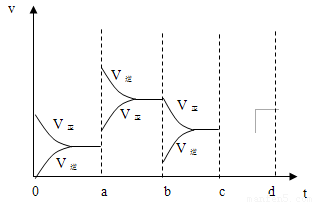
a b過(guò)程中改變的條件可能是 ;b c過(guò)程中改變的條件可能是 ; 若增大壓強(qiáng)時(shí),反應(yīng)速度變化情況畫在c~d處.
(3)請(qǐng)用化學(xué)平衡移動(dòng)知識(shí)解釋久置的氯水(尤其是長(zhǎng)期放置在見(jiàn)光環(huán)境),最后淺綠色消失,溶液變成稀鹽酸: .
(1)2mol/(L·min); 1mol/(L·min); (2)升溫;減小SO3濃度;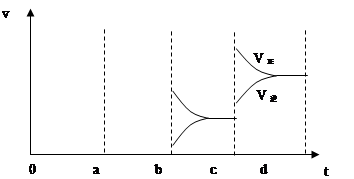
(3)在氯水中存在平衡:Cl2+H2O 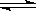 HCl + HClO ,HClO見(jiàn)光易分解為HCl和O2,使得平衡體系中HClO濃度減小,平衡向正反應(yīng)方向移動(dòng),Cl2濃度減小.HCl濃度增大,最后淺綠色消失,溶液變成稀鹽酸.
HCl + HClO ,HClO見(jiàn)光易分解為HCl和O2,使得平衡體系中HClO濃度減小,平衡向正反應(yīng)方向移動(dòng),Cl2濃度減小.HCl濃度增大,最后淺綠色消失,溶液變成稀鹽酸.
解析試題分析:(1)2min內(nèi)二氧化硫濃度變化為4mol/L,二氧化硫反應(yīng)速率為2 mol/(L·min),二氧化硫與氧氣速率比為2:1。(2) ab過(guò)程中反應(yīng)速率增大且平衡向逆反應(yīng)方向移動(dòng),所以改變的條件是升高溫度;bc過(guò)程中逆反應(yīng)速率突然減小、正反應(yīng)速率逐漸減小,所以改變的條件是改變濃度,平衡向右移動(dòng),所以改變的條件是減小生成物濃度;若增大壓強(qiáng),正、逆反應(yīng)速率均加快,但v(正)>v(逆),平衡向右移動(dòng)。(3)氯氣溶于水的反應(yīng)是可逆反應(yīng),氯水久置,HClO見(jiàn)光分解,次氯酸濃度減少,平衡向右移動(dòng),氯氣濃度減小,鹽酸濃度增大,最終變?yōu)橄←}酸。
考點(diǎn):化學(xué)反應(yīng)速率計(jì)算 化學(xué)反應(yīng)速率圖像 勒沙特列原理
點(diǎn)評(píng):觀察v-t圖像時(shí),若增加或減小物質(zhì)的濃度,則新、舊平衡速率連續(xù);若改變溫度、壓強(qiáng)、使用催化劑,則正、逆反應(yīng)速率同時(shí)變化,根據(jù)v(正)與v(逆)的相對(duì)大小判斷平衡移動(dòng)的方向。



| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來(lái)源: 題型:

查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:

查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
 (1)對(duì)于下列反應(yīng):2SO2+O2?2SO3,如果2min內(nèi)SO2的濃度由6mol/L下降為2mol/L,那么,用SO2濃度變化來(lái)表示的化學(xué)反應(yīng)速率為
(1)對(duì)于下列反應(yīng):2SO2+O2?2SO3,如果2min內(nèi)SO2的濃度由6mol/L下降為2mol/L,那么,用SO2濃度變化來(lái)表示的化學(xué)反應(yīng)速率為查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
已知:H+(aq) + OH-(aq) = H2O(l) △H =-57.3 kJ·mol-1。
對(duì)于下列反應(yīng):
①HCl(aq) + NH3·H2O(aq) = NH4Cl(aq) + H2O(l) △H=-a kJ·mol-1
②HNO3(aq) + KOH(aq) = KNO3(aq) + H2O(l) △H =-b kJ·mol-1[
則a、b的大小關(guān)系為
A.a(chǎn)>b B.b>a C.a(chǎn) = b D.無(wú)法比較
查看答案和解析>>
科目:高中化學(xué) 來(lái)源:2013屆廣東省廣州市高二上學(xué)期期中考試化學(xué)(理)試卷 題型:填空題
(1)對(duì)于下列反應(yīng):2SO2
+ O2 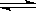 2SO3 , 如果2min內(nèi)SO2的濃度由6 mol/L下降為2 mol/L,那么,用SO2濃度變化來(lái)表示的化學(xué)反應(yīng)速率為_(kāi)___________,用O2濃度變化來(lái)表示的反應(yīng)速率為_(kāi)____________。
2SO3 , 如果2min內(nèi)SO2的濃度由6 mol/L下降為2 mol/L,那么,用SO2濃度變化來(lái)表示的化學(xué)反應(yīng)速率為_(kāi)___________,用O2濃度變化來(lái)表示的反應(yīng)速率為_(kāi)____________。
(2)下圖表示在密閉容器中反應(yīng):2SO2+O2 2SO3 △H<0達(dá)到平衡時(shí),由于條件改變而引起反應(yīng)速度和化學(xué)平衡的變化情況,a b過(guò)程中改變的條件可能是
;b c過(guò)程中改變的條件可能是
; 若增大壓強(qiáng)時(shí),反應(yīng)速度變化情況畫在c~d處.
2SO3 △H<0達(dá)到平衡時(shí),由于條件改變而引起反應(yīng)速度和化學(xué)平衡的變化情況,a b過(guò)程中改變的條件可能是
;b c過(guò)程中改變的條件可能是
; 若增大壓強(qiáng)時(shí),反應(yīng)速度變化情況畫在c~d處.
(3)請(qǐng)用化學(xué)平衡移動(dòng)知識(shí)解釋久置的氯水(尤其是長(zhǎng)期放置在見(jiàn)光環(huán)境),最后淺綠色消失,溶液變成稀鹽酸:
查看答案和解析>>
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com