
| 難溶電解質 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
分析 ①中為了不引入其他雜質離子,應加氨水使Fe3+沉淀,而不能用氫氧化鈉溶液;
②中根據溶解度表可知Mg(OH)2易轉化為Fe(OH)3,因此在氯化鎂溶液中加入足量的Mg(OH)2可除去Fe3+;
③由于Fe(OH)2的溶解度大于Fe(OH)3,所以一般將Fe2+先氧化成Fe3+,再調節溶液的pH=4,形成Fe(OH)3沉淀;
(1)Fe(OH)2的溶解度大于Fe(OH)3,上述三個除雜方案都能夠達到很好的效果,Fe2+、Fe3+都被轉化為Fe(OH)3而除去;
(2)加入試劑注意不能引入新的雜質;
(3)根據題干信息結合難溶電解質的溶解度進行分析出反應物和生成物;
(4)A.H2O2是綠色氧化劑,在氧化過程中不引進雜質、不產生污染;
B.Fe(OH)2的溶解度大于Fe(OH)3,形成Fe(OH)2沉淀Fe2+沉淀不完全;
C.加入的氫氧化銅或堿式碳酸銅可以與H+反應,導致溶液的pH增大,當pH=4的時候,Fe(OH)3完全沉淀,而Cu2+還沒沉淀,且加入氫氧化銅或堿式碳酸銅是固體,不會引入新的雜質;
D.pH=4的溶液中,Cu2+可以大量存在,而氫氧化銅或堿式碳酸銅是固體,不會引入新的雜質;
E.在pH>4的溶液中Fe3+全部以Fe(OH)3完全沉淀.
解答 解:(1)①中為了不引入其它雜質離子,應加氨水使Fe3+沉淀,生成Fe(OH)3,如用氫氧化鈉溶液進行沉淀,則沉淀表面含鈉離子和氫氧根離子,所以不用;
②根據溶解度表可知Mg(OH)2易轉化為Fe(OH)3,因此在氯化鎂溶液中加入足量的Mg(OH)2可除去Fe3+,;
③由于Fe(OH)2的溶解度大于Fe(OH)3,所以一般將Fe2+先氧化成Fe3+,再調節溶液的pH=4,形成Fe(OH)3沉淀,
故答案為:Fe(OH)3;
(2)①用氫氧化鈉溶液,會引入新的雜質,沉淀表面含鈉離子和氫氧根離子,為了不引入其它雜質離子,應加氨水使Fe3+沉淀,
故答案為:氨水;不會引入新的雜質;
(3)②中根據溶解度表可知Mg(OH)2易轉化為Fe(OH)3,因此在氯化鎂溶液中加入足量的Mg(OH)2可除去Fe3+:2Fe3++3Mg(OH)2=3Mg2++2Fe(OH)3,故答案為:2Fe3++3Mg(OH)2=3Mg2++2Fe(OH)3;
(4)A.根據H2O2是綠色氧化劑,在氧化過程中被還原成水,不引進雜質、不產生污染,故A正確;
B.根據Fe(OH)2的溶解度大于Fe(OH)3,形成Fe(OH)2沉淀Fe2+沉淀不完全,故B錯誤;
C.原來溶液是酸性較強,加入氫氧化銅或堿式碳酸銅可以與H+反應.H+反應后,PH增大,當PH=4的時候,Fe(OH)3完全沉淀,而Cu2+還沒沉淀.而氫氧化銅或堿式碳酸銅是固體,不會引入新的雜質,故C正確;
D.氫氧化銅或堿式碳酸銅與H+反應,H+反應后,PH增大,當PH=4的時候,Fe(OH)3完全沉淀,而Cu2+還沒沉淀,以Cu2+形式存在,而氫氧化銅或堿式碳酸銅是固體,不會引入新的雜質,故D正確;
E.在pH>4的溶液中Fe3+全部以Fe(OH)3完全沉淀,則Fe3+一定不能大量存在,故E正確;
故選:ACDE.
點評 本題主要考查物質的分離、提純,涉及難溶物溶解平衡及其沉淀轉化的實質,題目難度中等,明確鐵的化合物的性質靈活運用題目信息是解題的關鍵,注意掌握難溶物溶解平衡及其影響.


 輕松暑假總復習系列答案
輕松暑假總復習系列答案科目:高中化學 來源: 題型:選擇題
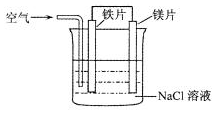
| A. | 鎂片為負極,鎂片上產生黃綠色氣體 | |
| B. | 鐵片為陽極,鐵片上產生無色氣體 | |
| C. | 溶液中鐵片與鎂片之間產生白色沉淀 | |
| D. | 溶液的pH將逐漸增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁制槽車可用來貯運濃硫酸、濃硝酸是因為常溫下鋁和濃硫酸、濃硝酸不反應 | |
| B. | 兩份相同質量的鋁粉,分別與足量的稀硫酸和氫氧化鈉溶液反應,產生的氫氣前者多 | |
| C. | 合金的熔點一般比組成它的各成分的熔點都高 | |
| D. | 工業上常利用鋁熱反應冶煉難熔金屬,如釩、鉻、錳 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
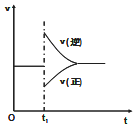 在一定條件下,向一帶活塞的密閉容器中充入2mol A和1mol B,發生下列反應:
在一定條件下,向一帶活塞的密閉容器中充入2mol A和1mol B,發生下列反應:| A. | 保持壓強不變,升高反應溫度 | |
| B. | 保持溫度不變,增大容器體積 | |
| C. | 保持溫度和容器體積不變,充入1 mol C(g) | |
| D. | 保持溫度和壓強不變,充入1 mol C(g) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
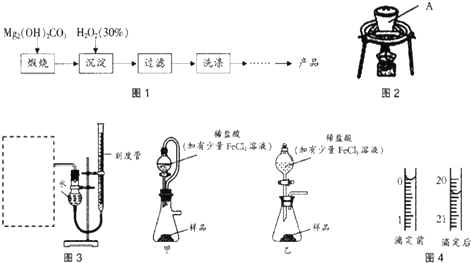
| 實驗編號 | 煅燒溫度(℃) | 煅燒時間(h) |
| ① | 550 | 2 |
| ② | 600 | 1 |
| ③ | 650 | 2 |
| ④ | 700 | 3 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
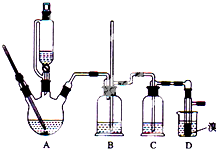 實驗室用少量的溴和足量的乙醇制備1,2-二溴乙烷的裝置如圖所示(加熱及夾持裝置省略):
實驗室用少量的溴和足量的乙醇制備1,2-二溴乙烷的裝置如圖所示(加熱及夾持裝置省略):| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 狀態 | 色液體 | 無色液體 | 無色液體 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸點/℃ | 78.5 | 132 | 34.6 |
| 熔點/℃ | -l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
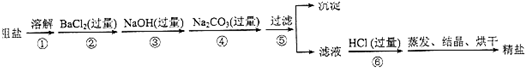
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶液pH:NaF>NaCN | B. | n1>n2 | ||
| C. | H2O的電離程度:NaF>NaCN | D. | c(F-)<c(CN-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com