
| A. | 加熱蒸干Na2CO3溶液,最后可以得到NaOH和Na2CO3的混合固體 | |
| B. | 除去MgCl2中的Fe3+,可以加入NaOH固體 | |
| C. | 明礬凈水的反應:Al3++3H2O?Al(OH)3(膠體)+3H+ | |
| D. | 加熱蒸干KCl溶液,最后得到KOH固體(不考慮CO2的反應) |
分析 A.Na2CO3水解生成的碳酸氫鈉和NaOH,由于生成的氫氧化鈉不具有揮發性,氫氧化鈉與碳酸氫鈉反應生成碳酸鈉;
B.鎂離子、鐵離子均能與氫氧化鈉反應;
C.鋁離子水解生成的氫氧化鋁膠體具有吸附性;
D.KCl在溶液中不水解.
解答 解:A.Na2CO3在溶液中水解生成碳酸氫鈉和氫氧化鈉,水解方程式為:Na2CO3+H2O?NaOH+NaHCO3,由于生成的NaOH不揮發,氫氧化鈉能夠與碳酸氫鈉發生中和反應生成碳酸鈉和水,所以將Na2CO3溶液加熱蒸發后最終得到的固體仍然為Na2CO3,故A錯誤;
B.鎂離子、鐵離子均能與氫氧化鈉反應,所以加NaOH不能除去MgCl2中的Fe3+,故B錯誤;
C.明礬在水中電離出鋁離子,鋁離子水解生成的氫氧化鋁膠體具有吸附性,即Al3++3H2O?Al(OH)3(膠體)+3H+,故C正確;
D.KCl在溶液中不水解,加熱蒸干KCl溶液,最后得到KCl固體,故D錯誤.
故選C.
點評 本題考查了鹽的水解原理及其應用,題目難度不大,試題側重基礎知識的考查,注意掌握鹽的水解原理及其應用方法,試題有利于培養學生靈活應用所學知識的能力.


科目:高中化學 來源: 題型:選擇題
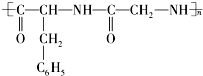 的單體是( )
的單體是( )| A. | ①③ | B. | ③④ | C. | ②③ | D. | ①② |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
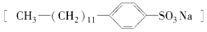 是常用洗滌劑的主要成分.其結構可用圖形
是常用洗滌劑的主要成分.其結構可用圖形 來表示,•端為鏈烴基,O端為極性基.根據這一結構特點,試分析和回答下列問題:
來表示,•端為鏈烴基,O端為極性基.根據這一結構特點,試分析和回答下列問題: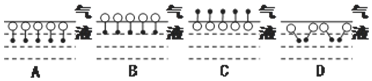
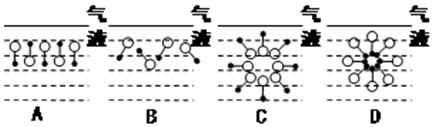
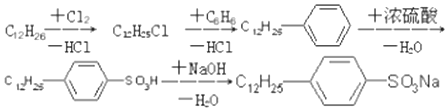
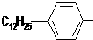 .
.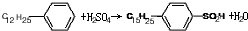 ,反應類型為取代反應.
,反應類型為取代反應.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
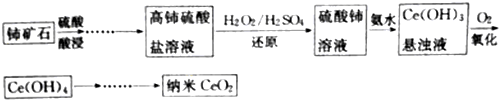
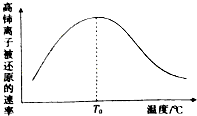
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
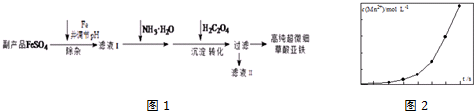
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
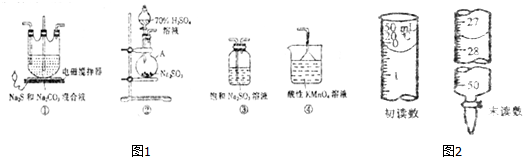

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com