
【題目】如圖是銅-鋅原電池示意圖。下列有關該原電池的描述中正確的是( )

A.鋅片作正極,不斷溶解
B.銅片作負極,有氣泡產生
C.負極反應:Zn2++2e-=Zn
D.正極反應:2H++2e-=H2↑
科目:高中化學 來源: 題型:
【題目】雙氧水在醫療、軍事和工業上用途廣泛,工業上合成雙氧水的方法有多種,其中一種合成工藝為乙基蒽醌(EAQ)法。
已知:
①反應原理為
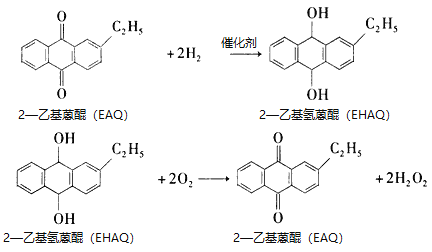
②工業制備流程如圖所示。
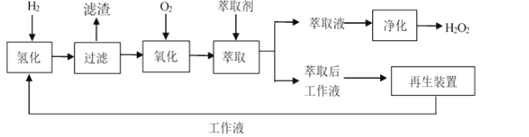
③制備過程中,將EAQ溶于有機溶劑中配制成工作液。
請回答下列問題:
(1)該流程中,循環使用的原料為___。
(2)現有甲、乙、丙三種有機溶劑,相關物質的溶解情況如表所示,則配制工作液時,應選用有機溶劑__(填“甲”“乙”或“丙”),原因為___。
物質 | 甲 | 乙 | 丙 |
EAQ | 互溶 | 不溶 | 互溶 |
EHAQ | 互溶 | 不溶 | 互溶 |
H2O2 | 不溶 | 不溶 | 互溶 |
H2O | 不溶 | 不溶 | 互溶 |
(3)“氧化”時,控制溫度為45~55℃,原因為___。
(4)“萃取”時,所選用的萃取劑是一種常見的溶劑,其化學名稱為__,選用該溶劑作為萃取劑的原因為__。
(5)“凈化”的目的是將萃取液中的過氧化氫分離出來,則應選用的分離方法為___。
(6)采用電解法制備雙氧水的裝置示意圖如圖所示,通入空氣的電極的電極反應式___。
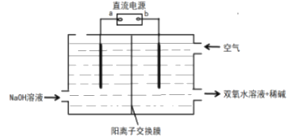
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1,2-丙二醇脫氧脫水反應的催化循環機理如下圖所示。

下列說法不正確的是
A. 產物CH2=CHCH3不存在順反異構
B. 過程②中有O—H鍵發生斷裂
C. 過程③④中均有C—C鍵發生斷裂
D. 該反應方程式為:2CH2(OH)CH(OH)CH3![]() HCHO+CH3CHO+CH2=CHCH3+2H2O
HCHO+CH3CHO+CH2=CHCH3+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下反應2SO2(g)+O2(g)![]() 2SO3(g)在恒容密閉容器中進行,從反應開始至10s時,O2的濃度減少了0.3 mol·L-1。則0~10s內平均反應速率為
2SO3(g)在恒容密閉容器中進行,從反應開始至10s時,O2的濃度減少了0.3 mol·L-1。則0~10s內平均反應速率為
A. ![]()
B. ![]()
C. ![]()
D. ![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生用如圖所示裝置做濃硫酸和蔗糖反應的實驗。下列有關實驗操作或敘述錯誤的是( )

A.打開A中分液漏斗活塞,加入濃硫酸,充分反應后燒瓶內出現黑色膨化固體
B.品紅溶液紅色褪去,證明有SO2氣體生成
C.檢驗A中產生的氣體中含有水蒸氣,應將E接在A和B之間
D.D中溶液變渾濁,即可證明反應產生了CO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】人類利用能源經歷了三個時期。
(1)柴草時期:從能量轉化的角度看,木材燃燒時化學能主要轉化成__能和光能。
(2)化石能源時期:天然氣的主要成分是甲烷。甲烷的電子式為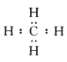 ,其化學鍵類型是__(選填“離子鍵”或“共價鍵”)
,其化學鍵類型是__(選填“離子鍵”或“共價鍵”)
(3)石油化工生產可以合成某有機物,其分子球棍模型如圖所示。
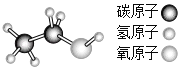
據此寫出該物質的結構式或結構簡式__。
(4)多能源結構時期:基于環保理念,將逐步減少傳統燃油汽車的使用,燃料電池汽車將有更廣闊的發展前景。下圖為氫氧燃料電池的示意圖,其基本工作原理與銅鋅原電池相同。

根據圖中電子流動方向判斷A電極是__(選填“正極”或“負極”);氫氧燃料電池的優點是__(寫一條即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知電導率越大導電能力越強。常溫下用0.100mol·L-1 NaOH溶液分別滴定10.00 mL 濃度均為0.100 mol·L-1的鹽酸和醋酸溶液,測得滴定過程中溶液的電導率如圖所示:
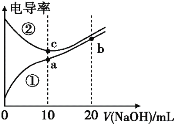
下列說法正確的是
A.曲線②代表滴定鹽酸的曲線
B.滴定醋酸的過程應該選擇甲基橙作為指示劑
C.a、b、c三點溶液中水的電離程度:a>c>b
D.b點溶液中:c(OH-)=c(H+)+c(CH3COO-)+ c(CH3COOH)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】燃煤產生的煙氣中含有較多的CO2、CO、SO2等影響環境的氣體。如何綜合利用這些氣體一直是科研單位研究的熱點。
(1)已知:2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g) ΔH1
CO(g)+H2O(g)CO2(g)+H2(g) ΔH2
2CO(g)+4H2(g)CH3OCH3(g)+H2O(g) ΔH3
用ΔH2、ΔH3表示ΔH1,ΔH1=_________。
(2)針對CO2與H2反應轉化為二甲醚(g)和H2O(g),研究發現,該反應中CO2的平衡轉化率隨反應溫度、投料比[n(H2)/n(CO2)]的變化曲線如圖:
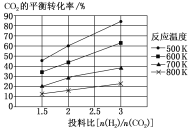
①ΔH1________(填“>”或“<”)0。
②若其他條件不變,僅僅增大壓強,則逆反應速率會________(填“增大”“減小”或“不變”,下同),平衡常數K會________。
(3)研究發現,催化劑可以促使煙氣CO、SO2轉化為CO2、S。反應原理為2CO(g)+SO2(g)2CO2(g)+S(l) ΔH=-270 kJ·mol-1。
①其他條件相同,研究發現,分別選取Fe2O3、NiO、Cr2O3作上述反應的催化劑時,SO2的轉化率隨反應溫度的變化如圖,研究得出,應該選擇Fe2O3作催化劑,主要原因可能是________________
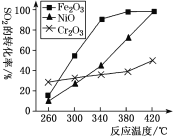
②若在2 L恒容密閉容器中,將3mol CO、1 mol SO2混合,在一定條件下引發反應,當SO2的平衡轉化率為40%時,此時K=________。
③向反應容器中再分別通入下列氣體,可以使SO2轉化率增大的是_____(填字母)。
A.CO B.SO2 C.N2 D.H2S E.CO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度為T時,向2.0 L恒容密閉容器中充入1.0 mol PCl5,發生反應:PCl5(g)![]() PCl3(g)+Cl2(g) ΔH=a kJ·mol-1(a>0)。0~10 min保持容器溫度不變,10 min時改變一種條件,整個過程中PCl5、PCl3、Cl2的物質的量隨時間的變化如圖所示。
PCl3(g)+Cl2(g) ΔH=a kJ·mol-1(a>0)。0~10 min保持容器溫度不變,10 min時改變一種條件,整個過程中PCl5、PCl3、Cl2的物質的量隨時間的變化如圖所示。
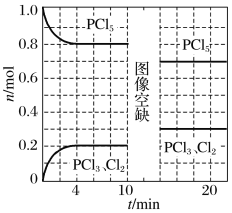
下列說法正確的是
A.0~4 min的平均速率v(PCl3)=0.025 mol·L-1·min-1
B.10 min時改變的條件是增加了一定量的PCl5
C.若起始時向該容器中充入2.0 mol PCl3和2.0 mol Cl2,保持溫度為T,反應達平衡時放出的熱量小于1.6a kJ
D.溫度為T,起始時向該容器中充入1.0 mol PCl5、0.10 mol PCl3和0.10 mol Cl2,反應達到平衡前v正<v逆
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com