
| A. | 銅鋅原電池中銅是正極 | B. | 用電解法精煉粗銅時粗銅做陽極 | ||
| C. | 在鍍件上鍍銅時可用金屬銅做陽極 | D. | 電解水制H2、O2時銅做陽極 |
分析 A.銅鋅原電池中,鋅易失電子而作負極,銅作正極;
B.電解精煉粗銅時,粗銅作陽極;
C.電鍍時,鍍層作陽極,鍍件作陰極;
D.陽極上銅失電子生成銅離子.
解答 解:A.銅鋅原電池中,鋅易失電子發生氧化反應而作負極,銅作正極,正極上得電子發生還原反應,故A正確;
B.電解精煉粗銅時,粗銅作陽極,純銅作陰極,故B正確;
C.電鍍時,鍍層作陽極,鍍件作陰極,所以在鍍件上電鍍銅時,銅作陽極,鍍件作陰極,故C正確;
D.電解水制H2、O2時,銅不能做陽極,銅作陽極,銅失電子,陽極上得不到氧氣,故D錯誤;
故選D.
點評 本題考查了原電池和電解池原理,題目難度不大,明確各個電極上得失電子是解本題關鍵,注意活潑金屬作電解池陽極時,金屬失電子而不是溶液中陰離子失電子,為易錯點.


科目:高中化學 來源: 題型:選擇題
| A. | 將Al條投入NaOH溶液中:Al+4OH-=AlO2-+2H2O | |
| B. | 銅溶于濃硫酸中并加熱:Cu+4H++SO42-$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO2↑+2H2O | |
| C. | 碳酸氫鈣溶液中加入少量氫氧化鈣溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| D. | 向碳酸鈉溶液中逐滴加入與之等體積等物質的量濃度的稀硫酸:CO32-+H+=HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K(HF)=c(F-)?c(H+)/c(HF ) | B. | K(HNO2)=7.2×10-4 | ||
| C. | 酸性強弱為 HF>HNO2 | D. | K(HNO2)<K(HF) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④⑤ | B. | 只有①④ | C. | 只有②③ | D. | 只有③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增大反應物濃度,可增大單位體積內活化分子的百分數,從而增大有效碰撞的次數 | |
| B. | 有氣體參加的化學反應,若增大壓強(即縮小反應容器的體積),可增加活化分子的百分數,從而使反應速率增大 | |
| C. | 升高溫度能使化學反應速率增大,主要原因是增加了反應物分子中活化分子的百分數 | |
| D. | 催化劑不影響反應活化能但能增大單位體積內活化分子的百分數,從而增大反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在CH3COONa 溶液中滴入無色酚酞,溶液變紅:CH3COO-+H2O?CH3COOH+OH- | |
| B. | 在Mg(OH)2白色懸濁液中滴入飽和FeCl3溶液,懸濁液變紅褐:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| C. | 在NaHSO3溶液中滴加紫色石蕊溶液,溶液變紅:NaHSO3=Na++H++SO32- | |
| D. | 在草酸溶液中滴入幾滴稀H2SO4酸化的KMnO4溶液,溶液無色:2MnO4-+5H2C2O4+6H +=2Mn2++10CO2↑+8H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 我國規定:室內甲醛含量不得超過0.08mg•m-3.某研究性學習小組欲利用酸性KMnO4溶液測定空氣中甲醛的含量,請你協助他們完成相關學習任務.(部分裝置如圖),其反應原理及步驟如下:
我國規定:室內甲醛含量不得超過0.08mg•m-3.某研究性學習小組欲利用酸性KMnO4溶液測定空氣中甲醛的含量,請你協助他們完成相關學習任務.(部分裝置如圖),其反應原理及步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ag得到電子 | B. | X為AgS | ||
| C. | O2被還原 | D. | 每生成1 mo1X轉移電子數4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
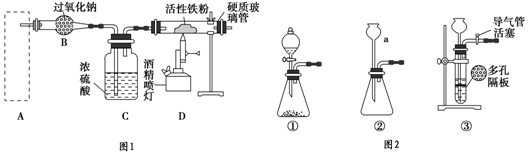
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com