
【題目】依據信息寫出下列反應的方程式或填充合適的物質。
⑴氫氧化銦[In(OH)3]廣泛應用于電子行業。以氧化銦廢渣(主要含In2O3和Fe3O4)為原料制備氫氧化銦的一種工藝流程如下:
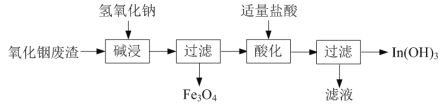
已知:In2O3為兩性氧化物,在強堿性條件下In元素以InO33-離子形式存在。
①寫出“堿浸”時反應的離子方程式:______。
②寫出“酸化”時反應的離子方程式:______。
⑵下表所示為部分酸的電離平衡常數:
酸 | H2SO3 | CH3COOH | HCOOH |
電離平衡常數 | Ka1=1.2×10-2 Ka2=5.6×10-8 | 1.75×10-5 | 1.8×10-4 |
從H2SO3、CH3COOH中選擇合適的物質,以實現HCOONa→HCOOH的轉化,寫出該反應的離子方程式:______。
⑶下表所示為部分物質的溶度積常數:
難溶物 | Mn(OH)2 | Co(OH)2 | MnCO3 |
溶度積常數 | 2×10-13 | 5.9×10-15 | 2.2×10-11 |
①從NaOH、Co(OH)2中選取合適的物質,填在如下轉化關系中:MnCl2→Mn(OH)2。______
②NaNO3、Na2CO3中選擇合適的物質,填在如下轉化關系中:MnCl2→NaCl。_______
【答案】In2O3+6OH-=2InO33-+3H2O InO33-+6H+===In(OH)3 HCOO-+H2SO3=== HCOOH+HSO3- NaOH Na2CO3
【解析】
(1)氧化銦廢渣(主要含In2O3和Fe3O4)堿浸發生In2O3+6OH-=2InO33-+3H2O,過濾除去Fe3O4,濾液中加鹽酸酸化,轉化成In(OH)3;
(2)根據電離平衡常數判斷酸性強弱;
(3)根據溶度積判斷。
(1)①In2O3為兩性氧化物,在強堿性條件下In元素以InO33-離子形式存在,“堿浸”時反應的離子方程式:In2O3+6OH-=2InO33-+3H2O;
②InO33-鹽酸化后生成In(OH)3,“酸化”時反應的離子方程式:InO33-+6H+===In(OH)3;
(2)電離平衡常數越大,酸性越大,酸性:H2SO3>HCOOH>CH3COOH>HSO3-,實現HCOONa→HCOOH的轉化,只有通入SO2,該反應的離子方程式:HCOO-+H2SO3=== HCOOH+HSO3-;
(3)Mn(OH)2是難溶物質,MnCl2+2NaOH→Mn(OH)2↓+2NaCl,Co(OH)2比Mn(OH)2更難溶,故選NaOH;
MnCO3難溶,MnCl2+Na2CO3=MnCO3↓+2NaCl,Mn(NO3)2易溶,不能用NaNO3,故選Na2CO3。


科目:高中化學 來源: 題型:
【題目】下列說法中正確的是( )
A.22.4L CO2與足量Na2O2反應轉移的電子數為NA
B.1mol·L-1的NaOH溶液中含Na+數目為NA
C.78gNa2O2晶體中含有的陰離子數目為2NA
D.a g CO和H2的混合氣體充分燃燒的產物與足量的Na2O2充分反應后,固體質量增加ag
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 用途廣泛。某探究小組同學以廢銅屑(含雜質鐵)為原料,在實驗室用如圖所示裝置制取硫酸銅,再進一步從所得溶液中獲得無水硫酸銅。
用途廣泛。某探究小組同學以廢銅屑(含雜質鐵)為原料,在實驗室用如圖所示裝置制取硫酸銅,再進一步從所得溶液中獲得無水硫酸銅。

Ⅰ.制備![]() 晶體
晶體
(1)儀器M名稱為________。
(2)將反應溫度控制在70℃-80℃,可采用的加熱方法是________。
(3)從反應后的混合溶液中獲得硫酸銅晶體的操作步驟如下:
①向溶液中加入________(填標號)至稀溶液pH約為4,過濾。
a. CuO b. NaOH溶液 c.![]()
②將濾液________、________(填操作名稱)過濾、用乙醇洗滌、低溫干燥,得![]() 晶體。
晶體。
(4)用乙醇代替蒸餾水洗滌晶體的目的是________,并縮短干燥所需時間。
Ⅱ.制備無水![]()
(5)灼燒法:實驗室可在________(填儀器名稱)中灼燒![]() ,晶體制備無水
,晶體制備無水![]() 。
。
(6)![]() 法:該方案采用如下圖裝置,________(填操作名稱)A使
法:該方案采用如下圖裝置,________(填操作名稱)A使![]() 氣體進入裝有
氣體進入裝有![]() 晶體的硬質玻璃管(已知:
晶體的硬質玻璃管(已知:![]() 的熔點為-105℃、沸點為76℃、遇水劇烈水解生成兩種酸性氣體)。裝置B中
的熔點為-105℃、沸點為76℃、遇水劇烈水解生成兩種酸性氣體)。裝置B中![]() 和
和![]() 發生反應的化學方程式為________。
發生反應的化學方程式為________。
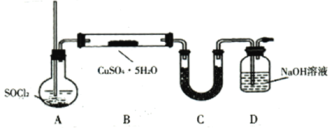
(7)![]() 法:相對灼燒法的優點為________________。(寫出一點即可)
法:相對灼燒法的優點為________________。(寫出一點即可)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有氯化鈉和碘化鈉的混合物共26.7 g,溶于水,通入足量氯氣后,蒸干、灼燒,固體質量變為 17.55 g。
(1)原混合物中碘化鈉的質量是________。
(2)原混合物中氯化鈉的質量分數是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下列四種物質的溶液:①Na2CO3 ②Al2(SO4)3 ③CH3COOH ④NaHCO3。
(1)寫出①溶液的電荷守恒:____________。
(2)常溫下,0.1 mol·L-1④溶液的pH大于8,則溶液中c(H2CO3)_____c(CO32-)(填“>”、“=”或“<”),原因是_______(用離子方程式和必要的文字說明)。
(3)常溫下0.1 mol/L的③溶液加水稀釋過程中,下列表達式的數據一定變大的是_________。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
(4)用②和④的溶液可以制作泡沫滅火劑,其原理為:________________(用離子方程式解釋)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 是元素周期表中前四周期的元素,各周期至少含有一種元素,且原子序數依次增大。
是元素周期表中前四周期的元素,各周期至少含有一種元素,且原子序數依次增大。![]() 、
、![]() 、
、![]() 三種元素原子的最外層電子數相同,
三種元素原子的最外層電子數相同,![]() 與
與![]() 能夠形成原子之比為
能夠形成原子之比為![]() 的化合物
的化合物![]() ,
,![]() 是前四周期基態原子含有未成對電子數目最多的元素,
是前四周期基態原子含有未成對電子數目最多的元素,![]() 與
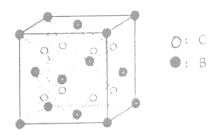
與![]() 形成的晶體
形成的晶體![]() 結構如圖所示。試用元素符號回答下列問題:
結構如圖所示。試用元素符號回答下列問題:
(1)![]() 、
、![]() 、
、![]() 三種元素的電負性由大到小的順序為_______。
三種元素的電負性由大到小的順序為_______。
(2)![]() 與
與![]() 兩種元素能夠形成兩種常見的化合物,則在這兩種化合物分子中,原子的雜化方式分別為______和______,且這兩種分子____(填選項)。
兩種元素能夠形成兩種常見的化合物,則在這兩種化合物分子中,原子的雜化方式分別為______和______,且這兩種分子____(填選項)。
A 都是極性分子 B 都是非極性分子 C 其中一種是極性分子另一種是非極性分子
(3)![]() 元素處于周期表的____區,其單質晶體堆積模型的名稱為_____。
元素處于周期表的____區,其單質晶體堆積模型的名稱為_____。
(4)![]() 元素的基態原子價層電子排布圖為______。
元素的基態原子價層電子排布圖為______。
(5)已知![]() 能溶于某濃度的硝酸中,得到藍色溶液的同時,會逸出一種與
能溶于某濃度的硝酸中,得到藍色溶液的同時,會逸出一種與![]() 互為等電子體的純凈氣體,則該反應的化學方程式為_____。經研究證實,所得溶液呈藍色,是因為溶液中含有由
互為等電子體的純凈氣體,則該反應的化學方程式為_____。經研究證實,所得溶液呈藍色,是因為溶液中含有由![]() 、
、![]() 、
、![]() 三種元素形成的一種配位離子,試寫出該離子的結構式______。
三種元素形成的一種配位離子,試寫出該離子的結構式______。
(6)由晶體![]() 的晶胞可知,
的晶胞可知,![]() 離子呈簡單立方堆積模型,形成立方體空隙,則
離子呈簡單立方堆積模型,形成立方體空隙,則![]() 離子對這些立方體空隙的填充率為_____
離子對這些立方體空隙的填充率為_____![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有四種短周期元素A、B、C、D,它們的核電荷數依次增大。A與C,B與D分別是同主族元素。B、D質子數之和是A、C質子數之和的2倍。這四種元素中A、C、D的單質均可在B的單質中燃燒。
(1)A的元素名稱是________,C的元素符號是________。
(2)D元素位于元素周期表的第______周期第______族。
(3)C元素的單質在B的單質中燃燒的產物的化學式是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵是地球表面最豐富的金屬之一,其合金、化合物具有廣泛用途。
⑴Fe3+可以與SCN-、CN-、有機分子等形成配合物。基態Fe3+的電子排布式為______;與SCN-互為等電子體且為非極性分子的化學式為______。
⑵化合物FeCl3是棕色固體、易潮解、100℃左右時升華,它的晶體類型是______。
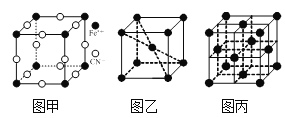
⑶普魯士藍俗稱鐵藍,結構如圖甲所示(K+未畫出),平均每兩個立方體中含有一個K+,該晶體的化學式為______。又知該晶體中鐵元素有+2價和+3價兩種,則Fe3+與Fe2+的個數比為______。
⑷在一定條件下鐵形成的晶體的基本結構單元如圖乙和圖丙所示,則圖乙和圖丙的結構中鐵原子的配位數之比為______,兩種晶體中空間利用率較高的是______。(填“圖乙”或“圖丙”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年10月27日,國際清潔能源會議(ICCE2019)在北京開幕。一碳化學成為這次會議的重要議程。甲醇、甲醛(HCHO) 等一碳化合物在化工 、醫藥,能源等方面都有著廣泛的應用。
(1)甲醇脫氫法可制備甲醛(反應體系中各物質均為氣態),反應生成 1mol HCHO過程中能量變化如圖1。

已知:CO2(g)+3H2(g)=CH3OH(g) +H2O(g) △H=-49.5kJ mo1-1,則反應CO2(g)+2H2(g)= HCHO(g) +H2O(g) △H= ___________kJ mo1-1。
(2)氧化劑可處理甲醛污染,結合圖2分析春季(水溫約為15℃)應急處理被甲醛污染的水源應選擇的試劑為__________(填化學式)。

(3)納米二氧化鈦催化劑可用于工業上合成甲醇,CO2(g)+2H2(g)![]() CH3OH(g) △H=akJmo1-1
CH3OH(g) △H=akJmo1-1
①按![]() =2,投料比將H2與CO充入VL恒容密閉容器中,在一定條件下發生反應測定CO的平衡轉化率與溫度、壓強的關系如圖3所示。則a _____(填“>”或“<”)0;壓強p1、p2、p3由小到大的關系是__________________。
=2,投料比將H2與CO充入VL恒容密閉容器中,在一定條件下發生反應測定CO的平衡轉化率與溫度、壓強的關系如圖3所示。則a _____(填“>”或“<”)0;壓強p1、p2、p3由小到大的關系是__________________。

②在溫度為T1℃,向某恒容密閉容器中充入 H2和CO發生上述反應,起始時c(H2)=c(CO)=2.0 mo1L-1。達到平衡時,CO的轉化率為圖3中的 M 點對應的轉化率,則在該溫度下,對應的N 點的平衡常數為__________(保留3 位有效數字)。
(4)工業上利用CH4(CO和H2)與水蒸氣在一定條件下制取 H2:CH4(g) +H2O(g)![]() CO(g)+3H2(g) △H=+203kJmo1-1,該中反應的逆反應速率及表達式為v逆=kc(CO)c3(H2),k 為速率常數,在某溫度下測得實驗數據如表所示,
CO(g)+3H2(g) △H=+203kJmo1-1,該中反應的逆反應速率及表達式為v逆=kc(CO)c3(H2),k 為速率常數,在某溫度下測得實驗數據如表所示,
CO濃度(mo1L-1) | H2濃度(mo1L-1) | 逆反應速率(mo1L-1min-1) |
0.1 | c1 | 8.0 |
c2 | c1 | 16.0 |
c2 | 0.15 | 6.75 |
由上還數據可得該溫度下,c2=____________,該反應的逆反應速率常數 k=______L3mo1-3min-1)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com