
分析 (1)根據實驗操作的步驟(計算→稱量→溶解、冷卻→移液→洗滌→定容→搖勻→裝瓶貼簽)以及每步操作需要儀器確定反應所需儀器分析;
(2)根據n=cV計算溶質Na2CO3的物質的量,利用Na2CO3•10H2O的物質的量等于Na2CO3的物質的量及m=nM計算Na2CO3•10H2O的質量;
(3)根據c=$\frac{n}{V}$計算不當操作對n或V的影響,如果n偏大或V偏小,則所配制溶液濃度偏高.
解答 解:(1)因配制順序是:計算→稱量→溶解、冷卻→移液→洗滌→定容→搖勻→裝瓶貼簽,一般用天平稱量(用到藥匙)稱量,在燒杯中溶解,冷卻后轉移到100mL容量瓶中,并用玻璃棒引流,轉移完畢,用少量蒸餾水洗滌燒杯及玻璃棒2~3次并將洗滌液全部轉移到容量瓶中,再加適量蒸餾水,當加水至液面距離刻度線1~2cm時,改用膠頭滴管滴加,使溶液的凹液面的最低點與刻線相平,塞好瓶塞,反復上下顛倒搖勻.所以需要的儀器為:托盤天平、藥匙、燒杯、玻璃棒、100mL容量瓶、膠頭滴管,還缺少燒杯、100mL容量瓶、膠頭滴管.
故答案為:燒杯;100mL容量瓶;膠頭滴管;
(2)因Na2CO3的物質的量n=cV=0.1L×1.0mol•L-1=0.1mol,Na2CO3•10H2O的物質的量等于Na2CO3的物質的量,所以Na2CO3•10H2O的質量0.1mol×286g/mol=28.6g,
故答案為:28.6;
(3)①只要最后定容時使凹液面與刻度線相切即可,原來容量瓶中有少量蒸餾水,對溶液體積無影響,則對溶液濃度無影響,故答案為:c;
②燒杯和玻棒沒有洗滌2-3次,會造成溶質的損失,則導致溶液濃度偏低,故答案為:b;
③配制的溶液裝入潔凈的但有少量蒸餾水的試劑瓶中,會對所配置的溶液造成稀釋,則濃度偏低,故答案為:b;
④若定容時俯視,會導致溶液體積偏小,則所配溶液的物質的量濃度偏高,故答案為:a.
點評 本題考查了一定物質的量濃度溶液的配制過程、儀器以及誤差分析,難度不大,注意實驗的基本操作方法和注意事項.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:填空題
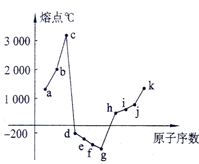 在1-18號元素中,部分連號元素單質的熔點情況如圖所示,試回答:
在1-18號元素中,部分連號元素單質的熔點情況如圖所示,試回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | C3H6不只表示一種物質 | |
| D. | 烯烴中各同系物中碳的質量分數相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
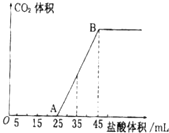 實驗室欲配制0.1mol/L NaOH溶液并進行有關性質實驗,請據此回答下列問題
實驗室欲配制0.1mol/L NaOH溶液并進行有關性質實驗,請據此回答下列問題查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 負極反應Al-3e-Al3+ | B. | 燃料氣體是氧氣 | ||
| C. | 正極反應為2CO2+O2+4e-2CO32- | D. | 該電池不能用烴類物質作燃料 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
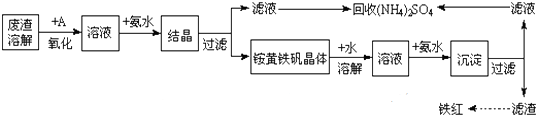
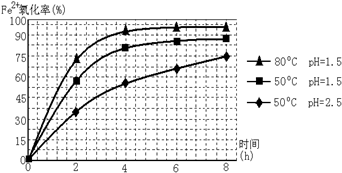
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2OH$→_{170℃}^{濃硫酸}$CH2═CH2↑+H2O | |
| B. | CH3CHBrCH3+NaOH$→_{△}^{乙醇}$CH3CH═CH2↑+NaBr+H2O | |
| C. | 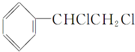 +2NaOH$→_{△}^{乙醇}$ +2NaOH$→_{△}^{乙醇}$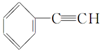 +2NaCl+2H2O +2NaCl+2H2O | |
| D. | 2CH3OH$→_{△}^{濃硫酸}$CH3-O-CH3+H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com