
 現有A、B、C、D、E、F原子序數依次增大的六種元素,它們位于元素周期表的前四周期.B元素含有3個能級,且每個能級所含的電子數相同;D的原子核外有8個運動狀態不同的電子;E元素與F元素處于同一周期相鄰的族,它們的原子序數相差3,且E元素的基態原子有4個未成對電子.請回答下列問題:
現有A、B、C、D、E、F原子序數依次增大的六種元素,它們位于元素周期表的前四周期.B元素含有3個能級,且每個能級所含的電子數相同;D的原子核外有8個運動狀態不同的電子;E元素與F元素處于同一周期相鄰的族,它們的原子序數相差3,且E元素的基態原子有4個未成對電子.請回答下列問題:分析 A、B、C、D、E、F原子序數依次增大的六種元素,它們位于元素周期表的前四周期;B元素含有3個能級,且每個能級所含的電子數相同,則B是C元素;
D的原子核外有8個運動狀態不同的電子,則D是O元素,C原子序數大于B而小于D,則C是N元素;
E元素與F元素處于同一周期相鄰的族,它們的原子序數相差3,且E元素的基態原子有4個未成對電子,E原子序數大于D,則E為Fe元素,F為Cu元素,
(1)B、C、D分別是C、N、O元素,同一周期元素,元素第一電離能隨著原子序數增大而呈增大趨勢,但第IIA族、第VA族元素第一電離能大于其相鄰元素;
(2)A.沸點:原子晶體>分子晶體;
B.同一周期元素,元素電負性隨著原子序數增大而增大;
C.等電子體結構相似但性質不同;
D.氫化物的穩定性與非金屬元素的非金屬性強弱有關,與氫鍵無關;
(3)離子晶體熔沸點與晶格能成正比,晶格能與離子半徑成反比、與電荷成正比;
(4)晶體中最近的兩個原子之間的距離為該晶體晶胞體長的$\frac{1}{4}$,該晶胞中原子個數=4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8,該晶胞體積=$\frac{\frac{12}{{N}_{A}}×8}{ρ}$cm3,該晶胞體長=$\sqrt{3}$×$\root{3}{\frac{96}{ρ{N}_{A}}}$cm.
解答 解:A、B、C、D、E、F原子序數依次增大的六種元素,它們位于元素周期表的前四周期;B元素含有3個能級,且每個能級所含的電子數相同,則B是C元素;
D的原子核外有8個運動狀態不同的電子,則D是O元素,C原子序數大于B而小于D,則C是N元素;
E元素與F元素處于同一周期相鄰的族,它們的原子序數相差3,且E元素的基態原子有4個未成對電子,E原子序數大于D,則E為Fe元素,F為Cu元素,
(1)B、C、D分別是C、N、O元素,同一周期元素,元素第一電離能隨著原子序數增大而呈增大趨勢,但第IIA族、第VA族元素第一電離能大于其相鄰元素,所以B、C、D第一電離能由低到高順序是C<O<N,
故答案為:C<O<N;
(2)A.沸點:原子晶體>分子晶體,二氧化硅是原子晶體、二氧化碳是分子晶體,所以沸點SiO2>CO2
,故A錯誤;
B.同一周期元素,元素電負性隨著原子序數增大而增大,所以電負性順序:C<N<O<F
,故B正確;
C.等電子體結構相似但性質不同,二者原子個數相等、價電子數相等,所以是等電子體,但二者不是同一物質,化學性質不同,故C錯誤;
D.氫化物的穩定性與非金屬元素的非金屬性強弱有關,與氫鍵無關,非金屬性O>S,所以穩定性:H2O>H2S
,故D錯誤;
故選ACD;
(3)Fe2+離子半徑比Fe3+離子半徑大,所帶電荷少,故FeO晶格能比Fe2O3小,FeO的熔點比Fe2O3低,
故答案為:低;Fe2+離子半徑比Fe3+離子半徑大,所帶電荷少,故FeO晶格能比Fe2O3低;
(4)該晶胞中原子個數=4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8,該晶胞體積=$\frac{\frac{12}{{N}_{A}}×8}{ρ}$cm3,該晶胞體長=$\sqrt{3}$×$\root{3}{\frac{96}{ρ{N}_{A}}}$cm,晶體中最近的兩個原子之間的距離為該晶體晶胞體長的$\frac{1}{4}$=$\frac{\sqrt{3}}{4}×\root{3}{\frac{96}{ρ{N}_{A}}}$cm,
故答案為:$\frac{\sqrt{3}}{4}×\root{3}{\frac{96}{ρ{N}_{A}}}$.
點評 本題考查物質結構和性質,涉及晶胞計算、電負性大小比較、第一電離能大小比較、等電子體等知識點,為高頻考點,注意等電子體物理性質相似但化學性質不同,難點是晶胞計算,注意該晶體中兩個距離最近原子之間距離與晶胞體長關系,為易錯點.


科目:高中化學 來源: 題型:選擇題
| A. | 63.00 | B. | 63.60 | C. | 64.00 | D. | 65.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 加熱或光照時,濃HNO3更易發生分解 | |
| B. | 加催化劑,使氮氣和氫氣在一定條件下轉化為氨氣 | |
| C. | 可用濃氨水和氫氧化鈉固體快速制取氨氣 | |
| D. | H2、I2、HI平衡混和氣加壓后顏色變深 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖所示,試管①中盛有98℃的水,試管②中充滿氣體B,將液體A滴入試管②中,充分反應后打開活塞K,發現試管①中的水立刻沸騰.則A與B可能是( )
如圖所示,試管①中盛有98℃的水,試管②中充滿氣體B,將液體A滴入試管②中,充分反應后打開活塞K,發現試管①中的水立刻沸騰.則A與B可能是( )| A. | 苯和氫氣 | B. | 稀硫酸與一氧化碳 | ||
| C. | 飽和食鹽水與氯氣 | D. | 濃溴水和乙烯 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應的焓變為負值 | |
| B. | 升高溫度,逆反應速率減小 | |
| C. | 恒溫恒容下,增大壓強,H2濃度一定減小 | |
| D. | 該反應化學方程式為CO2+H2?CO+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 碳酸二甲酯資料 | |||||
| 簡稱 | 鍵線式 | 熔點 | 沸點 | 化學性質 | 用途 |
| DMC | 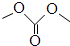 | 4℃ | 90.1℃ | 非常活潑、很易水解 毒性很低 | 有機合成中間體 |
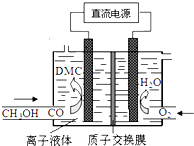 則下列說法正確的是( )
則下列說法正確的是( )| A. | 通O2區是陰極區,質子通過交換膜從陰極區移向陽極區 | |
| B. | 陽極反應:CO-2e-+2CH3OH═(CH3O)2CO+2H+ | |
| C. | 離子液體必須是水溶液,目的是傳遞電荷 | |
| D. | 電合成DMC的總反應方程式:CO+2CH3OH═(CH3O)2CO+H2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com