
【題目】H2、CO、CH4、CH3OH等都是重要的能源,也是重要為化工原料。
(1)已知25℃,1.01×105Pa時,,8.0DgCH4完全燃燒生成二氧化碳氣體和液態水放出444.8kJ熱量。寫山該反應的熱化學反應方程式:____________________。
(2)為倡導“節能減排”和“低碳經濟”,降低大氣中CO2的含量及有效地開發利用CO2,工業上可以用CO2來生產燃料甲醇。
在體積為2L的密閉容器中,充入lmolCO2和3molH2,一定條件下發生反應:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。經測得CO2和CH3OH(g)的物質的量隨時間變化如圖所示。
CH3OH(g)+H2O(g)。經測得CO2和CH3OH(g)的物質的量隨時間變化如圖所示。
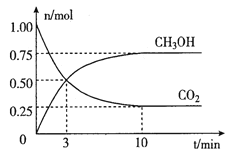
①從反或開始到平衡,CO2的平均反應速率v(CO2)=____。
②達到平衡時,H2的轉化率為__________。
③下列措施不能提高反應速率的是__________。
A.升高溫度 B.加入催化劑 C.增大壓強 D.及時分離出CH3OH
(3)工業上也用CO和H2為原料制備CH3OH,反應方程式為:CO(g)+2H2(g)![]() CH3OH(g),在一體積固定的密閉容器中投入一定量的CO和H2氣體進行上述反應。下列敘述中能說明上述反應達到平衡狀態的是______。
CH3OH(g),在一體積固定的密閉容器中投入一定量的CO和H2氣體進行上述反應。下列敘述中能說明上述反應達到平衡狀態的是______。
A.反應中CO與CH3OH的物質的量之比為1:1
B.混合氣體的壓強不隨時間的變化而變化
C.單位時間內每消耗1molCO,同時生成1mclCH3OH
D.CH3OH的質量分數在混合氣體中保持不變
E.混合氣體的密度保持不變
【答案】 CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H=-889.6kJ/mol 0.0375mol/(L·min) 75% D BD
【解析】(1)0.5mol甲烷完全燃燒放熱444.8kJ,1mol甲烷完全燃燒放熱889.6kJ,據此寫出甲烷完全燃燒的熱化學程式。
(2)利用三段式解題法進行相關計算,求出反應中變化量、平衡量;根據v=c/t計算,根據氫氣的平衡濃度判斷轉化的物質的量,進而可計算轉化率。
(3)當反應達到平衡狀態時,正、逆反應速率相等(同種物質),各物質的濃度、含量不再改變,以及由此衍生的一些物理量也不變,以此進行判斷。
(1)8.0gCH4的量為0.5mol,完全燃燒生成二氧化碳氣體和液態水放出444.8kJ熱量,1molCH4完全燃燒生成二氧化碳氣體和液態水放出889.6kJ熱量,熱化學方程式為:CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H=-889.6kJ/mol;正確答案:CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H=-889.6kJ/mol。
(2)利用三段式解題法計算:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起始量 1 3 0 0
變化量 0.75 2.25 0.75 0.75
平衡量 0.25 0.75 0.75 0.75
①反應達平衡,CO2的平均反應速率v(CO2)=0.75/2×10= 0.0375mol/(L·min);正確答案:0.0375mol/(L·min)。
②達到平衡時,H2的轉化率為2.25/3×100%=75%;正確答案:75%。
③A.升高溫度,反應速率加快,錯誤;B.加入催化劑,更大程度地加快反應速率,錯誤;C.增大壓強,縮小體積,增大物質濃度,反應速率加快,錯誤;D.及時分離出CH3OH,減小生成物濃度,反應速率減慢,正確;正確選項D。
(3)A.平衡時反應混合物各組分的物質的量不變,但各組分的物質的量不一定相等,A錯誤;B.因為該反應為氣體總量減小的反應,隨反應進行混合氣體總物質的量發生變化,混合氣體的壓強不隨時間的變化而變化,說明混合氣體總的物質的量再不變,說明反應到達平衡,B正確;C.單位時間內消耗1molCO,同時生成1molCH3OH,都表示正反應速率,反應始終按此關系進行,不能說明到達平衡, C錯誤;D.CH3OH的質量分數在混合氣體中保持不變,說明可逆反應到達最大限度,即平衡狀態, D正確;E.反應前后氣體總質量不變,容器的體積不變,混合氣體的密度始終為定值,不能判定反應達到平衡狀態,E錯誤;正確選項BD。


科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式書寫正確的是( )
A. 向氯化鋁溶液中加入過量氨水:Al3++4NH3·H2O=4AlO2-+4NH4++2H2O
B. 用硫化亞鐵與稀硫酸反應制硫化氫:S2-+2H+=H2S↑
C. 雙氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O
D. 向NH4HCO3溶液中加過量的NaOH溶液并加熱:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[化學——選修3:物質結構與性質]碳是地球上組成生命的最基本的元素之一。根據要求回答下列問題:
(1)碳原子的價電子排布式______________,核外有_________種不同運動狀態的電子。
(2)碳可以形成多種有機化合物,下圖所示是一種嘌呤和一種吡啶的結構,兩種分子中所有原子都在一個平面上。
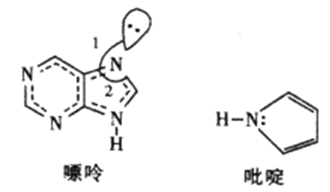
①嘌呤中所有元素的電負性由大到小的順序__________________。
②嘌呤中軌道之間的夾角∠1比∠2大,解釋原因__________________。
③吡啶結構中N原子的雜化方式__________________。
④分子中的大π鍵可用符號π![]() 表示,m代表形成大π鍵的原子數,n代表參與形成大π鍵的電子數。則吡啶結構中的大π鍵表示為__________。
表示,m代表形成大π鍵的原子數,n代表參與形成大π鍵的電子數。則吡啶結構中的大π鍵表示為__________。
(3)碳元素能形成CO、CO2、H2CO3等多種無機化合物。
①二氧化碳的晶體叫做干冰,每個二氧化碳分子周圍通常有__________個緊鄰的分子。
②在CO轉化成CO2的反應過程中,下列說法正確的是__________。
A.分子中孤電子對數不變 B.分子的極性發生變化
C.原子間成鍵方式發生改變 D.分子晶體的熔沸點升高
③H2CO3與H3PO4均有1個非羥基氧,H3PO4為中強酸,H2CO3為弱酸的原因_________。
(4)2017年,中外科學家團隊共同合成了碳的一種新型同素異形體:T-碳。T-碳的結構是將立方金剛石中的每個碳原子用一個由4個碳原子組成的正四面體結構單元取代形成碳的一種新型三維立方晶體結構,如下圖。已知T碳晶胞參數為a pm,阿伏伽德羅常數為NA,則T碳的密度的表達式為__________g/cm3。(寫出表達式即可)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SO2是主要大氣污染物之一,工業上可用如下裝置吸收轉化SO2(A、B為惰性電極)。下列說法正確的是

A. 電子流動方向為:B→b→a→A
B. a、A極上均發生氧化反應
C. 離子交換膜為陽離子交換膜
D. B極上的電極反應式為:SO2+2eˉ+2H2O=SO42-+4H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2017年我國承建全球首艘深海采礦船,具2500米深海作業能力,對未來深海礦產資源的開發具有重要戰略價值。海洋深處有豐富的錳結核礦(主要成分為MnO2,含少量Fe、Al等雜質元素),利用錳結核礦可以制備高純碳酸錳,請回答下列有關問題:
(1)寫出用MnO2和濃鹽酸制取氯氣的化學方程式________________。
(2)MnO2與過氧化氫的反應十分復雜。在酸性條件下,MnO2可以被H2O2還原成Mn2+,但H2O2又有氧化性,有研究表明,H2O2溶液的氧化性是HO2-所致。其他條件相同時,研究不同初始pH條件下H2O2溶液的漂白效果,結果如圖所示:
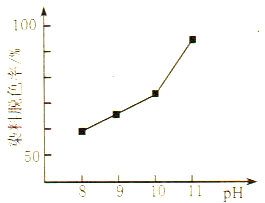
①寫出MnO2在酸性條件下與H2O2反應的離子方程式____________。
②由圖可得到的結論是_________,結合平衡移動原理簡述理由:__________。
(3)利用錳結核礦在實驗室制備高純碳酸錳的流程如下:
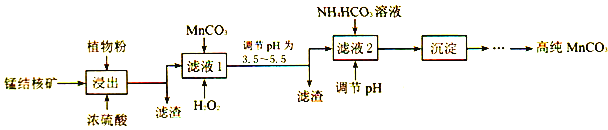
①可用SO2代替植物粉,植物粉的作用是___________。
②使用碳酸錳調pH的優勢是___________。
③加入NH4HCO3時,溫度要控制在35℃以下,其目的是___________。
(4)在廢水處理中常用H2S將Mn2+轉化為MnS除去,向含有0.020mo/LMn2+的廢水中通入一定量的H2S氣體,調節溶液的pH,當c(HS-)=1.0×10-4mol/L時,Mn2+開始沉淀,則此時溶液的pH=______。[已知:Ksp(MnS)=1.4×10-15;H2S的電離常數K1=1.3×10-7,K2=7.0×10-15]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電浮選凝聚法是工業上采用的一種污水處理方法,即保持污水的pH在5.0~6.0之間,通過電解生成Fe(OH)3膠體,Fe(OH)3膠體具有吸附作用,可吸附水中的污物而使其沉淀下來,起到凈水的作用,其原理如圖所示.下列說法正確的是( ) 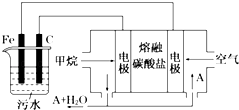
A.石墨電極上發生氧化反應
B.根據圖示,物質A為CO2
C.為增強污水的導電能力,可向污水中加入適量乙醇
D.甲烷燃料電池中CO32﹣向空氣一極移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦酸鋇(BaTiO3)在工業上有重要用途,主要用于制作電子陶瓷、PTC熱敏電阻、電容器等多種電子元件。以下是生產鈦酸鋇的一種工藝流程圖:
![]()
已知:①草酸氧化鈦鋇晶體的化學式為BaTiO(C2O4)2·4H2O;
②25℃時,BaCO3的溶度積Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合價為:__________。
(2)用鹽酸酸浸時發生反應的離子方程式為: __________。
(3)流程中通過過濾得到草酸氧化鈦鋇晶體后,為提高產品質量需對晶體洗滌。
①過濾操作中使用的玻璃儀器有_____________________。
②如何證明晶體已洗凈?_______________________。
(4)TiO2具有很好的散射性,是一種有重要用途的金屬氧化物。工業上可用TiCl4水解來制備,制備時需加入大量的水,同時加熱,其目的是:_______________。
(5)某興趣小組取19.70gBaCO3模擬上述工藝流程制備BaTiO3,得產品13.98g,BaTiO3的產率為:________。
(6)流程中用鹽酸酸浸,其實質是BaCO3溶解平衡的移動。若浸出液中c(Ba2+)=0.1mol/L,則c(CO32-)在浸出液中的最大濃度為__________ mol/L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室有下列試劑,其中必須用帶橡膠塞的試劑瓶保存的( )
①NaOH溶液 ②水玻璃 ③Na2S溶液 ④Na2CO3溶液 ⑤NH4Cl溶液 ⑥澄清石灰水 ⑦濃HNO3 ⑧濃H2SO4
A. ①⑥ B. ①②③④⑥ C. ①②③⑥⑦⑧ D. ⑤⑦⑧
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com