
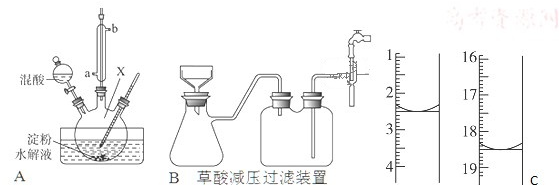
分析 (1)熟悉儀器的圖形,說出其名稱;
(2)冷凝水流向與蒸氣流向逆向時冷凝效果最佳;硝酸易揮發;
(3)草酸具有還原性,硝酸能進一步氧化C6H12O6和H2C2O4;
(4)反應后生成的產物為一氧化氮、二氧化氮,為有毒氣體,需要進行尾氣處理;
(5)依據減壓過濾的條件解答;依據減壓過濾的正確操作排序解答;
(6)高錳酸鉀為紫紅色,過程中不需要加指示劑;在酸性條件下,高錳酸根離子能和草酸發生氧化還原反應生成二價錳離子、二氧化碳和水,根據反應計算.
解答 解:(1)容器X的名稱為三頸燒瓶,故答案為:三頸燒瓶;
(2)冷凝水流向與蒸氣流向逆向時冷凝效果最佳,所以應從a口進入;硝酸易揮發,所以需要進行冷凝,故答案為:a;硝酸;
(3)混酸為65%HNO3與98%H2SO4的混合液,混合液溶于水放熱,溫度高能加快化學反應,硝酸能進一步氧化H2C2O4成二氧化碳,
故答案為:由于溫度過高、硝酸濃度過大,導致C6H12O6 和H2C2O4進一步被氧化;
(4)反應后生成的產物為一氧化氮、二氧化氮,為有毒氣體,需要進行尾氣處理,所以裝置最大的一個缺點缺少尾氣處理裝置;
故答案為:缺少尾氣處理裝置;
(5)草酸重結晶的減壓過濾裝置如圖B,通過儀器Y接在水龍頭上,起抽氣作用,使吸濾瓶、安全瓶中的壓強減小;
減壓過濾的操作為:②將濾紙放入漏斗并用水濕潤;③打開水龍頭;①將含晶體的溶液倒入漏斗;⑤拆下橡皮管;④關閉水龍頭;
故答案為:起抽氣作用,使吸濾瓶、安全瓶中的壓強減小;②③①⑤④;
(6)高錳酸鉀溶液為紫紅色,當達到滴定終點時,再滴入高錳酸鉀溶液時,淡紫色不再褪去,草酸鈉(Na2C2O4)溶于稀硫酸中,然后用酸性高錳酸鉀溶液進行滴定,離子方程式為:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,n(KMnO4)=0.016L×0.0200mol•L-1=3.2×10-3mol,根據方程式可得:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
2 5
3.2×10-3mol 8×10-3mol
樣品中二水合草酸的質量為m=8×10-3mol×126g/mol=8×126×10-3g=1.008g,
則該草酸晶體樣品中二水合草酸的質量分數為$\frac{1.008g}{1.2g}$×100%=84%,
故答案為:無色;紫紅色(或淡紫色);84%.
點評 本題考查了草酸的制取,把握實驗的原理,熟練進行氧化還原計算是解答的關鍵,注意用結晶法分離固體混合物及其抽濾的實驗操作,題目難度較大.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有①④ | B. | 只有②③④⑤ | C. | 只有①②③④ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 ,寫出該的單體的結構簡式:CH2=CH2、CH2=CH-CN、C6H5-CH=CH2
,寫出該的單體的結構簡式:CH2=CH2、CH2=CH-CN、C6H5-CH=CH2 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,物質A的化學式MgO.CaO.
,物質A的化學式MgO.CaO. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com