
【題目】已知無色溶液X可能含有H+、Na+、NH4+、Mg2+、Al3+、CO32-、NO3-、SO42-中的幾種離子,某化學興趣小組通過如下實驗確定了其成分(其中所加試劑均過量,氣體體積已轉化為標準狀況):
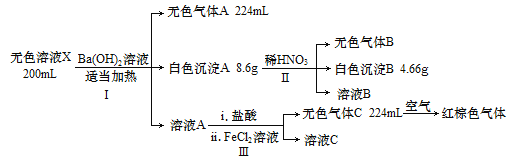
回答下列問題:
(1)實驗Ⅱ可確定無色溶液X中一定不存在的離子有________。
(2)無色氣體A的空間構型為_______;白色沉淀A的成分為_______(寫化學式)。
(3)實驗Ⅲ中的第ii步操作對應發生的反應的離子方程式為________。
(4)該無色溶液X中一定存在的陽離子及其物質的量濃度為________。
【答案】H+、Mg2+、Al3+ 三角錐形 BaCO3、BaSO4 3Fe2++4H++NO3-=3Fe3++NO↑+2H2O c(NH4+)=0.05mol/L,c(Na+)=0.4mol/L
【解析】
無色溶液X中加入Ba(OH)2溶液加熱產生無色氣體A是NH3,說明含有NH4+,根據氨氣的物質的量可計算出NH4+的物質的量;同時產生白色沉淀A,向該沉淀中加入稀硝酸產生無色氣體B,同時有白色沉淀B,說明沉淀A是BaSO4、BaCO3的混合物,二者的質量和為8.6g,沉淀B是BaSO4,氣體B是CO2,說明原溶液中含SO42-、CO32-,根據沉淀A、B的質量可計算出原溶液中含有的SO42-、CO32-的物質的量;向溶液A中加入鹽酸酸化,并加入FeCl2溶液,產生無色氣體C,該氣體與空氣變為紅棕色,則B是NO,說明III發生了氧化還原反應,A中含有NO3-,根據NO的體積,結合N元素守恒可得NO3-的物質的量,根據離子共存判斷是否含有其它離子,并進行分析解答。
根據上述分析可知:該溶液中一定含有NH4+、SO42-、CO32-、NO3-,由于CO32-與H+、Mg2+、Al3+會發生離子反應而不能大量共存,所以該溶液中一定不含有H+、Mg2+、Al3+離子;
(2)無色氣體A是NH3,該氣體分子呈三角錐形;白色沉淀A是BaSO4、BaCO3的混合物;
(3) 實驗Ⅲ中的第ii步操作是H+、NO3-與Fe2+發生氧化還原反應,根據電子守恒、電荷守恒及原子守恒。可得該反應的離子方程式為3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
(4)根據上述分析及題干已知信息,結合元素守恒可知,在原溶液中含有的離子的物質的量分別是:n(NH4+)=n(NH3)=0.224L÷22.4L/mol=0.01mol,n(SO42-)=n(BaSO4)=4.66g÷233g/mol=0.02mol,n(CO32-)=n(BaCO3)=(8.6-4.66)g÷197g/mol=0.02mol,n(NO3-)=n(NO)= 0.224L÷22.4L/mol=0.01mol。陰離子帶有的負電荷總數多于陽離子帶有的正電荷總數,根據溶液呈電中性,說明溶液中還含有陽離子Na+,其物質的量是n(Na+)=2n(SO42-)+2n(CO32-)+n(NO3-)- n(NH4+)=2×0.02mol+2×0.02mol+0.01mol-0.01mol=0.08mol,溶液的體積是200mL,則該無色溶液X中一定存在的陽離子的物質的量濃度c(NH4+)= n(NH4+)÷V=0.01mol÷0.2L=0.05mol/L;c(Na+)= n(Na+)÷V=0.08mol÷0.2L=0.4mol/L。


 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學 來源: 題型:
【題目】下列實驗操作、現象與結論對應關系正確的是
選項 | 實驗操作 | 實驗現象 | 結論 |
A | 相同溫度下,同時向 ①4 mL 0.1 molL-1 KMnO4酸性溶液和②4 mL 0.2 molL-1 KMnO4酸性溶液中,分別加入4 mL 1 molL-1 H2C2O4溶液 | ①中溶液先褪色 | 該實驗條件下,KMnO4濃度越小,反應速率越快 |
B | 向煤爐中灼熱的煤炭上灑少量水 | 產生淡藍色火焰,煤炭燃燒更旺 | 加少量水后,可使煤炭燃燒放出更多的熱量 |
C | 加熱2NO2(g) | 顏色加深 | 證明正反應是放熱反應 |
D | 分別測定室溫下等物質的量濃度的Na2SO3與Na2CO3溶液的pH | 后者較大 | 證明非金屬性 S>C |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.NaHS在水中的電離方程式為NaHS=Na++HS﹣,HS﹣![]() H++S2﹣
H++S2﹣
B.氧化還原反應中,一種元素被氧化的同時必有另一種元素被還原
C.1mol配合物Fe(CO)5(羰基鐵)中含有5mol配位鍵
D.氫氧化鐵膠體帶有正電荷,通電時向電源負極一端移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業制備合成氨原料氣過程中存在反應:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41kJ·mol-1,下列判斷正確的是
CO2(g)+H2(g) △H=-41kJ·mol-1,下列判斷正確的是
A. 該反應的逆反應是放熱反應B. 反應物總能量小于生成物總能量
C. 反應中生成22.4LH2(g),放出41kJ熱量D. 反應中消耗1mol CO(g),放出41kJ熱量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A是聚合反應生產膠黏劑基料的單體,亦可作為合成調香劑I、聚酯材料J的原料,相關合成路線如下:

已知:在質譜圖中烴A的最大質荷比為118,其苯環上的一氯代物共三種,核磁共振氫譜顯
示峰面積比為3:2:2:2:1。
根據以上信息回答下列問題:
(1)A的官能團名稱為__________________,B→C的反應條件為_____________,E→F的反應類型為_____________。
(2)I的結構簡式為____________________,若K分子中含有三個六元環狀結構,則其分子式為________________。
(3)D與新制氫氧化銅懸濁液反應的離子方程式為_______________________________。
(4)H的同分異構體W能與濃溴水反應產生白色沉淀,1 mol W參與反應最多消耗3 mol Br2,請寫出所有符合條件的W的結構簡式___________________________________。
(5)J是一種高分子化合物,則由C生成J的化學方程式為
______________________________________________________________________。
(6)![]() 已知:
已知:![]() (R為烴基)
(R為烴基)
設計以苯和乙烯為起始原料制備H的合成路線(無機試劑任選)。
[合成路線示例:]![]()
_____________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】人們對苯及芳香烴的認識有一個不斷深化的過程。
(1)由于苯的含碳量與乙炔相同,人們認為它是一種不飽和烴,寫出分子式為C6H6的一種含2個三鍵且無支鏈的不飽和鏈烴的結構簡式:______________________________。
(2)已知分子式為C6H6的結構有多種,其中的兩種結構簡式為
(I)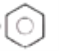 (II)
(II)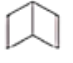
①這兩種結構的區別表現在:
定性方面(即化學性質方面):Ⅱ能______________(填標號,多選不給分),而Ⅰ不能。
a.被酸性高錳酸鉀溶液氧化 b.與溴水發生加成反應
c.與溴發生取代反應 d.與氫氣發生加成反應
定量方面(即消耗反應物的量的方面):1mol C6H6與H2加成時:Ⅰ需______________mol,而Ⅱ需________________mol。
②今發現C6H6還可能有另一種立體結構(如圖所示)。該結構的一氯代物有____________種。二氯代物有_____________種。
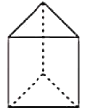
(3)萘也是一種芳香烴,它的分了式是C10H8,請你判斷,它的結構簡式可能是下列中的____(填標號)。
a. ![]() b.
b. 
c. ![]() d.
d. 
(4)根據第(3)小題中你判斷得到的萘結構簡式,它不能解釋萘的下列________事實(填標號)。
a.萘不能使溴水褪色 b.萘能與H2發生加成反應
c.萘分子中所有原子在同一平面上 d.一溴代萘(C10H7Br)只有兩種
(5)現代化學認為萘分子中碳碳之間的鍵是一種____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧化劑和還原劑在生產生活中廣泛使用。
(1)H3PO2均可將溶液中的 Ag+還原為 Ag,從而可用于化學鍍銀。
①H3PO2中P元素的化合價為___。
②利用H3PO2進行化學鍍銀反應中,氧化劑與還原劑物質的量之比為4:1,則氧化產物為___。
(2)氯酸是一種強酸,氯酸的濃度超過40%就會迅速分解,反應的化學方程式為8HClO3=3O2↑+2Cl2↑+4HClO4+2H2O。根據題意完成下列小題:
①該反應的還原產物是___(填化學式);
②所得混合氣體的平均相對分子質量為___。
(3)已知測定錳的一種方法是:錳離子轉化為高錳酸根離子,反應體系中有H+、Mn2+、H2O、IO3-、MnO4-、IO4-。
①有關反應的離子方程式為___。
②在錳離子轉化為高錳酸根離子的反應中,如果把反應后的溶液稀釋到1L,測得溶液的c(H+)=0.03mol/L,則在反應中轉移電子的物質的量為___mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知反應H2(g)+ ![]() O2(g)=H2O(g)的能量變化如圖所示,a、b、c表示能量變化,為正值,單位為kJ,下列說法正確的是 ( )
O2(g)=H2O(g)的能量變化如圖所示,a、b、c表示能量變化,為正值,單位為kJ,下列說法正確的是 ( )
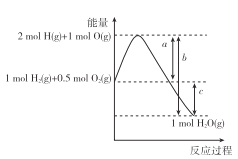
A. H2(g)+ ![]() O2(g)=H2O(g) △H=c kJ·mol-1
O2(g)=H2O(g) △H=c kJ·mol-1
B. 2H2O(g)=2H2 (g)+O2 (g) △H=—2(a-b) kJ·mol-1
C. 1 mol氫氣與0.5 mol氧氣總能量為akJ
D. 2 mol氫氣與1 mol氧氣完全反應生成2 mol液態水放出的熱量小于2(b-a)kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業合成氨反應:N2+3H2![]() 2NH3是一個放熱的可逆反應,反應條件是高溫、高壓,并且需要合適的催化劑。已知形成1 mol H-H鍵、1 mol N-H鍵、1 mol N≡N鍵放出能量分別為436 kJ、391 kJ、946 kJ。則:
2NH3是一個放熱的可逆反應,反應條件是高溫、高壓,并且需要合適的催化劑。已知形成1 mol H-H鍵、1 mol N-H鍵、1 mol N≡N鍵放出能量分別為436 kJ、391 kJ、946 kJ。則:
(1)若1 mol N2完全反應生成NH3可________(填“吸收”或“放出”)熱量________kJ。
(2)如果將1 mol N2和3 mol H2混合,使其充分反應,放出的熱量總小于上述數值,其原因是________________________。
(3)實驗室模擬工業合成氨時,在容積為2 L的密閉容器內,反應經過10 min后,生成10 mol NH3,則用N2表示的化學反應速率為________mol·L-1·min-1。
(4)一定條件下,當合成氨的反應達到化學平衡時,下列說法正確的是________。
a.正反應速率和逆反應速率相等
b.正反應速率最大,逆反應速率為0
c.N2的轉化率達到最大值
d.N2和H2的濃度相等
e.N2、H2和NH3的體積分數相等
f.反應達到最大限度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com