
【題目】如圖所示是一個有機物的核磁共振氫譜圖,請你觀察圖譜,分析其可能是下列物質中的 ( )
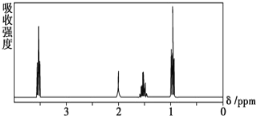
A.CH3CH2CH2CH3B.(CH3)3CCH3
C.CH3CH2CH2OHD.CH3CH2COOH
 小學期末沖刺100分系列答案
小學期末沖刺100分系列答案 期末復習檢測系列答案
期末復習檢測系列答案 超能學典單元期中期末專題沖刺100分系列答案
超能學典單元期中期末專題沖刺100分系列答案 黃岡360度定制密卷系列答案
黃岡360度定制密卷系列答案科目:高中化學 來源: 題型:
【題目】[化學——選修5:有機化學基礎]端炔烴在催化劑存在下可發生偶聯反應,稱為Glaser反應。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
該反應在研究新型發光材料、超分子化學等方面具有重要價值。下面是利用Glaser反應制備化合物E的一種合成路線:

回答下列問題:
(1)B的結構簡式為______,D 的化學名稱為______。
(2)①和③的反應類型分別為______、______。
(3)E的結構簡式為______。用1 mol E合成1,4二苯基丁烷,理論上需要消耗氫氣_______mol。
(4)化合物(![]() )也可發生Glaser偶聯反應生成聚合物,該聚合反應的化學方程式為_____________________________________。
)也可發生Glaser偶聯反應生成聚合物,該聚合反應的化學方程式為_____________________________________。
(5)芳香化合物F是C的同分異構體,其分子中只有兩種不同化學環境的氫,數目比為3:1,寫出其中3種的結構簡式_______________________________。
(6)寫出用2苯基乙醇為原料(其他無機試劑任選)制備化合物D的合成路線___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于熱化學反應的描述中正確的是
A.有氧氣參與的反應都是放熱反應
B.熱化學方程式既表示能量的變化,又表示物質的變化
C.若2CO2(g)![]() 2CO(g)+O2(g)△H=+566kJ·mol-1,則CO的燃燒熱△H=-566 kJ·mol-1
2CO(g)+O2(g)△H=+566kJ·mol-1,則CO的燃燒熱△H=-566 kJ·mol-1
D.放熱反應理論上都可以設計為原電池,將化學能轉化為電能
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度、壓強下,向密閉容器中投入一定量N2和H2,發生反應:N2+3H2![]() 2NH3 △H<0。
2NH3 △H<0。
(1)反應開始階段,v(正)_______(填“>”“<”或“=”)v(逆),隨后v(正)________逐漸(填“增大”或“減小”,下同),v(逆)逐漸_______,反應達到平衡時,v(正)_______(填“>”“<”或“=”)v(逆)。
(2)達到平衡后,若正反應速率用v(N2)表示,逆反應速率用v’(H2)表示,則v(N2)=____v’(H2)。
(3)下列措施中能加快反應速率并提高氫氣的轉化率的是_______(填字母)。
A 其他條件不變時,壓縮容器體積 B 其他條件不變時,升高反應體系溫度
C 使用合適的催化劑 D 保持容器體積不變,充入一定量的氮氣
(4)實際生產中往往需要將溫度控制在一個合適的范圍,分析溫度不宜過高也不宜過低的原因是_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上通常利用SiO2 和碳反應來制取硅,寫出反應的化學方程式___________________。
工業上還可以利用鎂制取硅,反應為2Mg+SiO2 = 2MgO+Si,同時會發生副反應:2Mg + Si = Mg2Si。如圖是進行Mg與SiO2反應的實驗裝置,試回答下列問題:

(1)由于O2和H2O(g)的存在對該實驗有較大影響,實驗中應通入氣體X作為保護氣,試管中的固體藥品可選用________(填序號)。
a.石灰石 b.鋅粒 c.純堿
(2)實驗開始時,必須先通一段時間X氣體,再加熱反應物,其理由是 ___________________________;當反應引發后,移走酒精燈,反應能繼續進行,其原因是______________________。
(3)反應結束后,待冷卻至常溫時,往反應后的混合物中加入稀鹽酸,可觀察到閃亮的火星,產生此現象的原因是副產物Mg2Si遇鹽酸迅速反應生成SiH4(硅烷)氣體,然后SiH4自燃.用化學方程式表示這兩個反應①________________________②___________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】標況下,a克氣體X與b克氣體Y的分子數相同,下列說法錯誤的是( )
A.X和Y的式量之比是a:b
B.氣體X和氣體Y的密度比為b:a
C.1g氣體X和1g氣體Y的分子數之比是a:b
D.1mol氣體X和1mol氣體Y的質量比是a:b
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學上以12C作為確定原子量的標準。若把12C的原子量定為24,并規定把24g12C所含碳原子數定為阿伏伽德羅常數,用NA表示,則下列推論中正確的是( )
A.12g碳單質完全燃燒需要體積約為11.2L(標準狀況)的氧氣
B.44gCO2和28gCO含有相同數目的分子
C.NA個氧分子和1mol氫分子的質量之比為8:1
D.氧氣的摩爾質量為64g/mol,所以32g氧氣所含分子數目為3.01×1023個
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向含有0.01 mol Cu,a mol Cu2O、b mol CuO的混合物中滴加6 mol·L-1的稀硝酸溶液至10ml時,固體恰好完全溶解,得到標準狀況下224mL氣體(純凈物)。下列說法正確的是
A.反應過程中轉移0.01 mol電子B.a:b=1:1
C.被還原的硝酸為0.06 molD.將少量鐵粉投入該稀硝酸中能生成Fe(NO3)2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校化學實驗興趣小組為了探究在實驗室制備Cl2的過程中有水蒸氣和HCl揮發出來,同時證明氯氣的某些性質,甲同學設計了如圖所示的實驗裝置(支撐用的鐵架臺省略),按要求回答問題(Cl2易溶于CCl4)。
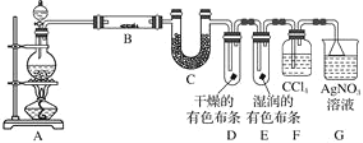
(1)若用含有7.3 g HCl的濃鹽酸與足量的MnO2反應制Cl2,制得的Cl2質量總是小于3.55 g的原因是________________________________。
(2)①裝置B中盛放的試劑名稱為________________,作用是________________________________,現象是_____________________________。
②裝置D和E中出現的不同現象說明的問題是___________________。
③裝置F的作用是__________________________________________。
(3)乙同學認為甲同學的實驗有缺陷,不能確保最終通入AgNO3溶液中的氣體只有一種。為了確保實驗結論的可靠性,證明最終通入AgNO3溶液的氣體只有一種,乙同學提出在某兩個裝置之間再加一個裝置。你認為該裝置應加在________與________之間(填裝置字母序號),裝置中應放入________(填寫試劑或用品名稱)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com