
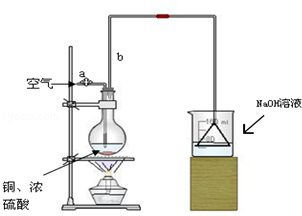
 某學校課外活動小組針對教材中銅與濃硫酸反應,提出了“能夠與銅反應的硫酸的最低濃度是多少?”的探究課題,并設計了如下方案進行實驗:實驗試劑:18mol/L硫酸20mL,純銅粉足量,足量2mol/LNaOH溶液.
某學校課外活動小組針對教材中銅與濃硫酸反應,提出了“能夠與銅反應的硫酸的最低濃度是多少?”的探究課題,并設計了如下方案進行實驗:實驗試劑:18mol/L硫酸20mL,純銅粉足量,足量2mol/LNaOH溶液.分析 (1)有連接裝置的實驗需要在開始時檢查裝置的氣密性;
(2)SO2是污染性氣體不能排放到空氣中,且是酸性氧化物,能和堿液反應生成鹽;
尾氣處理中有緩沖作用的裝置能防倒吸;
(3)燒瓶中是Cu和濃硫酸加熱反應生成CuSO4、SO2和H2O;裝置中長導氣管兼起導氣冷凝的作用,使水蒸氣冷凝回流;
(4)加入H2O2把Na2SO3氧化為Na2SO4,加入BaCl2溶液反應生成BaSO4沉淀,通過過濾、洗滌、干燥得到沉淀稱量計算S元素物質的量,依據S元素守恒結合化學方程式計算需要反應的硫酸最低濃度;
(5)不加入H2O2,沉淀為BaSO3、BaSO4沉淀,不能計算硫元素物質的量,對實驗產生誤差.
解答 解:(1)該裝置有連接裝置,實驗前應該檢驗裝置氣密性,否則二氧化硫易逸出或得不到二氧化硫,故答案為:檢驗裝置氣密性;
(2)SO2是污染性氣體不能排放到空氣中,且是酸性氧化物,能和堿液反應生成鹽,所以NaOH的作用是吸收未反應的SO2;
尾氣處理中有緩沖作用的裝置能防倒吸,導致的漏斗低口大,有緩沖作用,能防倒吸,
故答案為:SO2;防倒吸;
(3)燒瓶中是Cu和濃硫酸加熱反應生成CuSO4、SO2和H2O,反應方程式為Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;裝置中長導氣管兼起導氣冷凝的作用,使水蒸氣冷凝回流,
故答案為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;長導管;
(4)加入過氧化氫把亞硫酸鈉氧化為硫酸鈉,加入氯化鋇溶液反應生成硫酸鋇沉淀,通過過濾、洗滌、干燥得到沉淀,稱量固體的質量為13.98g為硫酸鋇沉淀,物質的量=$\frac{13.98g}{233g/mol}$=0.06mol,依據硫元素守恒,被氧化的硫酸為0.06mol,依據化學方程式可知,Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,反應的硫酸物質的量為0.12mol,剩余硫酸物質的量=18mol/L×0.020L-0.12mol=0.24mol,剩余需要的最低濃度=$\frac{0.24mol}{0.02L}$=12mol/L,
故答案為:過濾;洗滌;干燥;12mol/L;
(5)不加入過氧化氫,沉淀為亞硫酸鋇和硫酸鋇沉淀,不能計算硫元素物質的量,所以需要加入過氧化氫,氧化亞硫酸鈉為硫酸鈉后,再進行沉淀稱量計算,
故答案為:需要;在燒杯中生成的Na2SO3可能被部分氧化為Na2SO4,如果不加入雙氧水而直接測定沉淀質量則無法確定S元素的物質的量,從而使實驗結果錯誤.
點評 本題以濃硫酸和Cu的反應為載體考查性質實驗方案設計,為高頻考點,明確實驗原理、實驗基本操作原理、物質性質是解本題關鍵,注意該實驗中的長導管的作用,為易錯點.


 同步練習河南大學出版社系列答案
同步練習河南大學出版社系列答案 同步練習西南師范大學出版社系列答案
同步練習西南師范大學出版社系列答案科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗器材(省略夾持裝置) | 相應實驗 |
| A | 燒杯、玻璃棒、石棉網、酒精燈 | 濃縮結晶硫酸銅溶液制膽礬 |
| B | 燒杯、玻璃棒、膠頭滴管、漏斗、濾紙 | 用鹽酸除去硫酸鋇中的少量碳酸鋇 |
| C | 燒杯、玻璃棒、膠頭滴管、容量瓶 | 用固體氯化鈉配制100 mL 0.5 mol•L-1的溶液 |
| D | 燒杯、玻璃棒、膠頭滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
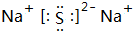 ;W2X2的結構式H-O-O-H.
;W2X2的結構式H-O-O-H.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用灼燒聞氣味法鑒別棉布和絲綢 | |
| B. | 用焰色反應鑒別NaCl和Na2SO4 | |
| C. | 用丁達爾效應鑒別Fe(OH)3膠體和FeCl3溶液 | |
| D. | 用加熱的方法鑒別Na2CO3和NaHCO3固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 12% | B. | 32% | C. | 44% | D. | 88% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | c(NO)/mol•L-1 | c(H2)/mol•L-1 | 速率/mol•L-1•min-1 |
| Ⅰ | 0.0060 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.0060 | 0.0020 | 3.6×10-4 |
| Ⅲ | 0.0010 | 0.0060 | 3.0×10-5 |
| Ⅳ | 0.0020 | 0.0060 | 1.2×10-4 |
| A. | 整個反應速度由第①步反應決定 | |
| B. | 正反應的活化能一定是①<② | |
| C. | 該反應速率表達式:v=5000c2(NO)•c(H2) | |
| D. | 該反應的熱化學方程式為2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-664kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④ | B. | ①⑥ | C. | ②④ | D. | 只有① |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com