
| A. | 加入催化劑,平衡常數不變 | |
| B. | 減小容器體積,正、逆反應速率均減小 | |
| C. | 保持容積不變,增大CO2的量,NH3的轉化率減小 | |
| D. | 降低溫度,平衡向逆反應方向移動 |
分析 A.催化劑改變化學反應速率,不改變化學平衡;
B.減小容器體積相當于增大壓強,反應速率增大;
C.增加二氧化碳,平衡正向移動;
D.反應是放熱反應,降低溫度,平衡正向進行.
解答 解:A.催化劑改變化學反應速率,不改變化學平衡,加入催化劑,平衡常數不變,故A正確;
B.減小容器體積相當于增大壓強,反應速率增大,正逆反應速率都增大,故B錯誤;
C.增加二氧化碳,平衡正向移動,NH3的轉化率增大,故C錯誤;
D.依據化學平衡移動原理分析,反應是放熱反應,降低溫度,平衡正向進行,故D錯誤;
故選A.
點評 本題考查了化學平衡影響因素分析判斷,為高頻考點,側重于學生的分析能力的考查,題目涉及平衡移動原理的理解應用,注意反應特征的方向,題目難度不大.


 小學生10分鐘口算測試100分系列答案
小學生10分鐘口算測試100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1 mol H2O中所含的粒子數目一定是NA | |
| B. | 1 molNH4+所含的質子數是10NA | |
| C. | 51 g NH3所含原子數為3NA | |
| D. | 氧氣的相對分子質量與2NA個氧原子質量(以g為單位)在數值上相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
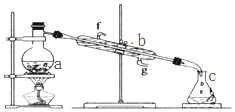 掌握儀器名稱、組裝及使用方法是中學化學實驗的基礎,圖為蒸餾實驗裝置.
掌握儀器名稱、組裝及使用方法是中學化學實驗的基礎,圖為蒸餾實驗裝置.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 除去NH4Cl溶液中的FeCl3,可向溶液中加入氨水調節pH | |
| B. | 除去金屬離子Cu2+、Hg2+,可向溶液中加入H2S、Na2S等沉淀劑 | |
| C. | 除去某溶液中的SO42-可向溶液中加入鎂鹽 | |
| D. | 除去ZnCl2溶液中的Fe3+可向溶液中加入ZnO |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,2.24 L CHCl3的原子總數為0.1 NA | |
| B. | 1 mol-OH中電子數為10 NA | |
| C. | 4.2 g C3H6中含有的碳碳雙鍵數一定為0.1 NA | |
| D. | 常溫常壓下,28 g丙烯和丁烯的混合氣體中含有的碳原子數為2 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蒸發操作時,應使混合物中的水分完全蒸干后,才能停止加熱 | |
| B. | 蒸餾操作時,應使溫度計水銀球靠近蒸餾燒瓶的支管口處 | |
| C. | 分液操作時,分液漏斗中下層液體從下口放出,上層液體從上口倒出 | |
| D. | 萃取操作時,應選擇有機萃取劑,且萃取劑不溶于水 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com