
| A. | NaCl | B. | Cl2 | C. | Na和Mg | D. | NaOH和H2 |
分析 A、海水蒸發即可得到氯化鈉;
B、可從海水中獲得氯化鈉,配制成飽和食鹽水,然后電解,即得氯氣;
C、海水中得到鈉、鎂,需要首先從海水中獲得氯化鈉和氯化鎂,然后再去電解熔融狀態的氯化鈉和氯化鎂即得鈉和鎂;
D、可從海水中獲得氯化鈉,配制成飽和食鹽水,然后電解,即得燒堿、氫氣和氯氣.
解答 解:A、海水蒸發水后可以得到氯化鈉,不需要化學變化,屬于物理變化,故A正確;
B、電解飽和食鹽水能得到氯氣,屬于化學變化,故B錯誤;
C、鈉與鎂在海水中均是以離子形式存在,需要電解熔融狀態的氯化鈉和氯化鎂即得鈉和鎂,屬于化學變化,故C錯誤;
D、電解飽和食鹽水可以得到NaOH和氫氣,屬于化學變化,故D錯誤;
故選A.
點評 本題考查了海水的成分,以及提煉溴、碘、鈉、鎂、氫氣等物質的原理,涉及的知識較多,掌握制備原理是解題的關鍵.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題

| 催化劑組分質量分數(%) | CuO | 0 | 25 | 50 | 75 | 100 |
| ZnO | 100 | 75 | 50 | 25 | 0 | |
| 到達平衡所需時間(h) | 2.5 | 7.4 | 8.1 | 12 | 無催化活性 | |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 飽和氯水中:Cl-、NO3-、Na+、CO32- | |
| B. | c(H+)=1.0×10-13mol•L的溶液中:MnO4-、K+、SO42-、AlO2- | |
| C. | c(AlO2-)=1.0mol•L的溶液中:SO42-、K+、Cl-、HCO3- | |
| D. | pH=7的溶液中:NO2-、I-、Na+、Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

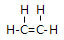 ;由元素④和元素②形成的化合物的電子式為
;由元素④和元素②形成的化合物的電子式為 ;元素⑦的原子結構示意圖為
;元素⑦的原子結構示意圖為 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將濃硫酸和濃硝酸分別長期露置在空氣中,濃度均會降低 | |
| B. | 在常溫下,濃硫酸和濃硝酸均能與銅劇烈反應 | |
| C. | 稀硫酸和稀硝酸分別與金屬反應時,S和N元素的化合價都會發生變化 | |
| D. | 因為濃硫酸和濃硝酸都能與鐵反應,所以常溫下二者都不能用鐵制容器盛裝 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用氫氧化鈉溶液除去二氧化碳氣體中的二氧化硫 | |
| B. | 可用干燥的淀粉碘化鉀試紙檢驗氯氣 | |
| C. | 某溶液焰色反應的火焰呈黃色,說明該溶液中肯定含鈉離子不確定是否含鉀離子 | |
| D. | 用分液漏斗分離水與乙醇的混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (若有配位鍵,用箭號表示)
(若有配位鍵,用箭號表示)
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | pH=5.6的由CH3COOH與CH3COONa組成的混合溶液中:c(Na+)>c(CH3C00-) | |
| B. | 將PH=a的醋酸稀釋為pH=a+1的過程中,C(OH-)不斷增大 | |
| C. | 等體積pH=a的鹽酸與pH=b的氨水溶液恰好中和時,a+b=14 | |
| D. | 濃度均為0.1 mol•L-1的CH3COOH溶液和氨水等體積混合后:c(CH3COO-)+c(H+)=c(NH4+)+c(OH-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com