
【題目】分別將鎂條和鋁條平行插人盛有一定濃度稀鹽酸、NaOH的燒杯中,用導線和電流計連接成兩個原電池,裝置如圖所示。原電池工作時,下列敘述正確的是
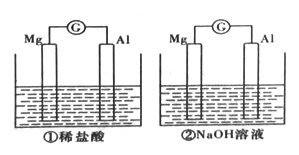
A. 因為Mg比Al活潑,所以兩個原電池中負極都是Mg
B. 兩個原電池中,電子都是由鎂條通過導線流向鋁條
C. 兩個原電池中,反應放出的能量都完全轉化成電能
D. 兩個原電池中,正極都有氫氣生成
【答案】D
【解析】第一個裝置中電解質為稀鹽酸,Mg、Al均能與鹽酸反應,Mg比Al活潑,Mg作負極,Al作正極;第二個裝置中電解質為NaOH,Mg不與NaOH溶液反應而Al能與NaOH溶液發(fā)生自發(fā)的氧化還原反應,故負極為Al,正極為Mg。
A、根據(jù)上分析可知第一個裝置中Mg為負極,第二個裝置中Al為負極,A錯誤。
B、第一個裝置中電子由Mg條通過導線流向Al條,第二個裝置中電子由Al條通過導線流向Mg條,B錯誤。C、原電池中,化學能不可能全部轉化為電能,C錯誤。D、兩個裝置中正極都是氫離子得電子生成氫氣,在正極會有氫氣產(chǎn)生,D正確。正確答案為D


科目:高中化學 來源: 題型:
【題目】有機物A的結構如圖所示,下列說法正確的是
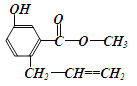
A. 一定條件下,1 mol A能與3 mol NaOH反應
B. 一定條件下,1 mol A能和5 mol氫氣發(fā)生加成反應
C. 一定條件下和濃溴水反應時,1 mol A能消耗3 mol Br2
D. A能與碳酸氫鈉溶液反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現(xiàn)有一瓶A和B的混合物,已知它們的性質如下表。
物質 | 熔點/℃ | 沸點/℃ | 密度/g·cm—3 | 溶解性 |
A | —11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
B | 17.9 | 290 | 1.26 |
據(jù)此分析,將A和B相互分離的常用方法是
A. 蒸餾 B. 蒸發(fā) C. 分液 D. 過濾
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】自然界中的許多植物中含有醛,其中有些具有特殊香味,可作為植物香料使用,例如桂皮含肉桂醛(![]() ),杏仁含苯甲醛(
),杏仁含苯甲醛(![]() )。下列說法錯誤的是
)。下列說法錯誤的是
A.肉桂醛能發(fā)生加成反應、取代反應和加聚反應
B.可用新制氫氧化銅懸濁液檢驗肉桂醛分子中的含氧官能團
C.肉桂醛和苯甲醛互為同系物
D.苯甲醛分子中所有原子可能位于同一平面內(nèi)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物H是合成抗心律失常藥物泰達隆的一種中間體,可通過以下方法合成:

(1)D中的含氧官能團名稱為 (寫兩種)。
(2)F→G的反應類型為 。
(3)寫出同時滿足下列條件的C的一種同分異構體的結構簡式 。
①能發(fā)生銀鏡反應;
②能發(fā)生水解反應,其水解產(chǎn)物之一能與FeCl3溶液發(fā)生顯色反應;
③分子中只有4種不同化學環(huán)境的氫。
(4)E經(jīng)還原得到F,E的分子是為C14H17O3N,寫出E的結構簡式 。
(5)已知:①苯胺(![]() )易被氧化
)易被氧化

請以甲苯和(CH3CO)2O為原料制備 ,寫出制備的合成路線流程圖。
,寫出制備的合成路線流程圖。
(無機試劑任用,合成路線流程圖示例見本題題干)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋁熱反應是鋁的一個重要性質。


(1)按如圖裝置進行實驗,可觀察到反應劇烈,火星四射,漏斗下方有紅熱熔融物“鐵塊”流出。
該反應的化學方程式為_____,其能量變化為如圖中的______(填“A”或“B”)所示。

(2)某校化學興趣小組同學,為了測定鋁熱反應后得到“鐵塊”混合物中鋁的含量。取“鐵塊”樣品研碎稱得質量為x g,加入如圖裝置,再滴入足量NaOH溶液充分反應,測量生成氣體體積為a ml(標況)。
①儀器A的名稱為_______。
②寫出樣品中Al與NaOH反應的化學方程式_______。
③該小組同學改進實驗,用恒壓漏斗(如圖)代替儀器A,其優(yōu)點有________(寫2點)。
④該樣品中鋁的含量為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應:2NO2![]() 2NO+O2 在密閉容器中反應,達到平衡狀態(tài)的標志是:( )
2NO+O2 在密閉容器中反應,達到平衡狀態(tài)的標志是:( )
①單位時間內(nèi)生成n molO2的同時生成2n molNO2
②單位時間內(nèi)生成n molO2的同時,生成2n mol NO
③用NO2、NO、O2的物質的量濃度變化表示的反應速率的比為2 : 2 : 1的狀態(tài)
④混合氣體的顏色不再改變的狀態(tài) ⑤混合氣體的密度不再改變的狀態(tài)
⑥ 混合氣體的平均相對分子質量不再改變的狀態(tài)
A. ①④⑥ B. ②③⑤ C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酸為弱酸,其鈉鹽(亞硝酸鈉NaNO2)外觀酷似食鹽且有咸味,過量使用會使人中毒。其銀鹽不溶于水。某化學興趣小組對亞硝酸鈉的制備進行了探究。
(1)請設計一種簡單方法鑒別NaCl和NaNO2 :___________。
(2)利用如圖完成一氧化氮與過氧化鈉反應制備業(yè)硝酸鈉。查閱資料:2NO + Na2O2 =2NaNO2, 2NO2+ Na2O2=2NaNO3, NO 能被酸性高錳酸鉀氧化為NO3-。回答下列問題:

① 檢查裝置氣密性后,應進行的操作是_________。
② 裝置B 中Cu 參與反應的離子方程式為______,裝置C 的作用是______。
③ 裝置E發(fā)生反應的離子方程式為________。
④ 同學們經(jīng)過討論認為上述裝置仍然存在缺陷,D中生成的產(chǎn)物不純,D管中可能含有的雜質為________(填化學式),你認為應該進行的改進是__________。
(3)測定制取樣品中NaNO2的純度。
步驟:a.在5個有編號的帶刻度的試管中分別加入不同體積、相同濃度的NaNO2溶液,各加入1mL的M溶液(M遇NaNO2呈紫紅色,NaNO2濃度越大顏色越深),再加蒸餾水至總體積均為10mL,并振蕩,制成標準色階;
試管編號 | ① | ② | ③ | ④ | ⑤ |
NaNO2含量(mg/L) | 0 | 20 | 40 | 60 | 80 |
b.稱量0.10g制得的樣品,溶于水配成500mL溶液。取5mL待測液,加入1mLM,再加入蒸餾水至l0mL,并振蕩,與標準色階比較。
比較結果:待測液與④標準色階相同,則制取樣品中NaNO2的純度是________。
查閱資料可知:維生素C可有效降低NaNO2的含量。請完成下列實驗驗證方案:取5 mL 待測液,加入______,振蕩,再加入1mL M溶液,_____,再振蕩,與④ 標準色階對比。實驗現(xiàn)象為紫紅色比④ 標準色階淺,則證明維生素C可以有效降低NaNO2的含量。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com