
【題目】2017年5月5日,中國國產大飛機C919首飛成功。為了減輕機身重量,飛機某些部件使用了鎂合金。
(1)基態鎂原子核外電子的軌道表達式為___________,其核外有_________種能量不同的電子。
(2)①第二電離能:Na_______Mg(填“>”“<”或“=”),其原因為______________。
②熱穩定性:CaCO3>MgCO3,其原因為___________________________。
(3)鎂不僅在工業生產中用途廣泛,也是動植物生命活動中必不可少的微量元素,下圖為葉綠素的結構示意圖。

①圖中與Mg形成配位鍵的N原子的標號為________(填寫“Ⅰ”“Ⅱ”“Ⅲ”“Ⅳ”)。
②葉綠素中,碳原子的雜化形式為________。
(4)碳化鎂是一種在化工行業用途廣泛的金屬碳化物,某種碳化鎂的晶體結構如圖1所示,圖2為其俯視圖。

①晶體中Mg的配位數為________。
②已知阿伏伽德羅常數的值為NA,據圖1中計算該碳化鎂的密度為________g·cm-3.
【答案】 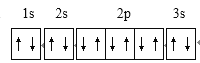 4 > Na失去1個電子后,2p能級處于全充滿的穩定狀態,故第二電離能Na>Mg r(Ca2+)>r(Mg2+),CaO晶格能小于MgO晶格能,故MgCO3更易分解為MgO,穩定性CaCO3>MgCO3 Ⅲ、Ⅳ sp2、sp3 6
4 > Na失去1個電子后,2p能級處于全充滿的穩定狀態,故第二電離能Na>Mg r(Ca2+)>r(Mg2+),CaO晶格能小于MgO晶格能,故MgCO3更易分解為MgO,穩定性CaCO3>MgCO3 Ⅲ、Ⅳ sp2、sp3 6 ![]()
【解析】(1)鎂的質子為12,基態鎂原子核外電子的軌道表達式為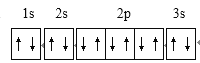 ,其核外有1s、2s、2p、3s,4種能量不同的電子。(2)①第二電離能:Na>Mg,其原因為Na失去1個電子后,2p能級處于全充滿的穩定狀態,故第二電離能Na>Mg。②熱穩定性:CaCO3>MgCO3,其原因為r(Ca2+)>r(Mg2+),CaO晶格能小于MgO晶格能,故MgCO3更易分解為MgO,穩定性CaCO3>MgCO3 。(3)①圖中Ⅲ、Ⅳ 提供孤電子對,與Mg形成配位鍵的N原子的標號為Ⅲ、Ⅳ 。②葉綠素中,形成4個單鍵的碳是sp3雜化,形成2個單鍵、1個雙鍵的碳是sp2雜化,碳原子的雜化形式為sp2、sp3。(4)某種碳化鎂的晶體結構①晶體中Mg的配位數為6。②已知阿伏伽德羅常數的值為NA,據圖1,晶胞中鎂離子為12×1/6+2×1/2=3,C為6,碳化鎂化學式為MgC2,該碳化鎂的密度為=
,其核外有1s、2s、2p、3s,4種能量不同的電子。(2)①第二電離能:Na>Mg,其原因為Na失去1個電子后,2p能級處于全充滿的穩定狀態,故第二電離能Na>Mg。②熱穩定性:CaCO3>MgCO3,其原因為r(Ca2+)>r(Mg2+),CaO晶格能小于MgO晶格能,故MgCO3更易分解為MgO,穩定性CaCO3>MgCO3 。(3)①圖中Ⅲ、Ⅳ 提供孤電子對,與Mg形成配位鍵的N原子的標號為Ⅲ、Ⅳ 。②葉綠素中,形成4個單鍵的碳是sp3雜化,形成2個單鍵、1個雙鍵的碳是sp2雜化,碳原子的雜化形式為sp2、sp3。(4)某種碳化鎂的晶體結構①晶體中Mg的配位數為6。②已知阿伏伽德羅常數的值為NA,據圖1,晶胞中鎂離子為12×1/6+2×1/2=3,C為6,碳化鎂化學式為MgC2,該碳化鎂的密度為=![]() =
=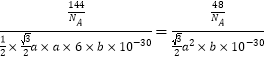 g·cm-3.
g·cm-3.


科目:高中化學 來源: 題型:
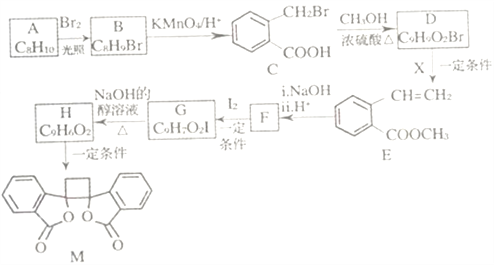
【題目】我國北方生長的一種植物中含有抗菌作用的化合物M,已知M的合成路線如下圖所示:
已知:i.RCH2Br![]() R-HC=CH-R';
R-HC=CH-R';
ii.R-HC=CH-R'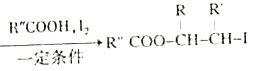 ;
;
iii.R-HC=CH-R'![]()
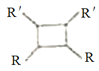 (以上R、R'、R"代表氫、烴基等)。
(以上R、R'、R"代表氫、烴基等)。
(1)A的化學名稱為_______,D中所含官能團的名稱是______。由H生成M的反應類型為_____。
(2)運用先進的分析儀器,極大改善了有機物結構鑒定。
①可利用_______(填“質譜”“紅外光譜”或”核磁共振氫譜)測得C的相對分子質量。
②測定B的結構:B的核磁共振氫譜顯示為_____組峰。
(3)1molM與足量NaOH溶液反應,消耗_____molNaOH。
(4)X的結構式為_____,F的結構簡式為______ 。
(5)由C生成H的化學方程式為__________。
(6)符合下列條件的B的同分異構體共______種(不考慮立體異構)。
①芳香族化合物 ②與E具有相同官能團 ③能發生銀鏡反應 ④酸性條件下水解產物遇氯化鐵溶液顯紫色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】前四周期元素A、B、C、D、E、F,原子序數依次增大,其中A和B同周期,固態的AB2能升華;C和E原子都有一個未成對電子,C+比E-少一個電子層,E原子得到一個電子后3p軌道全充滿;D最高價氧化物中D的質量分數為40%,且核內質子數等于中子數;F為紅色單質,有F+和F2+兩種離子。回答下列問題:
(1)元素電負性:D____E (填>、<或=);
(2)B、C單質熔點B_____C(填>、<或=);
(3)AE4中A原子雜化軌道方式為:________雜化;其固態晶體類型為_____________;
(4)氫化物的沸點:B比D高的原因______________;
(5)F的核外電子排布式為____________________________;向F的硫酸鹽中逐滴加入氨水先產生沉淀,后沉淀溶解為深藍色溶液,加入乙醇會析出深藍色晶體,該晶體的化學式為_______,其中關于該晶體下列說法中正確的是_____________________。
A.加入乙醇的目的是降低溶劑的極性,促使晶體析出
B.F與NH3之間的化學鍵為離子鍵
C.該配合物晶體中,N是配位原子,NH3為三角錐型
D.配離子內N原子排列成為平面正方形,則其中F離子是sp3雜化
E.向該晶體的水溶液中加入濃BaCl2溶液有白色沉淀生成
(6)元素X的某價態陰離子Xn-中所有電子正好充滿K和L電子層,CnX晶體的最小結構單元為立方體,結構如圖所示。該晶體中每個Xn-被________個等距離的C+離子包圍。已知該晶體的密度為ρg.cm-3,阿伏加德羅常數為NA,CnX的摩爾質量為M g/mol,C+和Xn-間的最短距離是_____________nm。(列出計算式即可)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A是合成離分子樹脂G和合成酚醛樹酯的原料之一。相關的合成路線如下圖所示:

已知:Ⅰ. (R1、R2、R3代表烴基)
(R1、R2、R3代表烴基)
Ⅱ.![]()
請回答下列問題:
(1) 經質譜測定,有機物A的相對分子質量為164,燃燒8.2g有機物A,生成標準狀況下11.2LCO2和5.4gH2O。則A的分子式是________,A中所含官能團的名稱是________。
(2)B的結構簡式________。
(3)C的名稱是________,請寫出在一定條件下C與足量新制氫氧化銅懸濁液反應的化學方程式________。
(4)D-F的反應類型是________,寫出由C和苯酚合成酚醛樹脂的化學方程式是___________。
(5)有機物![]() 有多種同分異構體,寫出同時滿足下列條件的一種同分異構體的結構簡式_________。
有多種同分異構體,寫出同時滿足下列條件的一種同分異構體的結構簡式_________。
Ⅰ.分子中除苯環外,無其它環狀結構;
Ⅱ.核磁共振氯譜顯示為5組峰;
Ⅲ.能發生水解反應,不能與Na反應
Ⅳ.能發生銀鏡反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高鐵電池是一種新型可充電電池,與普通高能電池相比,該電池長時間保持穩定的放電電壓。高鐵電池的總反應為:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列敘述不正確的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列敘述不正確的是
A. 放電時負極反應為:Zn-2e-+2OH-=Zn(OH)2
B. 充電時陽極反應為:Fe(OH)3-3e-+5OH-=![]() +4H2O
+4H2O
C. 放電時每轉移3 mol電子,正極有1 mol K2FeO4被氧化
D. 放電時正極附近溶液的堿性增強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】沙丁胺醇(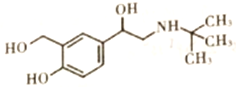 )是一種新型藥物,常用于緩解哮喘等肺部疾病,其一種合成路線如下。
)是一種新型藥物,常用于緩解哮喘等肺部疾病,其一種合成路線如下。
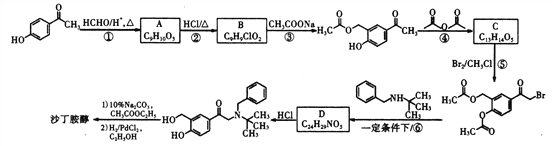
(1)沙丁胺醇的分子式為_____________,C中官能團的名稱為_____________。
(2)①的反應類型為____________,⑥的反應類型為____________。
(3)B的結構簡式為_____________。
(4)A在酸性條件下發生縮聚反應的化學方程式為__________________________。
(5)符合下列條件的B的同分異構體有________種(不考慮立體異構),其中任意一種的結構簡式為_____________。
a.苯環上有兩個取代基; b.能與NaHC03反應生成CO2。
(6)寫出以苯酚、甲醛和乙酸酐(![]() )為原料制備高分子
)為原料制備高分子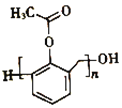 的合成路線:____________________________________________________(無機試劑任選)
的合成路線:____________________________________________________(無機試劑任選)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新型高效的甲烷燃料電池采用鉑為電極材料,兩電極上分別通入CH4和O2 ,電解質為KOH溶液。某研究小組將兩個甲烷燃料電池串聯后作為電源,進行飽和氯化鈉溶液電解實驗,如圖所示。

回答下列問題:
(1)甲烷燃料電池正極、負極的電極反應分別為________________ 、_______________ ;
(2)閉合K開關后,a、b電極上均有氣體產生.其中a電極上得到的是_________(填化學式),電解氯化鈉溶液的總反應方程式為___________________;
(3)若每個電池甲烷通入量為1 L(標準狀況),且反應完全,則理論上最多能產生的氯氣體積為____________L(標準狀況);
(4)若飽和氯化鈉溶液體積為100mL,電解一段時間后,常溫下測得溶液pH為13,若要使溶液恢復到電解前的狀態,可向溶液中加(或通)入__________(填寫物質的化學式)_________g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將等物質的量的金屬Na、Mg、Al分別與100 mL 2 mol·L-1的鹽酸反應,實驗測得生成氣體的體積V(已折合為標準狀況)與時間t的關系如圖所示,則下列說法錯誤的是

A. x=2.24 B. 鋁的物質的量為0.2 mol
C. 反應時,Na、Mg、Al均過量 D. 曲線C為Al與鹽酸反應的圖像
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組將SO2通入Na2S和Na2SO3的混合溶液中制備硫代硫酸鈉(Na2S2O3)。其裝置如下圖所示(省略夾持裝置),下列說法錯誤的是
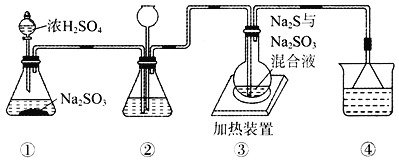
A. 裝置②的作用之一是觀察SO2的生成速率,其中的液體可以是飽和NaHSO3溶液
B. 為提高產品純度,使燒瓶中Na2S和Na2SO3恰好完全反應,則![]()
C. 裝置④的作用是吸收尾氣,同時防止倒吸
D. 裝置①也可用于高錳酸鉀與濃鹽酸反應制備氯氣
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com