

(2)天然的和絕大部分人工制備的晶體都存在各種缺陷,例如在某種NiO晶體中就存在如圖所示的缺陷:一個Ni2+空缺,另兩個被兩個Ni3+所取代,但晶體仍呈現電中性,只是化合物中Ni和O的比值發生了變化。某氧化鎳樣品組成為Ni0.97O,試計算該晶體中Ni3+與Ni2+的離子數之比。

解析:(1)密度=![]() ,選取體積有不同方法,可選取晶體中最小的重復結構單位(即晶胞)為研究對象,也可選取晶體中1 cm3空間為研究對象,求出對應體積中NiO的物質的量、質量,從而求出密度。主要解題步驟如下:
,選取體積有不同方法,可選取晶體中最小的重復結構單位(即晶胞)為研究對象,也可選取晶體中1 cm3空間為研究對象,求出對應體積中NiO的物質的量、質量,從而求出密度。主要解題步驟如下:
1 cm3該晶體中陰、陽離子總數=![]() 。
。
1 cm3中Ni2+—O2-離子對數=![]() 。
。
密度= 。
。
(2)解法一:電荷守恒法:
設1 mol Ni0.97O中含Ni3+x mol,Ni2+(0.97-x)mol根據電中性:
3x mol+2×(0.97-x)mol=2×1 mol
x=0.06,Ni2+為(0.97-x)mol=0.91 mol
離子數之比為Ni3+:Ni2+=0.06∶0.91=6∶91。
解法二:差量比例法:
將化學式放大100倍為Ni97O100。
根據題意:每3個Fe2+相當于2個Fe3+所帶正電荷,
即:去掉 增加Ni3+ 空缺
3 2 1
9 ← 6 ← 3
則每97個Ni中含有Ni3+6個,Ni2+91個。
則![]() 。
。
解法三:列方程組法:
設有a個Ni3+,b個Ni2+,c個O。
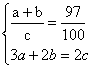
解得:a∶b=6∶91
解法四:把晶體看作Ni2O3和NiO兩種成分組成。設Ni2O3 x mol,NiO y mol,化合物Ni0.97O共1 mol

解得![]() ,則
,則![]() 。
。


 勵耘書業暑假銜接寧波出版社系列答案
勵耘書業暑假銜接寧波出版社系列答案科目:高中化學 來源: 題型:
(2)天然和絕大部分人工制備的晶體都存在各種缺陷,例如在某種NiO晶體中就存在如圖所示的缺陷:一個Ni2+空缺,另兩個被兩個Ni3+所取代,但晶體仍呈現電中性,只是化合物中Ni和O的比值發生了變化。某氧化鎳樣品組成為Ni0.97O,試計算該晶體中Ni3+與Ni2+的離子數之比。

圖3-26
查看答案和解析>>
科目:高中化學 來源: 題型:
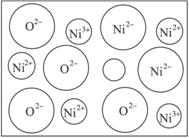
圖3-40
(2)天然和絕大部分人工制備的晶體都存在各種缺陷,例如在某種NiO晶體中就存在如圖340所示的缺陷:一個Ni2+空缺,另兩個Ni2+被兩個Ni3+所取代。其結果晶體仍呈電中性,但化合物Ni和O的比值卻發生了變化。某氧化鎳樣品組成為Ni0.97O,試計算晶體中Ni3+與Ni2+的離子數之比。
查看答案和解析>>
科目:高中化學 來源: 題型:
 (1)中學教材上圖示了NaCl晶體結構,它向三維空間延伸得到完美晶體。NiO(氧化鎳)晶體結構與NaCl相同,Ni2+與最鄰近的O2—的核間距離為a×10-8cm,計算NiO晶體的密度。(已知NiO的摩爾質量為:74.7g·mol-1)
(1)中學教材上圖示了NaCl晶體結構,它向三維空間延伸得到完美晶體。NiO(氧化鎳)晶體結構與NaCl相同,Ni2+與最鄰近的O2—的核間距離為a×10-8cm,計算NiO晶體的密度。(已知NiO的摩爾質量為:74.7g·mol-1)
(2)天然的和大部分人工晶體都存在各種缺陷,例如在某種NiO晶體中就存在如右圖所示的缺陷;一個Ni2+空缺,另有兩個Ni2+被兩個Ni3+所代替。其結果晶體仍呈電中性。但化合物中Ni和O的比值卻發生了變化。某氧化鎳樣品組成為Ni0.97O,試計算該晶體中Ni3+與Ni2+的離子數之比。
查看答案和解析>>
科目:高中化學 來源: 題型:
(1)中學教材上圖示了NaCl晶體結構,它向三維空間延伸得到完美晶體。 NiO(氧化鎳〕晶體的結構與NaQ相同,Ni2+與最鄰近O2-的核間距離為a10-8cm,計算NiO晶體的密度(已知NiO的摩爾質量為74.7g.mol-1).
(2)天然的和絕大部分人工制備的晶體都存在各種缺陷,例如在某種NiO晶體中就存在如右圖所示的缺陷:一個Ni2+空缺,另有兩個Ni2+被兩個Ni3+所取代。其結果晶體仍呈電中性,但化合物中Ni和O的比值卻發生了變化。某氧化鎳樣品組成為Nio970,試計算該晶體中Ni3+與Ni2+的離子數之比。
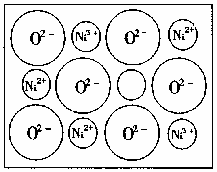
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com