
高鐵酸鉀(K2FeO4)是一種集氧化、吸附、絮凝于一體的新型多功能水處理劑。其生產工藝流程如下:
請同答下列問題:
(l)寫出向KOH溶液中通入足量Cl2發生反應的離子方程式_______ 。
(2)在溶液I中加入KOH固體的目的是______(填編號)。
| A.為下一步反應提供堿性的環境 |
| B.使KClO3轉化為KClO |
| C.與溶液I中過量的Cl2繼續反應,生成更多的KClO |
| D.KOH固體溶解時會放出較多的熱量,有利于提高反應速率 |

(1)2OH-+Cl2=ClO-+Cl-+H2O (2) AC (3) 2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O 0.45
(4) 4FeO42- +10H2O 4Fe(OH)3 (膠體) +3O2↑+8 OH- (5) Fe+8OH—6e-= FeO42- -+4H2O
4Fe(OH)3 (膠體) +3O2↑+8 OH- (5) Fe+8OH—6e-= FeO42- -+4H2O
(6)Zn+2OH—2e-=Zn(OH)2或Zn+2OH=Zn(OH)2+2e-。
解析試題分析:(l) KOH溶液與足量Cl2發生反應的離子方程式為2OH-+Cl2=ClO-+Cl-+H2O。(2)在溶液I中加入KOH固體的目的是為下一步反應提供堿性的環境;與溶液I中過量的Cl2繼續反應,生成更多的KClO。故選項為A. C.(3) 反應③中發生的離子反應方程式為2Fe3++3ClO-+10OH-=2FeO42-+ Cl-+5H2O .在方程式中每產生2mol的FeO42-轉移電子6mol.消耗氧化劑3mol.現在n(K2FeO4)= 59.4g÷198g/mol=0.3mol所以消耗氧化劑的物質的量為3÷2×0.3mol=0.45mol.(4) 高鐵酸鉀(K2FeO4)水解的離子方程式為4FeO42- +10H2O  4Fe(OH)3 (膠體) +3O2↑+8 OH-(5) 電解法是制備K2FeO4較好的方法,Fe作陽極,電極反應為Fe+8OH—6e-= FeO42- +4H2O,石墨作陰極,電極反應為:O2+ 2H2O+4e-=4OH—.(6)高鐵電池放電時電池的負極反應式為Zn+2OH—2e-=Zn(OH)2。
4Fe(OH)3 (膠體) +3O2↑+8 OH-(5) 電解法是制備K2FeO4較好的方法,Fe作陽極,電極反應為Fe+8OH—6e-= FeO42- +4H2O,石墨作陰極,電極反應為:O2+ 2H2O+4e-=4OH—.(6)高鐵電池放電時電池的負極反應式為Zn+2OH—2e-=Zn(OH)2。
考點:考查新型多功能水處理劑高鐵酸鉀(K2FeO4)的制法、原理、電子轉移及高鐵電池等反應原理的知識。


 走進文言文系列答案
走進文言文系列答案科目:高中化學 來源: 題型:填空題
高鐵酸鉀(K2FeO4)具有很強的氧化性,在生產、生活中有廣泛應用。
(1)K2FeO4常用做高效水處理劑,其兩種作用分別是_____。
[已知:FeO42-+3e-+4H2O Fe(OH)3+5OH-]
Fe(OH)3+5OH-]
(2)制備K2FeO4可以采用濕式氧化法,流程如下圖: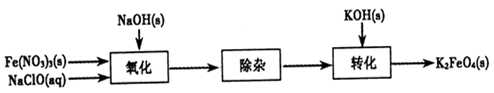
①完成氧化工序的離子方程式: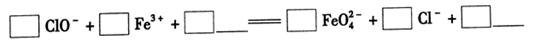
②除雜工序目的是除去Na2FeO4溶液中的雜質,除去的雜質主要有_____(寫化學式)。
③轉化工序控制在某溫度下進行,則該溫度下溶解度:Na2FeO4_____K2FeO4 (填“>”、“<”或“=”)。
(3)實驗室模擬工業電解法制取K2FeO4,裝置如右圖。
①此裝置中電源的負極是____(填“a”或“b”)。
②陽極的電極反應式為______。
(4)已知K2FeO4稀溶液中存在如下平衡:4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2。實驗測得K2FeO4溶液濃度與溫度和pH的關系分別如下圖所示:
4Fe(OH)3+8OH-+3O2。實驗測得K2FeO4溶液濃度與溫度和pH的關系分別如下圖所示:
①由圖I可得出的結論:該反應的△H___0(填“>”、“<”或“=”)。
②圖Ⅱ中pH1___pH3(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一百多種化學元素中,非金屬占了23種。80%的非金屬元素在社會中占重要位置。如C、N、O、Si、Cl等。
(1)氯元素原子最外電子層上有 種能量不同的電子,該元素的簡單陰離子核外電子排布式是 。
(2)由氮元素與硅元素組成的物質,可用于制造發動機的耐熱部件,因為它屬于 晶體,請寫出該化合物的化學式 。
(3)下列事實能說明氯與氧兩元素非金屬性相對強弱的有 。(選填編號)
a.Cl原子最外層電子數比氧多
b.酸性:HCl>H2O
c.ClO2中氯元素為+4價,氧元素為?2價
d.沸點:H2O>HCl
與Cl2相比較,ClO2處理水時被還原成Cl-,不生成有機氯代物等有害物質。工業上可用亞氯酸鈉和稀鹽酸為原料制備ClO2,反應如下:NaClO2 +HCl ClO2↑+___________________(沒有配平)
ClO2↑+___________________(沒有配平)
(4)上述方程式中,缺項物質是___________,配平方程式,并在下面補全反應物系數。____NaClO2 +____HCl
(5)該反應中氧化劑和還原劑的物質的量之比是 。生成0.2 mol ClO2轉移電子的物質的量為_______ mol。
(6)ClO2對污水中Fe2+、Mn2+、S2-和CN-等有明顯的去除效果。某污水中含CN-a mg/L,現用ClO2將CN-氧化,只生成兩種無毒氣體。處理100m3這種污水,至少需要ClO2 _______ mol 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整個過程中含碘物質的物質的量與所加入KBrO3的物質的量的關系如圖所示。
請回答下列問題:
(1)b點時,KI反應完全,則消耗的氧化劑與還原劑物質的量之比為 。
(2)已知b→c過程中,僅有一種元素發生化合價變化,寫出并配平該反應的離子方程式 ________________________________________。
(3)n(KBrO3) = 4時,對應含碘物質的化學式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
許多物質的氧化能力受溶液酸堿性的影響。高錳酸鉀在不同的條件下發生的還原反應如下:
MnO4—+ 5e + 8H+ → Mn2+ + 4H2O
MnO4— + 3e + 2H2O → MnO2 + 4OH—
MnO4— + e → MnO42—(溶液呈綠色)
MnO2的還原反應可表示如下:MnO2+4H+ + 2e → Mn2++2H2O
(1)MnO2與稀鹽酸不能制取氯氣,其原因是 。
(2)將SO2通入KMnO4溶液中,發生還原反應的過程為______→_______
(用化學式或離子符號表示)。
(3)將PbO2投入到酸性MnSO4溶液中攪拌,溶液變為紫紅色。下列敘述正確的是________(選填編號)。
a.氧化性:PbO2>KMnO4 b.還原性:PbO2> KMnO4
c.該反應可以用鹽酸酸化
(4)將高錳酸鉀溶液逐滴加入到硫化鉀溶液中可發生如下反應,其中K2SO4和S的物質的量之比為3:2。完成并配平該反應的化學方程式。
___KMnO4+___K2S+___ _____ → ___K2MnO4 +___K2SO4 +__S↓+___ ___
反應若生成5.44 g單質硫,反應過程中轉移電子的物質的量為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Fe2+和I-是兩種常見的還原性離子。
(1)向FeSO4溶液中滴加氯水,溶液由淺綠色變成黃色,反應的離子方程式為________________________;向KI溶液中滴加氯水,溶液由無色變成黃色,反應的離子方程式為______________________。
(2)請以FeSO4溶液、KI溶液、氯水、2% KSCN為試劑證明I-的還原性強于Fe2+。設計實驗方案,補充完成實驗步驟、預期現象和結論。
| 實驗步驟 | 預期現象與結論 |
| 步驟1:取2mLFeSO4溶液和2mLKI溶液混合于試管中,再滴加1~2滴氯水。 | 現象:溶液變成黃色。 結論: 。 |
| 步驟2:__________________________ __________________________________ | 現象: ; 結論: |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
實驗室可以用KMnO4固體和濃鹽酸反應制取氯氣,反應方程式如下:
2KMnO4+16HCl(濃)=2KCl+2MnCl2+5Cl2↑+8H2O。
①請用“雙線橋”標出電子轉移的方向和數目;(2分)
②該反應中被氧化和未被氧化的HCl的物質的量之比是 _______。(1分)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2KMnO4+16HCl=2MnCl2+5Cl2↑+8H2O+2KCl,在這個反應中,氧化劑是 ,氧化產物是 ,用雙線橋標出電子的轉移方向和數目 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
實驗室也可用反應2KMnO4+16HCl(濃)=2KCl+2MnCl2+5Cl2↑+8H2O來快速制取氯氣。
(1)請標出電子的轉移方向和數目
2KMnO4+16HCl(濃)=2KCl+2MnCl2+5Cl2↑+8H2O
(2)若產生標準狀況下Cl2 11.2L,則反應過程中轉移的電子數為________ ,被氧化的還原劑
的物質的量為___________。
(3)需消耗36.5%的濃鹽酸多少質量?
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com