
| 物質 | Al | Al2O3 | Fe | Fe2O3 |
| 熔點/℃ | 660 | 2054 | 1535 | 1462 |
| 沸點/℃ | 2467 | 2980 | 2750 | - |
分析 (1)鋁的熔點比鐵低,生成鐵和液態鋁一起滴落至盛有沙子的容器中形成合金;
(2)根據鋁與NaOH溶液反應的性質設計實驗方案;
(3)A.濃硫酸易使鐵、鋁鈍化,不能使合金溶解;
B.活潑金屬與稀硫酸反應;
C.稀硝酸與金屬反應生成污染性氣體;
D.鐵不與NaOH溶液反應.
解答 解:(1)鋁的熔點比鐵低,生成鐵和液態鋁一起滴落至盛有沙子的容器中形成合金,所以鋁熱反應所得到的熔融物應是鐵鋁合金,故答案為:合理;
(2)鋁與NaOH溶液反應生成氣體,反應的化學方程式為2Al+2OH-+H2O=2AlO2-+3H2↑,所以可用NaOH溶液檢驗所得的塊狀熔融物中含有金屬鋁,
故答案為:NaOH溶液;2Al+2OH-+H2O=2AlO2-+3H2↑;
(3)A.濃硫酸易使鐵、鋁鈍化,不能使合金溶解,故A錯誤;
B.活潑金屬與稀硫酸反應,熔融物可溶解于稀硫酸中,故B正確;
C.稀硝酸與金屬反應生成污染性氣體,不是最佳選擇,故C錯誤;
D.鐵不與NaOH溶液反應,不能將熔融物全部溶解,故D錯誤.
故答案為:B.
點評 本題考查鋁熱反應,題目難度不大,本題中注意(1),為易錯點,注意分析表中數據.


科目:高中化學 來源: 題型:選擇題
| A. | 皮膚上沾有苯酚可以用酒精清洗 | |
| B. | 502膠把手指粘到一起可以用丙酮溶解502膠 | |
| C. | 有機物都是能燃燒的 | |
| D. | 氟氯代烷可用作制冷劑、滅火劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaOH、BaCl2、Na2CO3、HCl | B. | BaCl2、HCl、Na2CO3、NaOH | ||
| C. | BaCl2、Na2CO3、HCl、NaOH | D. | Na2CO3、NaOH、BaCl2、HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.5mol CO+2mol H2O(g)+1mol CO2+1mol H2 | |
| B. | 1mol CO+1mol H2O(g)+1mol CO2+1mol H2 | |
| C. | 0.5mol CO+1.5mol H2O(g)+0.4mol CO2+0.4molH2 | |
| D. | 0.5mol CO+1.5mol H2O(g)+0.5molCO2+0.5mol H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
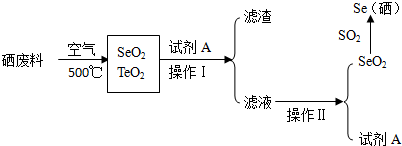
 | 沸點/℃ | 溶解性 |
| SeO2 | 684 | 易溶于水和乙醇 |
| TeO2 | 1260 | 微溶于水,不溶于乙醇 |
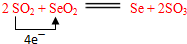 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | BaCl2、HCl | B. | Ba(NO3)2、HNO3 | C. | Ba(NO3)2、HCl | D. | BaCl2、H2SO4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com