
【題目】高錳酸鉀是常用的氧化劑。工業上以軟錳礦(主要成分是MnO2)為原料制備高錳酸鉀晶體。中間產物為錳酸鉀。下圖是實驗室模擬制備KMnO4晶體的操作流程:
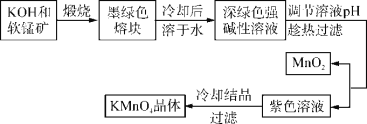
已知:錳酸鉀(K2MnO4)是墨綠色晶體,其水溶液呈深綠色,這是錳酸根離子(MnO![]() )在水溶液中的特征顏色,在強堿性溶液中能穩定存在;在酸性、中性和弱堿性環境下,MnO
)在水溶液中的特征顏色,在強堿性溶液中能穩定存在;在酸性、中性和弱堿性環境下,MnO![]() 會發生自身氧化還原反應,生成MnO
會發生自身氧化還原反應,生成MnO![]() 和MnO2。
和MnO2。
回答下列問題:
(1)KOH的電子式為____________。
(2)調節溶液pH過程中,所得氧化產物與還原產物的物質的量之比為____________。
(3)趁熱過濾的目的是_____________________________________________。
(4)已知20 ℃時K2SO4、KCl、CH3COOK的溶解度分別為11.1 g、34 g、217 g,則從理論上分析,選用下列酸中________(填標號),得到的高錳酸鉀晶體純度更高。
A.稀硫酸 B.濃鹽酸 C.醋酸 D.稀鹽酸
(5)產品中KMnO4的定量
①配制濃度為0.1250 mg· mL-1的KMnO4標準溶液100 mL。
②將上述溶液稀釋為濃度分別為2.5、5.0、7.5、10.0、12.5、15.0(單位:mg·L-1)的溶液,分別測定不同濃度溶液對光的吸收程度,并將測定結果繪制成曲線如下。

③稱取KMnO4樣品(不含K2MnO4)0.1250 g按步驟①配得產品溶液1000 mL,取10 mL稀釋至100 mL,然后按步驟②的方法進行測定,兩次測定所得的吸光度分別為0.149、0.151,則樣品中KMnO4的質量分數為________。
(6)酸性KMnO4溶液與FeSO4溶液反應的離子方程式為____________________。
【答案】 ![]() 2∶1 防止析出高錳酸鉀,降低產率 C 90.0% MnO
2∶1 防止析出高錳酸鉀,降低產率 C 90.0% MnO![]() +5Fe2++8H+===Mn2++5Fe3++4H2O
+5Fe2++8H+===Mn2++5Fe3++4H2O
【解析】軟錳礦的主要成分是MnO2,由工藝轉化關系可知,MnO2和KOH在空氣中熔融煅燒生成錳酸鉀(K2MnO4),調節錳酸鉀(K2MnO4)強堿溶液的pH,制備KMnO4,通過過濾分離出MnO2,對KMnO4溶液冷卻結晶過濾得到KMnO4晶體。
(1)本題考查電子式的書寫和儀器的選擇,KOH屬于離子化合物,其電子式為![]() ,
,
故答案為:![]() ;
;
(2)考查氧化還原反應中得失電子數目守恒,根據信息,錳酸鉀在酸性、中性、弱堿性環境中發生歧化反應,MnO2是錳酸鉀中Mn由+6價→+4價,化合價降低得到,因此MnO2是還原產物,KMnO4是氧化產物,n(KMnO4)×1=n(MnO2)×2,得出n(KMnO4):n(MnO2)=2:1,
故答案為:2∶1;
(3)考查物質的分離,高錳酸鉀溶于水,MnO2不溶于水,因此趁熱過濾目的是防止析出高錳酸鉀,降低產率;
故答案為:防止析出高錳酸鉀,降低產率;
(4)考查物質的分離和提純,高錳酸鉀與濃鹽酸反應,因此選項B錯誤;然后根據三種物質的溶解度大小,溶解度越大,得到高錳酸鉀純度越高,
故選項c正確;
(5)③考查化學計算,吸光度的平均值為(0.149+0.151)/2=0.150,此時對應的KMnO4的濃度為11.25mg·L-1,則1000mL的溶液中KMnO4的濃度為11.25×![]() mg·L-1=112.5mg·L-1,因此高錳酸鉀的質量分數為
mg·L-1=112.5mg·L-1,因此高錳酸鉀的質量分數為![]() 100%=90.0%;
100%=90.0%;
故答案為:90.0%;
(6)本題考查氧化還原反應方程式的書寫,利用高錳酸鉀的氧化性,把Fe2+氧化成Fe3+,本身被還原成Mn2+,然后根據化合價的升降法進行配平,即離子反應方程式為MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案為:MnO![]() +5Fe2++8H+===Mn2++5Fe3++4H2O。
+5Fe2++8H+===Mn2++5Fe3++4H2O。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】X、Y、Z、W、J是元素周期表前四周期中的五種常見元素![]() 其相關信息如下表:
其相關信息如下表:
元素 | 相關信息 |
X | X的基態原子核外3個能級上有電子,且每個能級上的電子數相等 |
Y | M層上有2對成對電子 |
Z | Z和Y同周期,Z的電負性大于Y |
W | W的一種核素的質量數為63,中子數為34 |
J | J的氣態氫化物與J的最高價氧化物對應的水化物可反應生成一種鹽 |
![]() 元素X的一種同位素可測定文物年代,這種同位素的符號是 ______ ;
元素X的一種同位素可測定文物年代,這種同位素的符號是 ______ ;
![]() 元素Y位于元素周期表第 ______ 周期第 ______ 族;
元素Y位于元素周期表第 ______ 周期第 ______ 族;
![]() 元素Z的原子最外層共有 ______ 種不同運動狀態的電子;
元素Z的原子最外層共有 ______ 種不同運動狀態的電子;
![]() 的基態原子核外價電子排布圖是 ______ ;
的基態原子核外價電子排布圖是 ______ ;
![]() 的氣態氫化物與J的最高價氧化物對應的水化物可反應生成一種鹽的化學式為______________ 。
的氣態氫化物與J的最高價氧化物對應的水化物可反應生成一種鹽的化學式為______________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈣是人體必需的常量元素,成年人每天需要800mg的鈣,下列補鈣的途徑正確的是
A. 經常吃水果、蔬菜B. 經常飲用鈣離子含量高的硬水
C. 經常飲用牛奶、豆奶D. 大量補充維生素C
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D四物質有如下轉化關系(反應條件和部分產物已略去):A![]() B
B![]() C
C![]() D,回答下列問題:
D,回答下列問題:
(1)若A為氣態氫化物和D能通過化合反應生成一種鹽,則
①簡述檢驗該鹽中陽離子的方法:_____________________________________;
②寫出實驗室制取A的化學方程式:______________________________________;
③寫出由A生成B的化學方程式:______________________________________;
④某同學用干燥的圓底燒瓶收集一瓶A氣體,用滴入酚酞的水做噴泉實驗,能觀察到美麗的紅色噴泉。用方程式解釋噴泉呈紅色的原因:____________________。
(2)若A與B反應能生成一種淡黃色固體單質,寫出該反應的化學方程式: ________________________________________________________________。
(3)若A是金屬單質,C是一種淡黃色固體,寫出C生成D的離子方程式:______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質中:①氯水;②濃硫酸;③溴蒸氣;④燒堿;⑤氧氣;⑥酸性KMnO4溶液,其中在一定條件下可以與甲烷發生化學反應的是 ( )
A. ①②③⑤ B. ④⑤⑥ C. ③⑤ D. ②③④⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式正確的是
A. 氯氣通入冷的氫氧化鈉溶液中:Cl2 + 2OH = Cl + ClO + H2O
B. Fe與少量稀硝酸的反應:Fe + 4H+ + NO3 = Fe3+ + NO↑+ 2H2O
C. 碳酸鋇溶于醋酸:BaCO3 + 2H+ = Ba2+ + H2O + CO2↑
D. 用石墨電極電解MgCl2 溶液:2Cl + 2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數的值,下列敘述正確的是
A. 18 g D2O所含的電子數為10NA
B. 1 mol H2O2中含有極性鍵的數目為3NA
C. 標準狀況下,22.4 L四氯化碳所含分子數為NA
D. 32g O2和O3的混合物中含有的氧原子數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硼鎂泥是一種工業廢料,主要成份是MgO(占40%,質量分數),還有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等雜質,以此為原料制取的硫酸鎂,可用于印染、造紙、醫藥等工業。從硼鎂泥中提取MgSO47H2O的工藝流程如下:
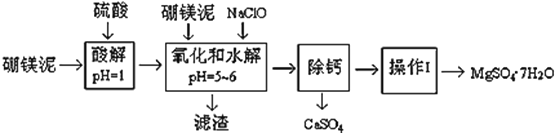
(1)實驗中需要1 mol/L的硫酸800 mL,若用 98% 的濃硫酸(ρ= 1.84 g/mL)來配制,量取濃硫酸需要使用量筒的規格為__________(填寫選項字母)
A.10 mL B.20 mL C.50 mL D.100 mL
(2)加入的NaClO可與Mn2+ 反應:Mn2+ + ClO + H2O = MnO2↓+ 2H+ + Cl ,在該步驟中還有一種離子也會被NaClO氧化,該反應的離子方程式為___________________。
(3)濾渣的主要成分除含有Fe(OH)3、Al(OH)3外,還含有__________,___________。
(4)在“除鈣”前,需檢驗濾液中Fe3+ 是否被除盡,簡述檢驗方法___________________。(寫出操作、現象和結論)
(5)已知MgSO4、CaSO4 的溶解度(單位為 g/100 g 水)如下表:
溫度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除鈣”是將MgSO4和CaSO4混合溶液中的CaSO4除去,根據上表數據,簡要說明操作步驟______。“操作Ⅰ”是將濾液繼續蒸發濃縮,冷卻結晶,______,便得到了MgSO47H2O
(6)實驗中提供的硼鎂泥共100 g,得到 MgSO47H2O為172.2 g ,則MgSO47H2O 的產率為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋁是重要的金屬材料,鋁土礦(主要成分是Al2O3和少量的SiO2、Fe2O3雜質)是工業上制取鋁的原料。實驗室模擬工業上以鋁土礦為原料制取Al2(SO4)3和銨明礬晶體[NH4Al(SO4)2·12H2O]的工藝流程如圖所示:
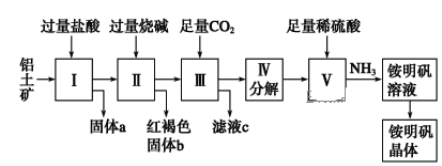
請回答下列問題:
(1)固體a的化學式為________。
(2)寫出Ⅱ中加過量的燒堿涉及到的反應離子方程式______________、_____________;Ⅲ中通入足量CO2氣體發生反應的離子方程式為_________________。
(3)由Ⅲ中得到濾液c的實驗操作為__________,從銨明礬溶液中獲得銨明礬晶體的實驗操作依次為(填操作名稱)________、冷卻結晶、過濾洗滌。
(4)濾液c顯________性,日常生活中常用其溶質來________________(任寫一點);
(5)向銨明礬NH4Al(SO4)2中加氫氧化鋇使硫酸根離子完全沉淀化學方程式為_____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com