
分析 (1)氨氣分子中原子物質的量為氨氣的4倍,根據原子數目相等計算水的物質的量,再根據N=nNA計算水分子數目;
(2)含有相同氧原子數目的NO和NO2兩種氣體,則NO、NO2的物質的量之比為2:1,根據m=nM計算二者質量之比,相同條件下,氣體的體積之比等于其物質的量之比;
(3)根據電荷守恒:c(Na+)+2c(Mg2+)=c(Cl-)+2c(SO42-).
解答 解:(1)氨氣分子中原子物質的量為0.3mol×4=1.2mol,與之含有相同原子數目的水的物質的量為$\frac{1.2mol}{3}$=0.4mol,則水分子數目為0.4mol×6.02×1023 mol-1=2.408×1023,
故答案為:2.408×1023;
(2)含有相同氧原子數目的NO和NO2兩種氣體,則NO、NO2的物質的量之比為2:1,根據m=nM可知二者質量之比=30g/mol×2mol:46g/mol×1=30:23,相同條件下,氣體的體積之比等于其物質的量之比,故二者體積之比為2:1,
故答案為:30:23;2:1;2:1;
(3)根據電荷守恒:c(Na+)+2c(Mg2+)=c(Cl-)+2c(SO42-),則:
0.2mol•L-1+2×0.25mol•L-1=0.4mol•L-1+2c(SO42-)
解得c(SO42-)=0.15 mol•L-1
故答案為:0.15 mol•L-1.
點評 本題考查物質的量有關計算,比較基礎,注意電解質混合溶液中常利用電荷守恒進行離子濃度及物質的量的計算.


科目:高中化學 來源: 題型:選擇題
| A. | CH3COOH 溶液加水稀釋后,溶液中$\frac{c(CH3COOH)}{c(CH3COO-)}$ 的值減小 | |
| B. | 已知一定溫度下,醋酸溶液的物質的量濃度為c,電離度為α,Ka=$\frac{{{{(cα)}^2}}}{c(1-α)}$.若加入少量醋酸鈉固體,則CH3COOH?CH3COO-+H+向左移動,α減小,Ka變小 | |
| C. | 實驗測得環己烷(l)、環己烯(l)和苯(l)的標準燃燒熱分別為-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以證明在苯分子中不存在獨立的碳碳雙鍵 | |
| D. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol. CO(g)+$\frac{1}{2}$O2(g)═CO2(g),△H=-283.0 kJ/mol. C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol. 則4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

 .
. +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
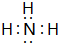 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 原子序數依次增大的五種元素A、B、C、D、E,其中A是周期表中原子半徑最小元素,B原子基態時最外層電子數是其內層電子數的2倍,D原子基態時2p原子軌道上有2個未成對的電子,E的原子序數為29.回答下列問題(所有元素均用元素符號表示):
原子序數依次增大的五種元素A、B、C、D、E,其中A是周期表中原子半徑最小元素,B原子基態時最外層電子數是其內層電子數的2倍,D原子基態時2p原子軌道上有2個未成對的電子,E的原子序數為29.回答下列問題(所有元素均用元素符號表示):查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學的特征是認識分子 | |
| B. | 新制氯水應保存在棕色試劑瓶中,放于陰涼處 | |
| C. | 在化學反應中,參加反應的各物質的質量比等于其物質的量之比 | |
| D. | 英國化學家玻義耳提出原子學說,為近代化學的發展奠定了堅實的基礎 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 在一定條件下,向某一密閉容器中,加入一定量的HI或加入一定量的PCl5,反應達到平衡后,在t時刻改變條件,其反應速率與時間的變化關系均可用圖表示.那么對于不同反應在t時刻改變條件的敘述正確的是( )
在一定條件下,向某一密閉容器中,加入一定量的HI或加入一定量的PCl5,反應達到平衡后,在t時刻改變條件,其反應速率與時間的變化關系均可用圖表示.那么對于不同反應在t時刻改變條件的敘述正確的是( )| A. | 對于2HI(g)?I2(g)+H2(g)反應,t時刻保持溫度和體積不變,再加入一定量的HI | |
| B. | 對于2HI(g)?I2(g)+H2(g)反應,t時刻保持溫度和壓強不變,再加入一定量的HI | |
| C. | 對于PCl5(g)?PCl3(g)+Cl2(g)反應,t時刻保持溫度和體積不變,再加入一定量的PCl5 | |
| D. | 對于PCl5 (g)?PCl3(g)+Cl2(g)反應,t時刻保持溫度和壓強不變,再加入一定量的PCl3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| C-F | 427 | C-Cl | 330 | C-I | 218 |
| H-H | 436 | S=S | 255 | H-S | 339 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com