
 ,而不排布成
,而不排布成 ,其直接的根據是洪特規則.
,其直接的根據是洪特規則. 分析 (1)3d軌道半充滿說明3d軌道中含有5個電子,根據電子排布規則知,該原子的4s能級上電子全滿或半充滿,結合構造原理來分析解答;
(2)根據激發態原子核外電子排布式確定該原子核外電子數,原子中核外電子數=原子序數,從而確定該元素,根據構造原理寫出該元素基態原子核外電子排布式;
(3)洪特規則要求電子優先占據一個空軌道,并且在一個軌道中自旋方向相反.
解答 解:(1)3d軌道半充滿說明3d軌道中含有5個電子,根據電子排布規則知,該原子的4s能級上電子全滿或半充滿,所以該基態原子的核外電子排布式為:[Ar]3d54s1或[Ar]3d54s2,所以為Cr和Mn,則原子序數比較小的Cr元素基態原子的電子排布式為[Ar]3d54s1;有6個未成對電子;
故答案為:Cr;Mn;[Ar]3d54s1;6;
(2)根據激發態原子核外電子排布式知該元素核外有16個電子,根據構造原理知,其基態原子核外電子排布式為:1s22s22p63s23p4,故答案為:1s22s22p63s23p4;
(3)因為洪特規則要求電子優先占據一個空軌道,并且在一個軌道中自旋方向相反,所以在d軌道中電子排布成 ,而不排布成
,而不排布成 ,其直接的根據是洪特規則,故答案為:洪特規則;
,其直接的根據是洪特規則,故答案為:洪特規則;
點評 本題考查了元素核外電子排布,明確電子排布規則即構造原理是解本題關鍵,注意原子軌道中電子處于全空、半滿、全滿時最穩定,難度中等.


科目:高中化學 來源: 題型:選擇題
| A | B | C | D | |
| 電解質溶液 | HCl | AgNO3 | BaCl2 | KOH |
| pH值變化 | 減小 | 增大 | 變大 | 不變 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH3的百分含量不變 | B. | N2的體積分數增大 | ||
| C. | N2的轉化率增大 | D. | NH3的百分含量增小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
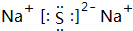 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向鐵粉中加入稀硝酸 | |
| B. | 向燒堿溶液中通入CO2氣體 | |
| C. | 向稀鹽酸中滴入少量的NaAlO2溶液 | |
| D. | 向MgSO4、H2SO4的混合溶液中加入過量的Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗 | 實驗目的 |
| A | 鈉和鎂分別投入冷水中 | 判斷鈉和鎂金屬性強弱 |
| B | 在MgCl2與AlCl3溶液中分別加入過量的氨水 | 判斷鎂與鋁的金屬性強弱 |
| C | 向硅酸鈉溶液中通入CO2 | 判斷碳酸與硅酸的酸性強弱 |
| D | Br2與I2分別與足量的H2反應 | 判斷溴與碘的非金屬性強弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
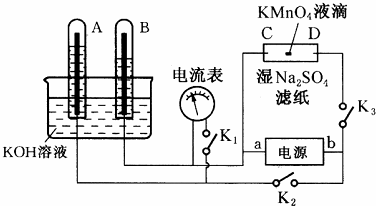
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
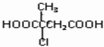 的合成路線流程圖(無機試劑任選).合成路線流程圖示例如下:(RCH3CH=CH2+HCl$\stackrel{催化劑}{→}$RCH3CHClCH3)
的合成路線流程圖(無機試劑任選).合成路線流程圖示例如下:(RCH3CH=CH2+HCl$\stackrel{催化劑}{→}$RCH3CHClCH3)  .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com