
| A. | 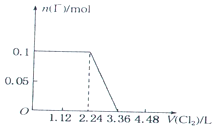 | B. | 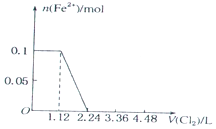 | ||
| C. | 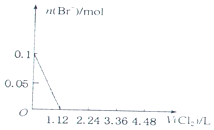 | D. | 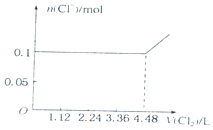 |
分析 離子還原性I->Fe2+>Br-,故首先發生反應2I-+Cl2=I2+2Cl-,然后發生反應2Fe2++Cl2=2Fe3++2Cl-,最后發生反應2Br-+Cl2=Br2+2Cl-,根據發生反應順序計算離子開始反應到該離子反應完畢時氯氣的體積,據此判斷.
解答 解:A、0.1molI-完全反應消耗0.05氯氣,所以一開始時碘離子的物質的量就減少,故A錯誤;
B、0.1molI-完全反應消耗0.05氯氣,故亞鐵離子開始反應時氯氣的體積為0.05mol×22.4L/mol=1.12L,由2Fe2++Cl2=2Fe3++2Cl-可知,0.1molFe2+完全反應消耗0.05氯氣,故Fe2+完全時消耗的氯氣體積為0.1mol×22.4L/mol=2.24L,圖象與實際符合,故B正確;
C、開始階段與還原強的碘離子反應,而不是溴離子,故C錯誤;
D、只要氧化還原反應發生,氯離子的物質的量就在增大,故D錯誤;
故選B.
點評 本題以圖象形式考查氧化還原反應、有關離子反應計算等,難度中等,確定離子反應發生的先后順序是解題的關鍵.


科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
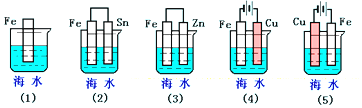
| A. | (5)(2)(1)(3)(4) | B. | (2)(5)(3)(4)(1) | C. | (5)(3)(4)(1)(2) | D. | (1)(5)(3)(4)(2) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過氧化鈉加入到紫色石蕊試液中,紫色石蕊先變紅后褪色且有氣泡產生 | |
| B. | 冷的濃硫酸和濃硝酸都可以用鋁、鐵的容器盛裝 | |
| C. | 硅、氯、硫、氮、鈉元素在自然界只有化合態沒有游離態 | |
| D. | 濃硝酸有氧化性,稀硝酸沒有氧化性 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶于水能導電,屬于電解質 | |
| B. | 使品紅溶液褪色,有漂白性 | |
| C. | 使酸性高錳酸鉀溶液褪色,有還原性 | |
| D. | 能殺菌、消毒,可按照國家標準用作食物的防腐劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
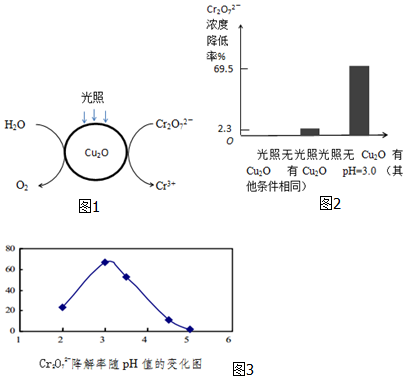
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com