
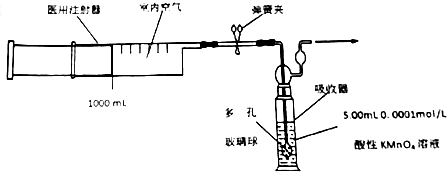
分析 實驗操作:用容積為1000mL的醫用注射器抽取空氣,緩慢注入酸性高錳酸鉀溶液中(裝置如圖),當酸性高錳酸鉀溶液正好褪色時,停止注入.
①依據溶質物質的量不變列式計算;
②在吸收器中注入水并使其淹沒多孔玻璃球,改變容器中的溫度,若導氣管出現液面上升可證明氣密性完好,多孔玻璃球的作用是增大吸收面積,吸收充分;
③根據高錳酸鉀的質量計算甲醛的質量,然后計算空氣中甲醛的含量和標準進行比較得出結論;
④甲醛是氣體可以開窗通風措施減少室內空氣污染;
解答 解:①用0.1000mol/L的酸性KMnO4溶液配制實驗中使用的酸性KMnO4溶液1000mL,濃度為0.00010mol/L,溶質物質的量不變列式計算得到,0.1000mol/L×V=0.00010mol/L×1000mL
V=1ml
需0.1000mol/L的酸性KMnO4溶液的體積為1ml,
故答案為:1ml;
②在吸收器中注入水并使其淹沒多孔玻璃球,用手捂住吸收器下半部,若一段時間后導管中液面上升,表示氣密性良好,裝置中多孔玻璃球的作用是使甲醛被酸性高錳酸鉀溶液充分吸收,
故答案為:在吸收器中注入水并使其淹沒多孔玻璃球,用手捂住吸收器下半部,若一段時間后導管中液面上升,表示氣密性良好;甲醛被酸性高錳酸鉀溶液充分吸收;
③設甲醛的質量為x
4KMnO4 +6H2SO4+5CH2O=4MnSO4+2K2SO4+5CO2↑+11H2O
4 150
5×10-3 L×0.0001mol/L x
x=1.875×10-5g=0.01875mg
因為每次用注射器抽取1000mL室內空氣,第200次恰好反應,則通入的空氣體積為:1000ml×200=200000mL=0.2m3,所以該居室內空氣中甲醛的含量=$\frac{0.01875mg}{0.2{m}^{3}}$=0.09375mg/m3>0.08mg/m3,故甲醛超標,
答:該居室空氣中甲醛含量超標;
(3)開窗通風可降低室內甲醛的含量,故答案:多開窗通風
點評 本題是有關室內甲醛含量的測定的探究,涉及的知識點較多:質量守恒定律的運用、根據化學式的計算、根據化學方程式的計算等,綜合性較強,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 在pH=1的溶液中:NH4+、ClO-、Cl- | |
| B. | 有SiO32-存在的溶液中:Na+、SO42-、Cl- | |
| C. | 有NO3-存在的溶液中:H+、Ba2+、Fe2+ | |
| D. | 室溫下,水電離的c水(H+)=1.0×10-13mol•L-1溶液中:Na+、S2-、AlO2- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 聚乙烯、聚氯乙烯、纖維素都屬于合成高分子 | |
| B. | 油脂、淀粉和蛋白質都是食物中含有的重要營養物質,一定條件下都能水解 | |
| C. | 除去乙酸乙酯中的少量乙酸,可加入氫氧化鈉溶液充分反應后分液 | |
| D. | 丙烷的同分異構體共有3種 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
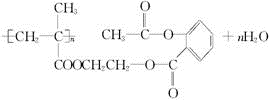
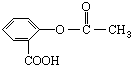 ,它可以接在一種高聚物載體上形成緩釋長效藥劑.其中的一種結構如下:
,它可以接在一種高聚物載體上形成緩釋長效藥劑.其中的一種結構如下: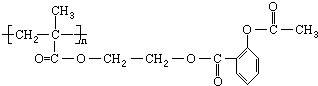
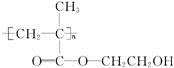 .
.
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 容器內壓強不再發生變化 | |
| B. | v正(CO)=v正(H2O) | |
| C. | 生成n mol CO的同時,消耗n mol H2O | |
| D. | 1 mol H-H鍵斷裂的同時,形成2 mol H-O鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鋇溶液與硫酸的反應OH-+H+═H2O | |
| B. | 鐵與稀硫酸反應:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 銅片插入硝酸銀溶液中Cu+Ag+═Cu2++Ag | |
| D. | 金屬鈉與水反應:2Na+2H2O═2Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 物質均是由分子構成,分子均是由原子構成的 | |
| B. | 某物質經測定,只含有一種組成元素,則該物質一定是單質 | |
| C. | 純凈的硫酸是純凈物,而不含雜質的鹽酸是混合物 | |
| D. | 堿性氧化物均是金屬氧化物,酸性氧化物均是非金屬氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.0mol•L-1 | B. | 0.10mol•L-1 | C. | 1.0mol•L-1 | D. | 0.50mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com