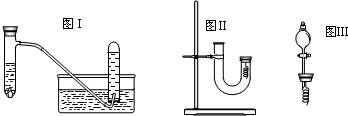
甲同學釆用如圖Ⅰ所示裝置驗證銅與稀硝酸的反應,并用排水法收集NO氣體
(1)寫出試管內溶液中發生反應的化學方程式
3Cu+8HNO3=3Cu(NO3 ) 2+2NO↑+4H2O
3Cu+8HNO3=3Cu(NO3 ) 2+2NO↑+4H2O
(2)在實驗過程中觀察到試管內的溶液呈
綠
綠
色;收集氣體的試管內的氣體呈
無
無
色
(3)乙同學認為甲雖然收集到的氣體是一氧化氮,但并不能說明反應中一定生成一氧化氮.他的理由是
在銅和稀硝酸反應容器的上部看到了紅棕色氣體
在銅和稀硝酸反應容器的上部看到了紅棕色氣體
在銅和稀硝酸反應容器的上部看到了紅棕色氣體
在銅和稀硝酸反應容器的上部看到了紅棕色氣體
有關化學方程式為:
2NO+O2=2NO2
2NO+O2=2NO2
(4)丙同學釆用如圖Ⅱ所示裝置進行實驗,證明了銅與稀硝酸反應生成一氧化氮.該同學的步驟如下表所示,請回答實驗中的有關問題.
| 實驗步驟 |
問題 |
| 1從U型管左端加入稀硝酸直至充滿U型管右端 |
∥/ |
| 2用附有銅絲的膠塞塞住U型管右端,觀察現象 |
現象是 有無色氣體產生,右邊溶液逐漸變成綠色 有無色氣體產生,右邊溶液逐漸變成綠色 |
| 3待反應停止后打開膠塞,觀察實驗現象 |
現象是 無色氣體與空氣接觸后立即變成紅棕色 無色氣體與空氣接觸后立即變成紅棕色 |
(5)從環保的角度看,丙同學的實驗存在的缺陷是
將氮氧化合物放入空氣中會污染環境
將氮氧化合物放入空氣中會污染環境
.
(6)丁同學用圖Ⅲ所示裝置代替圖Ⅱ中U型管右端的附有銅絲的膠塞進行實驗,待反應停止后將一氧化氮氣體排入分液漏斗中,觀察到的實驗現象與丙同學實驗的第
3
3
步驟的相同.丁同學要將一氧化氮氣體排入分液漏斗中應進行的正確操作是①
打開分液漏斗上部的塞子
打開分液漏斗上部的塞子
②
慢慢打開分液漏斗的活塞
慢慢打開分液漏斗的活塞
③
待液面與膠塞接觸時立即關閉活塞
待液面與膠塞接觸時立即關閉活塞
(7)實驗結束后丁同學向分液漏斗中注入適量水并充分振蕩,試寫出發生的化學反應方程式
3NO2+H2O=2 HNO3+NO
3NO2+H2O=2 HNO3+NO
(8)若將32.64g銅與140mL一定濃度的硝酸反應,銅完全溶解,產生的NO和NO
2混合氣體在標準狀況下的體積為11.2L(不考慮NO
2的反應),試回答:
①若銅與硝剛好反應完全,則原硝酸溶液的物質的量濃度為
10.86mol﹒L-1
10.86mol﹒L-1
②將產生的氣體全部釋放后,向溶液中加入VmL amol?L
-1的NaOH溶液,恰好使溶液中的Cu
2+全部轉化為沉淀,則原硝酸溶液的物質的量濃度為
③已知NO和NO
2的混合氣與足量氧氣混合后能被水完全吸收成硝酸,則要使上述11.2L氣體完全被水吸收成硝酸,理論上需消耗標準狀況下的氧氣
5.71
5.71
升.(保留兩位小數);解題過程:
設生成的一氧化氮為xmol,二氧化氮為ymol.
3Cu+8HNO
3=3Cu(NO
3 )
2+2NO↑+4H
2O
3 2
1.5xmol xmol
Cu+4HNO
3(濃)=Cu(NO
3 )
2+2NO
2↑+2H
2O
1 2
ymol.ymol.
所以方程組為
所以
即一氧化氮為0.26mol,二氧化氮為0.24mol.
4NO+2H
2O+3O
2=4HNO
3
4 3
0.26mol 0.195mol
4 NO
2+2H
2O+O
2=4HNO
341
0.24mol 0.06mol
所以需要氧氣0.195mol+0.06mol=0.255mol,體積為0.255mol×22.4L/mol=5.71L
設生成的一氧化氮為xmol,二氧化氮為ymol.
3Cu+8HNO
3=3Cu(NO
3 )
2+2NO↑+4H
2O
3 2
1.5xmol xmol
Cu+4HNO
3(濃)=Cu(NO
3 )
2+2NO
2↑+2H
2O
1 2
ymol.ymol.
所以方程組為
所以
即一氧化氮為0.26mol,二氧化氮為0.24mol.
4NO+2H
2O+3O
2=4HNO
3
4 3
0.26mol 0.195mol
4 NO
2+2H
2O+O
2=4HNO
341
0.24mol 0.06mol
所以需要氧氣0.195mol+0.06mol=0.255mol,體積為0.255mol×22.4L/mol=5.71L
.




