
(14分)
(1)反應Fe(s)+CO2(g)FeO(s)+CO(g) △H1,平衡常數為K1
反應Fe(s)+H2O(g)FeO(s)+H2(g) △H2,平衡常數為K2
在不同溫度時K1、K2的值如下表:
|
| 700℃ | 900℃ |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
①反應 CO2(g) + H2(g)CO(g) + H2O(g) △H,平衡常數K,則△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述計算可知,反應
CO2(g) + H2(g)CO(g) + H2O(g)是 反應(填“吸熱”或“放熱”)。
②能判斷CO2(g) + H2(g)CO(g) + H2O(g)達到化學平衡狀態的依據是 (填序號)。
A.容器中壓強不變 B.混合氣體中c(CO)不變
C.v正(H2)= v逆(H2O) D.c(CO)= c(CO2)
(2)一定溫度下,向某密閉容器中加入足量鐵粉并充入一定量的CO2氣體,發生反應Fe(s)+CO2(g)FeO(s)+CO(g) △H > 0,CO2的濃度與時間的關系如圖所示:
① 該條件下反應的平衡常數為 ;若鐵粉足量,CO2的起始濃度為2.0 mol·L-1,則平衡時CO2的濃度為 mol·L-1。
②下列措施中能使平衡時增大的是 (填序號)
A.升高溫度
B.增大壓強
C.充入一定量的CO2
D.再加入一定量鐵粉
科目:高中化學 來源: 題型:
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
| K1 |
| K2 |
| K1 |
| K2 |
| 各物質某一狀態時的物質的量濃度/mol?L-1 | ||||||
| c(CO2) | c(H2 ) | c(CO) | c(H2O ) | Qc | 平衡 | |
| ① | 0.004 | 0.004 | 0.006 | 0.006 | 已達平衡 | |
| ② | 0.062 | 0.084 | 0.039 | 0.279 | 2.09 | |
| ③ | 0.182 | 0.086 | 0.098 | 0.359 | 2.25 | |
| ④ | 0.078 | 0.142 | 0.280 | 0.120 | 平衡逆向移動 | |
查看答案和解析>>
科目:高中化學 來源: 題型:
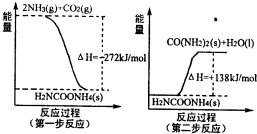
| 溫度/ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
2- 3 |
- 3 |
2- 3 |
- 3 |
- 3 |
2- 3 |
2- 3 |
- 3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 編號 | 化學方程式 | 平衡常數 | 溫度 | |
| 979K | 1173K | |||
| Ⅰ | Fe(s)+CO2?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| Ⅱ | CO(g)+H2O(g)?CO2(g)+H2(g) | K2 | 1.62 | b |
| Ⅲ | Fe(s)+H2O(g)? FeO(s)+H2(g) |
K3 | a | 1.68 |
| A、a>b |
| B、增大壓強;平衡狀態II不移動 |
| C、升高溫度平衡狀態Ⅲ向正反應方向移動 |
| D、反應Ⅱ,Ⅲ均為放熱反應 |
查看答案和解析>>
科目:高中化學 來源:2011-2012學年湖北省襄陽市高三3月調研考試理科綜合試卷(化學部分) 題型:填空題
(14分)
(1)反應Fe(s)+CO2(g) FeO(s)+CO(g)
△H1,平衡常數為K1
FeO(s)+CO(g)
△H1,平衡常數為K1
反應Fe(s)+H2O(g) FeO(s)+H2(g) △H2,平衡常數為K2
FeO(s)+H2(g) △H2,平衡常數為K2
在不同溫度時K1、K2的值如下表:
|
|
700℃ |
900℃ |
|
K1 |
1.47 |
2.15 |
|
K2 |
2.38 |
1.67 |
①反應 CO2(g) + H2(g) CO(g) + H2O(g) △H
,平衡常數K,則△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述計算可知,反應
CO(g) + H2O(g) △H
,平衡常數K,則△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述計算可知,反應
CO2(g) + H2(g) CO(g) + H2O(g)是 反應(填“吸熱”或“放熱”)。
CO(g) + H2O(g)是 反應(填“吸熱”或“放熱”)。
②能判斷CO2(g) + H2(g) CO(g) + H2O(g)達到化學平衡狀態的依據是 (填序號)。
CO(g) + H2O(g)達到化學平衡狀態的依據是 (填序號)。
A.容器中壓強不變 B.混合氣體中c(CO)不變
C.v正(H2)= v逆(H2O) D.c(CO)= c(CO2)
(2)一定溫度下,向某密閉容器中加入足量鐵粉并充入一定量的CO2氣體,發生反應Fe(s)+CO2(g) FeO(s)+CO(g) △H > 0,CO2的濃度與時間的關系如圖所示:
FeO(s)+CO(g) △H > 0,CO2的濃度與時間的關系如圖所示:
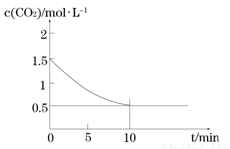
① 該條件下反應的平衡常數為 ;若鐵粉足量,CO2的起始濃度為2.0 mol·L-1,則平衡時CO2的濃度為 mol·L-1。
②下列措施中能使平衡時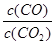 增大的是 (填序號)
增大的是 (填序號)
A.升高溫度
B.增大壓強
C.充入一定量的CO2
D.再加入一定量鐵粉
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com