
【題目】以某鉻礦石(主要成分是Cr2O3,含FeO、SiO2等雜質)為原料生產Cr2O3的流程如下:
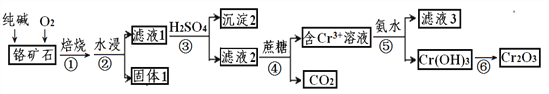
已知:Cr2O72-+H2O![]() 2CrO42-+2H+,Ksp[Cr(OH)3] =6.4×10-31,lg2 = 0.3
2CrO42-+2H+,Ksp[Cr(OH)3] =6.4×10-31,lg2 = 0.3
(1)步驟①中為了提高反應速率應該采取的措施有____、_____。(寫2種)
(2)焙燒時Cr2O3被氧化成Na2CrO4,配平下面的化學方程式,并用單線橋表示電子轉移的方向和數目:
Na2CO3+ Cr2O3+ O2![]() Na2CrO4 + CO2,______________
Na2CrO4 + CO2,______________
(3)流程中沉淀2為_________(填化學式)
(4)步驟④發生的反應中Cr2O72-和蔗糖(C12H22O11)的物質的量之比為_____。
(5)步驟⑤中為了使Cr3+完全沉淀[此時,c(Cr3+)≤10-5mol·L-1],pH至少調至____。
(6)濾液3中的主要溶質是兩種鹽,化學式為_________、________。
(7)另一種制取Cr(OH)3的工藝是將NaCrO2溶解后通入CO2得到更為純凈的Cr(OH)3,則NaCrO2溶液與過量CO2反應的離子方程式為_____________________。。
【答案】 適當升溫 粉碎鉻礦石或攪拌等合理答案  H2SiO3 8:1 5.6 (NH4)2SO4 Na2SO4 CrO2- + CO2 +2H2O = Cr(OH)3↓+ HCO3-
H2SiO3 8:1 5.6 (NH4)2SO4 Na2SO4 CrO2- + CO2 +2H2O = Cr(OH)3↓+ HCO3-
【解析】(1)步驟①中為了提高反應速率應該采取的措施有適當升溫 、粉碎鉻礦石或攪拌等;正確答案: 適當升溫 、粉碎鉻礦石。
(2)Cr元素由+3價升高到+6價,氧元素由0價降低到-2價,根據元素得失電子數相等規律,找出最小公倍數,填系數最后根據原子守恒進行其他物質的配平。根據所填系數,可知該反應共轉移電子12e-;單線橋注意是還原劑把電子給了氧化劑;正確答案:
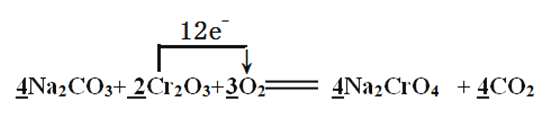
(3)二氧化硅與純堿加熱反應生成硅酸鈉,加入稀硫酸后,產生了硅酸沉淀;正確答案:H2SiO3。
(4)根據流程分析看出:設Cr2O72-有xmol, C12H22O11有y mol,根據電子守恒:x×2×(6-3)=y×12×(4-0),解之得x:y=8:1;正確答案:8:1。
(5)根據Ksp[Cr(OH)3] = c(Cr3+)×c3(OH-)=10-5×c3(OH-)=6.4×10-31,c3(OH-)=6.4×10-26mol/L,c(OH-)=4×10-9mol/L, c(H+)=1/4×10-5mol/L, 已知lg2 = 0.3,pH=6-0.3=5.7;正確答案:5.6或5.7(近似值)
(6)整個流程中加入了碳酸鈉、加入了硫酸,經過一系列反應后,溶液中剩下鈉離子和硫酸根離子,加入氨水后,剩余銨根離子,因此濾液3中的主要溶質是兩種鹽,化學式為(NH4)2SO4 、 Na2SO4 ; 正確答案:NH4)2SO4 、Na2SO4。
(7)利用強酸制備弱酸的規律:NaCrO2溶液與過量CO2反應生成碳酸氫鈉和Cr(OH)3,離子方程式:CrO2- + CO2 +2H2O = Cr(OH)3↓+ HCO3-;正確答案:CrO2- + CO2 +2H2O = Cr(OH)3↓+ HCO3-。


 口算題卡北京婦女兒童出版社系列答案
口算題卡北京婦女兒童出版社系列答案科目:高中化學 來源: 題型:
【題目】向5 mL NaCl溶液中滴入一滴AgNO3溶液,出現白色沉淀,繼續滴加一滴KI溶液并振蕩,沉淀變為黃色,再滴入一滴Na2S溶液并振蕩,沉淀又變成黑色,根據上述變化過程,分析此三種沉淀物的溶解度關系為
A. AgCl=AgI=Ag2S B. AgCl<AgI<Ag2S
C. AgCl>AgI>Ag2S D. AgI>AgCl>Ag2S
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究發現,可以用石墨作陽極、鈦網作陰極、熔融CaF2—CaO作電解質,利用圖示裝置獲得金屬鈣,并以鈣為還原劑還原二氧化鈦制備金屬鈦。下列說法中正確的是( )
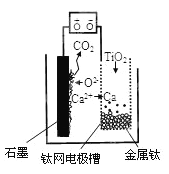
A. 將熔融CaF2—CaO換成Ca(NO3)2溶液也可以達到相同目的
B. 陽極的電極反應式為:C+2O2--4e-=CO2↑
C. 在制備金屬鈦前后,整套裝置中CaO的總量減少
D. 石墨為陰極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質中,能與Fe3+反應,且能證明Fe3+具有氧化性的是( )
①SCN﹣;②Fe;③Fe2+;④Cu;⑤Zn;⑥OH﹣ .
A.①②③
B.②④⑤
C.①③⑥
D.①②⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g)。平衡常數如下表:下列說法正確的是( )
CH3OH(g)。平衡常數如下表:下列說法正確的是( )
溫度/℃ | 0 | 100 | 200 | 300 | 400 |
平衡常數 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A. 該反應的△H> 0
B. 加壓、增大H2濃度和加入催化劑都能提高CO的轉化率
C. 工業上采用5 ×103 kPa和 250℃的條件,其原因是原料氣的轉化率高
D. t℃時,向 1 L密閉容器中投入0.1 mol CO和0.2 mol H2,平衡時CO轉化率為50%,則該溫度時反應的平衡常數的數值為100
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是部分短周期元素的常見化合價與原子序數的關系:
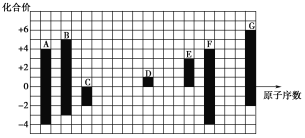
(1)元素A在周期表中的位置為________________________。
(2)用電子式表示D2G的形式過程:__________________________________,其所含化學鍵類型為__________。
(3)C2-、D+、G2-半徑由大到小的順序是________(填離子符號)。
(4)C、G的簡單氫化物中,沸點較低的是________(填化學式),原因是________________。兩種氣態氫化物的穩定性C________G(填“>”或“<”)。
(5)C與D形成的具有強氧化性的化合物的電子式為________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com