
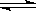 2HI(g)△ H<0,并達到平衡,HI的體積分數ω(HI)隨時間變化如圖(Ⅱ)所示。若改變反應條件, ω(HI)的變化曲線如圖(Ⅰ)所示,則改變的條件可能是
2HI(g)△ H<0,并達到平衡,HI的體積分數ω(HI)隨時間變化如圖(Ⅱ)所示。若改變反應條件, ω(HI)的變化曲線如圖(Ⅰ)所示,則改變的條件可能是 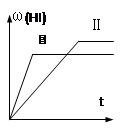
| A.恒溫恒容條件下,加入適當催化劑 |
| B.恒溫條件下,縮小反應容器體積 |
| C.恒容條件下升高溫度 |
| D.恒溫條件下,擴大反應容器體積 |
科目:高中化學 來源:不詳 題型:單選題

| A.高溫、高壓 | B.適宜溫度、高壓、催化劑 |
| C.低溫、低壓、不斷分離出甲醇 | D.低溫、高壓、催化劑 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題
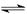 xB(氣)+C(氣)并達到平衡,A在平衡混合氣中的體積百分含量為58.6%,混合氣的總質量為46g,密度為0.72g·L-1。求:
xB(氣)+C(氣)并達到平衡,A在平衡混合氣中的體積百分含量為58.6%,混合氣的總質量為46g,密度為0.72g·L-1。求:查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO3(g) ΔH<0,某研究小組研究了其他條件不變時,改變某一條件對上述反應的影響,下列分析正確的是
2SO3(g) ΔH<0,某研究小組研究了其他條件不變時,改變某一條件對上述反應的影響,下列分析正確的是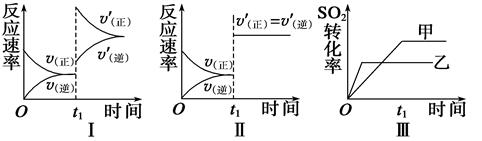
| A.圖Ⅰ表示的是t1時刻增大O2的濃度對反應速率的影響 |
| B.圖Ⅱ表示的是t1時刻加入催化劑后對反應速率的影響 |
| C.圖Ⅲ表示的是催化劑對平衡的影響,且甲的催化效率比乙高 |
| D.圖Ⅲ表示的是壓強對化學平衡的影響,且乙的壓強較高 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
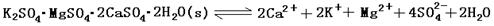
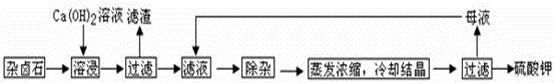
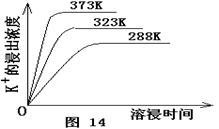

查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2NH3(g) △H =-92.3kJ·mol-1,在一定溫度和催化劑的條件下,向一密閉容器中,通入1molN2和3molH2,達到平衡狀態I;相同條件下,向另一體積相同的密閉容器中通入0.9molN2、2.7molH2和0.2molNH3,達到平衡狀態II,則下列說法正確的是
2NH3(g) △H =-92.3kJ·mol-1,在一定溫度和催化劑的條件下,向一密閉容器中,通入1molN2和3molH2,達到平衡狀態I;相同條件下,向另一體積相同的密閉容器中通入0.9molN2、2.7molH2和0.2molNH3,達到平衡狀態II,則下列說法正確的是| A.兩個平衡狀態的平衡常數的關系:KI < KII | B.H2的百分含量相同 |
| C.N2的轉化率:平衡I <平衡II | D.反應放出的熱量:QI =QII < 92.3 kJ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
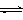 CH3OH(g)+H2O(g);△H=-49.0kJ/mol測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g)+H2O(g);△H=-49.0kJ/mol測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
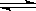 CO(g)+H2O(g),
CO(g)+H2O(g),| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.向SO2水溶液中加鹽酸有利于SO32-離子濃度的減少 |
| B.加入催化劑有利于氨的氧化反應 |
| C.室溫下比高溫更有利于合成氨中氨的生成 |
| D.用排飽和食鹽水來除Cl2中HCl |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com