
【題目】50mL0.5mol·L-1的鹽酸與50mL0.55mol·L-1的NaOH溶液在下圖所示的位置中進行中和反應。通過測定反應過程中放出的熱量可計算中和熱。回答下列問題:
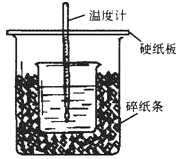
(1)從實驗裝置上看,圖中尚缺少的一種玻璃用品是__________。
(2)燒杯間填滿碎紙條的作用是____________。
(3)大燒杯上如不蓋硬紙板,求得的中和熱數值____(填“偏大、偏小、無影響”)
(4)如果用60mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液進行反應,與上述實驗相比,所放出的熱量_________(填“相等、不相等”),所求中和熱__________(填“相等、不相等”),簡述理由___________
(5)用相同濃度和體積的氨水(NH3·H2O)代替NaOH溶液進行上述實驗,測得的中和熱的數值會______________;(填“偏大”、“偏小”、“無影響”)。
(6)肼(N2H4)可作為火箭發動機的燃料,與氧化劑N2O4反應生成N2和水蒸氣。
已知:①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJmol-1
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJmol-1
寫出肼和N2O4反應的熱化學方程式________ 。
【答案】環形玻璃攪拌棒減少實驗過程中的熱量損失偏小不相等相等因為中和熱是指酸堿中和反應生成1mol水所放出的熱量,與酸堿用量無關偏小2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H=-1048.9kJ/mol
【解析】
(1)根據量熱計的構造可知該裝置的缺少儀器是環形玻璃攪拌器;
(2)中和熱測定實驗成敗的關鍵是保溫措施,大小燒杯之間填滿碎紙條的作用是:減少實驗過程中的熱量損失;
(3)大燒杯上如不蓋硬紙板,會有一部分熱量散失,求得的中和熱數值將會減小;
(4)反應放出的熱量和所用酸以及堿的量的多少有關,并若用60mL0.25mol·L﹣1H2SO4溶液跟50mL0.55mol·L﹣1NaOH溶液進行反應,與上述實驗相比,生成水的量增多,所放出的熱量偏高,但是中和熱的均是強酸和強堿反應生成1mol水時放出的熱,與酸堿的用量無關,所測得中和熱數值相等;
(5)氨水為弱堿,電離過程為吸熱過程,所以用氨水代替稀氫氧化鈉溶液反應,反應放出的熱量小于57.3kJ,故偏小;
(6)①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJmol-1
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJmol-1
根據蓋斯定律得出肼和N2O4反應的熱化學方程:②×2-①得到: 2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g),△H=△H2×2-△H1=-1048.9kJ/mol.


 直通貴州名校周測月考直通名校系列答案
直通貴州名校周測月考直通名校系列答案 培優三好生系列答案
培優三好生系列答案科目:高中化學 來源: 題型:
【題目】海水提鎂的主要流程如下,下列說法正確的是

①試劑M是鹽酸 ②流程中的反應全部都是非氧化還原反應
③操作b只是過濾 ④用海水曬鹽后的飽和溶液加石灰乳制Mg(OH)2
⑤采用電解法冶煉鎂是因為鎂很活潑
A. ①②③④⑤ B. ②③ C. ④⑤ D. ①④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】磷的單質和化合物在科研與生產中有許多重要用途,銅及其合金是人類最早使用的金屬材料。請回答下列問題:
(1)白磷是磷的一種單質,其分子結構如圖所示,則一個分子中有____對成鍵電子對和____對孤電子對。

(2)N和P都有+5價,PCl5能形成離子型晶體,晶格中含有[PCl4]+和[PCl6]-,則[PCl4]+空間構型為______。
(3)電負性比較:P_____S(填“>”“=”“<”);而P的第一電離能比S大的原因是______。
(4)銅及其合金是人類最早使用的金屬材料,Cu2+能與NH3形成配位數為4的配合物[Cu(NH3)4]SO4。
①銅元素在周期表中的位置是__________ ,1mol[Cu(NH3)4]SO4 有___mol配位鍵 ;②[Cu(NH3)4]SO4中,存在的化學鍵的類型有_____(填標號)。
A.離子鍵 B.金屬鍵 C.配位鍵 D.非極性鍵 E.極性鍵
(5)磷化鎵(GaP)材料是研制微電子器件、光電子器件的新型半導體材料。GaP的晶體結構是閃鋅礦型結構(如圖所示),晶胞參數apm。
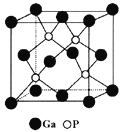
①與Ga緊鄰的P個數為________。
②GaP晶體的密度為(列出計算式) ______g·cm-3(NA為阿伏加德羅常數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校學習小組的同學擬用工業廢鐵屑(主要成分為Fe,還含有少量FeS、Fe3P等)制備FeSO4·7H2O,并探究FeSO4·7H2O高溫分解的產物。

I.制備實驗步驟如下:
①稱取一定量的廢鐵屑,用熱的碳酸鈉溶液浸泡,再用蒸餾水洗滌。
②將處理后的廢鐵屑放入錐形瓶中,加入適量3mol·L-1的硫酸,連接好裝置(如圖)后水浴加熱至反應完全。
③依據現象停止加熱,趁熱過濾,向濾液中補加少量硫酸。
④將濾液冷卻、結晶、過濾、洗滌。
回答下列問題
(1)步驟①稱量5.6g廢鐵屑時,若砝碼與物品的位置放反了,則稱得的廢鐵屑的質量會____ (填“增大”“減小”或“不變”)。
(2)步驟②中需控制硫酸的用量,使鐵粉過量,其目的是_____________________。
(3)裝置C的作用是__________________________。
(4)步驟④中洗滌時所用的洗滌劑最好是______(填標號)。
A.稀硝酸 B.無水乙醇 C.苯
(5)測定產品的純度:
稱取mg產品,放入錐形瓶中,用經煮沸過且冷卻的蒸餾水和稀硫酸溶解,然后用cmol·L-1的KMnO4標準溶液滴定,消耗VmLKMnO4標準溶液。
蒸餾水煮沸的原因:______________,KMnO4標準溶液用______(酸或堿)式滴定管,產品的純度為_______(列出計算表達式即可)。
Ⅱ.探究FeSO4·7H2O高溫分解的產物的實驗裝置及步驟如下,請完成相關填空:
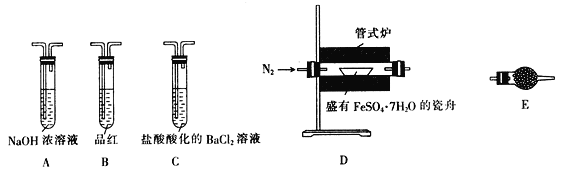
操作步驟 | 實驗現象 | 解釋原因 |
組裝好儀器,先充入氮氣,再加熱管式爐至700℃一段時間 | 試管E中的白色固體變藍 | 分解得到的產物中含水蒸氣 |
氣體產物經過試管B時 | 品紅溶液褪色 | (6) 產物中含有 _________________ |
氣體產物經過試管C時 | 試管C中出現白色沉淀 | (7)C中反應的化學方程式為 ___________________________ |
將瓷舟中反應后的固體溶于足量稀硫酸,再滴入幾滴KSCN溶液 | (8)____________________ | (9) 溶液中含有 _______________ |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】最新發現的第113號、115號、117號和118號元素已正式寫入元素周期表。根據物質結構、元素周期律的知識,下列說法正確的是( )
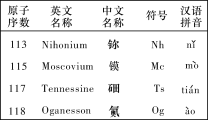
A. Nh(OH)3具有兩性
B. Mc位于元素周期表中第七周期第ⅤA族,其原子半徑小于Ts
C. Og是一種人工合成的稀有氣體元素,在元素周期表中位于第七周期0族
D. 若制得Ts的最高價氧化物對應的水化物,其酸性強于HClO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對塑料的敘述不正確的是 ( )
A.熱塑性塑料具有長鏈狀的線型結構
B.熱固性塑料在形成初期是長鏈狀的
C.熱固性塑料鏈與鏈之間會形成共價鍵,產生一些交聯
D.熱固性塑料在高溫時共價鍵也不斷裂
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用化學原理可以對工廠排放的廢水、廢渣等進行有效檢測與合理處理。某工廠對制革工業污泥中Cr(Ⅲ)的處理工藝流程如下圖所示:
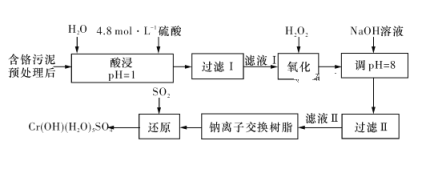
其中硫酸浸取液中的金屬離子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)實驗室用18.4 mol·L-1的濃硫酸配制240 mL 4.8 mol·L-1的硫酸溶液,需量取濃硫酸__________mL;配制時所用玻璃儀器除量筒、燒杯、膠頭滴管和玻璃棒外,還需____________。
(2)“酸浸”時,為了提高浸取率可采取的措施有__________________。
(3)H2O2的作用是將“濾液Ⅰ”中的Cr3+轉化為Cr2O72-,寫出此反應的離子方程式:___________________。
(4)常溫下,部分陽離子以氫氧化物形式沉淀時溶液的pH如下表所示:
陽離子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
開始沉淀時的pH | 2.7 | — | — | — |
沉淀完全時的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
加入NaOH溶液使溶液呈堿性,Cr2O72-轉化為CrO42-。過濾后“濾液Ⅱ”中的陽離子主要有Na+、Ca2+、Mg2+,但溶液的pH不能超過8,其理由是__________________。
(5)鈉離子交換樹脂的反應原理為Mn++nNaR===MRn+nNa+,利用鈉離子交換樹脂除去“濾液Ⅱ”中的金屬陽離子是________(填離子符號)。
(6)寫出上述流程中用SO2進行還原時發生反應的化學方程式:___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 同溫同壓下甲烷和氧氣的密度之比為2∶1
B. 1 g甲烷和1 g氧氣的原子數之比為5∶1
C. 等物質的量的甲烷和氧氣的質量之比為2∶1
D. 在標準狀況下等質量的甲烷和氧氣的體積之比為1∶2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com