
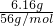 ;116x+89y=12.49
;116x+89y=12.49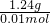 =124g/mol,
=124g/mol,

科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源:2011-2012學年江蘇省高三上學期質量檢測化學試卷 題型:填空題
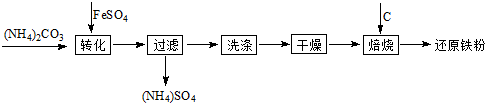
還原鐵粉是粉末冶金工業的重要原料,利用生產鈦白的副產品綠礬制備還原鐵粉的工業流程如下:
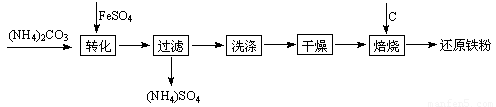
⑴干燥過程主要是為了脫去游離水和結晶水,過程中會有少量FeCO3·nH2O被空氣氧化為FeOOH,其化學方程式為 。
⑵取干燥后的FeCO3樣品12.49 g焙燒至600℃,質量變為8.00 g,繼續加熱最終得到Fe 6.16 g,則600℃產物的可能組成為 ,計算FeCO3樣品中FeCO3與FeOOH的質量。
⑶若將28.12 g還原鐵粉(含少量FexC)在氧氣流中加熱,得到標準狀況下的CO2 224 mL;將相同質量的還原鐵粉與足量硫酸反應,得到標準狀況下的H2 10.752 L,計算FexC的化學式。(假設還原鐵粉僅含兩種物質)
查看答案和解析>>
科目:高中化學 來源: 題型:
還原鐵粉是粉末冶金工業的重要原料,利用生產鈦白的副產品綠礬制備還原鐵粉的工業流程如下:
⑴干燥過程主要是為了脫去游離水和結晶水,過程中會有少量FeCO3·nH2O被空氣氧化為FeOOH,其化學方程式為 。
⑵取干燥后的FeCO3樣品12.49 g焙燒至600℃,質量變為8.00 g,繼續加熱最終得到Fe 6.16 g,則600℃產物的可能組成為 ,計算FeCO3樣品中FeCO3與FeOOH的質量。
⑶若將28.12 g還原鐵粉(含少量FexC)在氧氣流中加熱,得到標準狀況下的CO2 224mL;將相同質量的還原鐵粉與足量硫酸反應,得到標準狀況下的H210.752 L,計算FexC的化學式。(假設還原鐵粉僅含兩種物質)
查看答案和解析>>
科目:高中化學 來源:2012屆江蘇省如皋中學高三上學期質量檢測化學試卷 題型:填空題
還原鐵粉是粉末冶金工業的重要原料,利用生產鈦 白的副產品綠礬制備還原鐵粉的工業流程如下:
白的副產品綠礬制備還原鐵粉的工業流程如下: 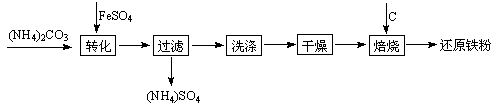
⑴干燥過程主要是為了脫去游離水和結晶水,過程中會有少量FeCO3·nH2O被空氣氧化為FeOOH,其化學方程式為 。
⑵取干燥后的FeCO3樣品12.49 g焙燒至600℃,質量變為8.00 g,繼續加熱最終得到Fe 6.16 g,則600℃產物的可能組成為 ,計算FeCO3樣品中FeCO3與FeOOH的質量。
⑶若將28.12 g還原鐵粉(含少量FexC)在氧氣流中加熱,得到標準狀況下的CO2 224 mL;將相同質量的還原鐵粉與足量硫酸反應,得到標準狀況下的H2 10.752 L,計算FexC的化學式。(假設還原鐵粉僅含兩種物質)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com