
【題目】草木灰主要成分是碳酸鉀。現從草木灰中提取鉀鹽,并用實驗檢驗其中的S![]() 、C
、C![]() 和Cl-。
和Cl-。
(1)從草木灰中提取鉀鹽的實驗操作順序如下:①稱量樣品,②溶解和沉淀,③______,④_______,⑤冷卻結晶。
(2)用托盤天平(指針向上的)稱量樣品時,若指針偏向右邊,則表示___。
A.左盤重,樣品輕 B.左盤輕,砝碼重
C.右盤重,砝碼輕 D.右盤輕,樣品重
(3)在進行②③④操作時都要用到玻璃棒,其作用分別是_____、______、______。
(4)將制得的少量晶體放入試管,加蒸餾水溶解并把溶液分成三份,分裝在三支試管里。
①在第一支試管里加入稀鹽酸,可觀察有___生成,證明溶液中有_____;
②在第二支試管里加入足量稀鹽酸后,再加入氯化鋇溶液,可觀察有________生成,證明溶液中有__________;
③在第三支試管里加入足量稀硝酸后,再加入硝酸銀溶液,可觀察有______生成,證明溶液中有Cl-。
【答案】過濾 蒸發 B 加速溶解 引流 受熱均勻(防止液體飛濺) 氣泡 ![]() 白色沉淀
白色沉淀 ![]() 白色沉淀
白色沉淀
【解析】
(1)草木灰中的鉀鹽可以溶于水中形成溶液,可以利用過濾的方法來獲得鉀鹽的水溶液;
(2)根據天平平衡的原理來回答;
(3)根據玻璃棒的作用是攪拌和引流來回答;
(4)①碳酸根離子可以和鹽酸反應生成水和二氧化碳;
②硫酸根離子可以和鋇離子之間反應生成不溶于酸的硫酸鋇沉淀;
③氯離子、碳酸根離子以及硫酸根離子均可以和銀離子反應生成沉淀。
(1)草木灰中的鉀鹽可以溶于水中形成溶液,然后利用過濾的方法可以獲得鉀鹽的水溶液,將所得的水溶液蒸發結晶可以獲得氯化鉀的固體;
(2) 用托盤天平稱量樣品時,若指針偏向右邊,則表示左盤輕、砝碼重,故答案為:B;
(3)在溶解固體時,使用玻璃棒可以加速溶解,在過濾操作中,可以用玻璃棒來引流,在蒸發結晶操作中,用玻璃棒來攪拌,使得受熱均勻(防止液體飛濺),故答案為:加速溶解;引流;受熱均勻(防止液體飛濺);
(4)①碳酸根離子能和鹽酸反應生成二氧化碳,向溶液中加入稀鹽酸后有氣泡生成說明有碳酸根離子,故答案為:氣泡;CO32-;
②向原溶液中滴加鹽酸酸化的氯化鋇溶液,排除了其它陰離子的干擾,如果產生白色沉淀,就說明溶液中有硫酸根離子,故答案為:白色沉淀;SO42-;
③向原溶液中滴加足量稀硝酸后,排除了其它離子的干擾,再加入AgNO3溶液,產生白色沉淀,說明溶液中有氯離子,故答案為:白色沉淀。


科目:高中化學 來源: 題型:
【題目】氧釩![]() 堿式碳酸銨
堿式碳酸銨![]() 難溶于水
難溶于水![]() 化學式為
化學式為![]() ,它是制備熱敏材料
,它是制備熱敏材料![]() 的原料。
的原料。![]() 價釩在弱酸性條件下具有還原性。一種制備氧釩
價釩在弱酸性條件下具有還原性。一種制備氧釩![]() 堿式碳酸銨方案如下:
堿式碳酸銨方案如下:
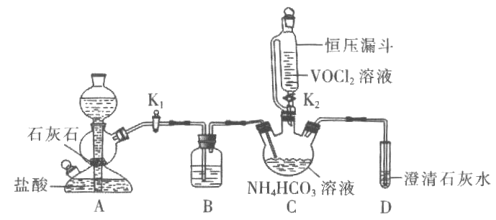
請回答下列問題:
(1)![]() 裝置盛裝的試劑是________
裝置盛裝的試劑是________![]() 填名稱
填名稱![]() 。A中反應的離子方程式為________。相對分液漏斗,恒壓漏斗優點是________。
。A中反應的離子方程式為________。相對分液漏斗,恒壓漏斗優點是________。
(2)實驗時,先關閉![]() ,打開
,打開![]() ,當________
,當________![]() 填實驗現象
填實驗現象![]() 時,后________
時,后________![]() 填實驗操作
填實驗操作![]() 。
。
(3)實驗完畢后,從C裝置中分離產品的操作方法是________![]() 填操作名稱
填操作名稱![]() 。
。
(4)測定粗產品中釩的含量。實驗步驟如下:
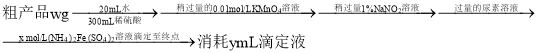
已知:滴定反應為![]()
![]() 該粗產品中釩的質量分數的表達式為________
該粗產品中釩的質量分數的表達式為________![]() 。
。
![]() 若滴定前仰視讀數,終點時俯視讀數,則測得結果________填“偏高”、“偏低”或“無影響”
若滴定前仰視讀數,終點時俯視讀數,則測得結果________填“偏高”、“偏低”或“無影響”![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式見圖,下列說法正確的是( )
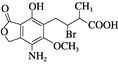
A. 分子式為C14H16O6NBr
B. 該分子中含有兩個手性碳原子
C. 不能使酸性高錳酸鉀溶液褪色
D. 在一定條件下與氫氧化鈉溶液反應,1 mol該有機物最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸是重要的化工材料,二氧化硫生成三氧化硫是工業制硫酸的重要反應之一。
(1)將0.050molSO2和0.030molO2放入容積為1L的密閉容器中,反應2SO2(g)+O2(g)![]() 2SO3(g)在一定條件下達到平衡,測得c(SO3)=0.040mol·L-1
2SO3(g)在一定條件下達到平衡,測得c(SO3)=0.040mol·L-1
①從平衡角度分析采用過量O2的目的是___。
②該條件下反應的平衡常數K=___。
③已知:K(300℃)>K(350℃),正反應是___(填“吸”或“放”)熱反應。若反應溫度升高,SO2的轉化率___(填“增大”“減小”或“不變”)。
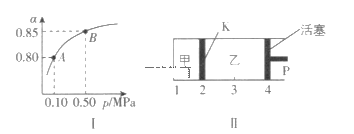
(2)某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如圖I所示。平衡狀態由A變到B時,平衡常數K(A)___K(B)(填“大于”“等于”或“小于”,下同)。
(3)如圖II所示,保持溫度不變,將2molSO2和1molO2加入甲容器中,將4molSO3加入乙容器中,隔板K不能移動。此時控制活塞P,使乙的容積為甲的2倍。
①若移動活塞P,使乙的容積和甲相等,達到新平衡時,SO3的體積分數甲___乙。
②若保持乙中壓強不變,向甲、乙容器中通人等質量的氦氣,達到新平衡時,SO3的體積分數甲___乙。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿式碳酸鎂![]() 是重要的無機化工產品。一種由白云石
是重要的無機化工產品。一種由白云石![]() 主要成分為
主要成分為![]() ,還含少量
,還含少量![]() 、
、![]() 等
等![]() 為原料制備堿式碳酸鎂
為原料制備堿式碳酸鎂![]() 國家標準中CaO的質量分數
國家標準中CaO的質量分數![]()
![]() 的實驗流程如下:
的實驗流程如下:

![]() “煅燒”時發生主要反應的化學方程式為________________。
“煅燒”時發生主要反應的化學方程式為________________。
![]() 常溫常壓下“碳化”可使鎂元素轉化為
常溫常壓下“碳化”可使鎂元素轉化為![]() ,“碳化”時終點pH對最終產品中CaO含量及堿式碳酸鎂產率的影響如圖1和圖2所示。
,“碳化”時終點pH對最終產品中CaO含量及堿式碳酸鎂產率的影響如圖1和圖2所示。
圖1 CaO含量與碳化終點pH的關系
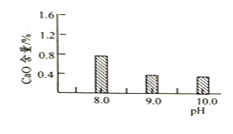
圖2堿式碳酸鎂產率與碳化終點pH的關系
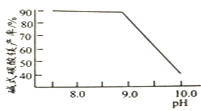
![]() 應控制“碳化”終點PH約為__________。
應控制“碳化”終點PH約為__________。
![]() 圖
圖![]() 中,當
中,當![]()
![]() 時,鎂元素的主要存在形式是__________________
時,鎂元素的主要存在形式是__________________![]() 寫化學式
寫化學式![]() 。
。
![]() “過濾”時須用到的玻璃儀器有:燒杯、玻璃棒、__________________。
“過濾”時須用到的玻璃儀器有:燒杯、玻璃棒、__________________。
![]() 一種測定堿式碳酸鎂img src="http://thumb.zyjl.cn/questionBank/Upload/2020/11/27/00/64e4569f/SYS202011270030549119707263_ST/SYS202011270030549119707263_ST.001.png" width="188" height="27" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />組成的方法如下:
一種測定堿式碳酸鎂img src="http://thumb.zyjl.cn/questionBank/Upload/2020/11/27/00/64e4569f/SYS202011270030549119707263_ST/SYS202011270030549119707263_ST.001.png" width="188" height="27" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />組成的方法如下:
![]() 稱取一定量的堿式碳酸鎂晶體溶于足量的鹽酸,收集到氣體
稱取一定量的堿式碳酸鎂晶體溶于足量的鹽酸,收集到氣體![]() 標準狀況
標準狀況![]() ;往所得溶液中加入足量的NaOH溶液,過濾,將所得沉淀洗滌、干燥,稱量得固體
;往所得溶液中加入足量的NaOH溶液,過濾,將所得沉淀洗滌、干燥,稱量得固體![]() 。
。
![]() 另取一定量的堿式碳酸鎂晶體在空氣中加熱,固體殘留率
另取一定量的堿式碳酸鎂晶體在空氣中加熱,固體殘留率![]() 固體樣品的剩余質量
固體樣品的剩余質量![]() 固體樣品的起始質量
固體樣品的起始質量![]() 隨溫度的變化如下圖所示
隨溫度的變化如下圖所示![]() 樣品在
樣品在![]() 時完全失去結晶水
時完全失去結晶水![]() 。
。
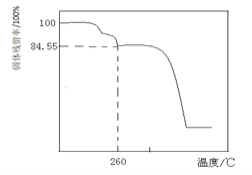
根據以上實驗數據計算確定堿式碳酸鎂晶體的化學式![]() 寫出計算過程
寫出計算過程![]() _________。
_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業從廢鉛酸蓄電池的渣泥(主要成分為PbSO4、PbO2)回收鉛。RSR 工藝的主要流程如下:
![]()
(1)鉛酸蓄電池放電時總反應為:
Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O(l)
正極反應:PbO2(s) + SO42-(aq) + 4H+(aq) + 2e- = PbSO4(s) + 2H2O(l)
負極反應:________。
(2)向渣泥中加入Na2CO3溶液將PbSO4轉化為更難溶的PbCO3。
①用化學平衡移動原理解釋其原因:________。
②工業上常用NaHCO3溶液代替Na2CO3溶液,將PbSO4轉化為PbCO3。PbSO4與NaHCO3溶液或Na2CO3溶液不同物質的量比時,PbSO4的轉化率見下表。
Ⅰ | n(PbSO4)∶ n(NaHCO3) | 1∶1.5 | 1∶2 | 1∶3 |
PbSO4轉化率/% | 95.5 | 96.9 | 97.8 | |
Ⅱ | n(PbSO4)∶ n(Na2CO3) | 1∶1.5 | 1∶2 | 1∶3 |
PbSO4轉化率/% | 98 | 98 | 98 |
依據上表數據,物質的量比相同時,Ⅱ中PbSO4的轉化率比Ⅰ中的略大,原因是________。
③上述反應除生成PbCO3外,還可能生成堿式碳酸鉛[2PbCO3·Pb(OH)2],二者受熱都易分解生成PbO。通過實驗確定產物中含有2PbCO3·Pb(OH)2,則該實驗操作及現象是________;通過定量實驗確定產物中2PbCO3·Pb(OH)2的含量,則需測定的數據是________。
(3)渣泥中加入Na2SO3溶液,利用其性質是________。
(4)H2SiF4溶液溶解PbCO3的化學方程式是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,在10mL0.1mol·L1 Na2CO3溶液中逐滴加入0.1mol·L1 HCl溶液,溶液的pH逐漸降低,此時溶液中含碳微粒的物質的量分數變化如圖所示,下列說法不正確的是
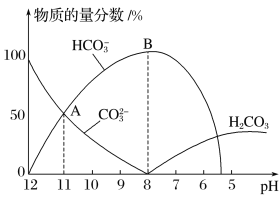
A.溶液的pH為7時,溶液的總體積大于20mL
B.在B點所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+c(Cl-)
C.在A點所示的溶液中:c(Na+)=c(CO32-)=c(HCO3-)>c(OH-)>c(H+)
D.已知CO32-水解常數為2×10-4,當溶液中c(HCO3-)=2c(CO32-)時,溶液的pH=10
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某二元酸H![]() B在水中的電離方程式是
B在水中的電離方程式是![]() 、HB
、HB![]() H
H![]() 。
。
![]() 的NaHB溶液顯酸性,原因是________________________________。
的NaHB溶液顯酸性,原因是________________________________。
![]() 在
在![]() 的Na2B溶液中,下列粒子濃度關系式正確的是________
的Na2B溶液中,下列粒子濃度關系式正確的是________![]() 填標號
填標號![]() 。
。
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗室廢液含![]() 、Na+、Fe3+、Cr3+、
、Na+、Fe3+、Cr3+、![]() 、
、![]() 等離子,現通過如下流程變廢為寶制備K2Cr2O7。
等離子,現通過如下流程變廢為寶制備K2Cr2O7。
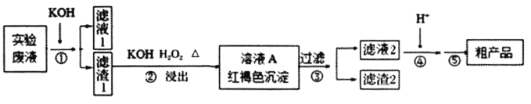
已知:
(a)![]() ;
;![]()
(b)金屬離子形成氫氧化物沉淀的pH范圍如表。
金屬離子 | pH | |
開始沉淀 | 完全沉淀 | |
Fe3+ | 2.7 | 3.7 |
Cr3+ | 4.9 | 6.8 |
請回答:
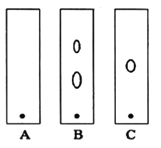
(1)某同學采用紙層析法判斷步驟①加入KOH的量是否合適。在加入一定量KOH溶液后,用毛細管取樣、點樣、薄層色譜展開、氨熏后的斑點如圖所示。加入KOH最適合的實驗編號是(實驗順序已打亂)________,C的斑點顏色為________。
(2)步驟②含Cr物質發生的主要反應的離子方程式為________________________。
(3)在下列裝置中,②應選用________。(填標號)
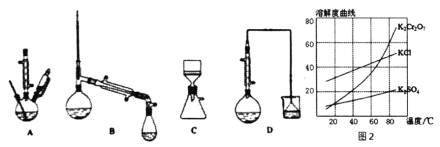
(4)部分物質的溶解度曲線如圖2,步驟⑤可能用到下列部分操作:a.蒸發至出現大量晶體,停止加熱;b.冷卻至室溫;c,蒸發至溶液出現晶膜,停止加熱;d.洗滌;e.趁熱過濾;f.抽濾。請選擇合適操作的正確順序________。
(5)步驟⑤中合適的洗滌劑是________(“無水乙醇”、“乙醇-水混合液”、“熱水”、“冰水”)。
(6)取mg粗產品配成250mL溶液,取25.00mL于錐形瓶中,用cmol·L-1的(NH4)2Fe(SO4)2標準溶液滴定(雜質不反應),消耗標準(NH4)2Fe(SO4)2溶液VmL,則該粗產品中K2Cr2O7的純度為________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com