
 .若有標準狀況下V L氨氣完全反應,并轉移n個電子,則阿伏加德羅常數(NA)可表示為$\frac{22.4n}{5V}$(寫出含字母的表達式).
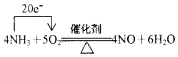
.若有標準狀況下V L氨氣完全反應,并轉移n個電子,則阿伏加德羅常數(NA)可表示為$\frac{22.4n}{5V}$(寫出含字母的表達式). 分析 反應4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O中,N元素化合價由-3價升高到+2價,則NH3為還原劑,O元素化合價由0價降低到-2價,則O2為氧化劑,轉移電子數為20e-,據此分析解答.
解答 解:(反應4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O中,N元素化合價由-3價升高到+2價,則NH3為還原劑,O元素化合價由0價降低到-2價,則O2為氧化劑,轉移電子數為20e-,用單線橋法表示該氧化還原反應電子轉移的方向和數目為: ;若有標準狀況下V L氨氣完全反應,并轉移n個電子,則$\frac{n}{N{\;}_{A}}$=$\frac{V}{22.4}$×5,所以阿伏加德羅常數(NA)可表示為:$\frac{22.4n}{5V}$,
;若有標準狀況下V L氨氣完全反應,并轉移n個電子,則$\frac{n}{N{\;}_{A}}$=$\frac{V}{22.4}$×5,所以阿伏加德羅常數(NA)可表示為:$\frac{22.4n}{5V}$,
故答案為:O2;NH3; ;$\frac{22.4n}{5V}$.
;$\frac{22.4n}{5V}$.
點評 本題考查氧化還原反應的基本概念,側重于學生的分析能力的考查,為高考常見題型,把握反應中元素的化合價變化為解答的關鍵,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | Na在空氣中燃燒,發出黃色火焰 | B. | Na在空氣中燃燒,產物是Na2O | ||
| C. | Na是銀白色金屬,硬度小,熔點低 | D. | Na、K合金可作原子反應堆的導熱劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
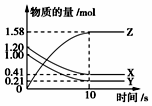 一定溫度下,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示,下列描述正確的是( )
一定溫度下,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示,下列描述正確的是( )| A. | 反應開始到10 s,用Z表示的反應速率為0.079mol•(L•s)-1 | |
| B. | 反應開始到10 s,X的物質的量濃度減少了0.79mol•L-1 | |
| C. | 該反應不是可逆反應 | |
| D. | 反應的化學方程式為X(g)+Y(g)?Z(g) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 保持容器容積不變,向其中加入1 mol N2(N2不參加反應),反應速率加快 | |
| B. | 提高起始的反應溫度,正反應速率加快,逆反應速率減慢,平衡正向移動 | |
| C. | 保持容器內氣體壓強不變,向其中加入1 mol Ne,反應速率加快,平衡正向移動 | |
| D. | 保持容器內氣體壓強不變,向其中加入1 mol H2(g)和1 mol I2(g),反應速率不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 目 的 | 分離方法 | 原 理 |
| A | 分離溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度較大 |
| B | 分離乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 除去乙烷中混有的乙烯 | 酸性高錳酸鉀溶液洗氣 | 乙烯與酸性高錳酸鉀溶液反應而乙烷不能 |
| D | 除去乙酸乙酯中混有的乙酸 | 用飽和碳酸鈉溶液洗滌后分液 | 乙酸能與碳酸鈉反應生成溶于水的鹽 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
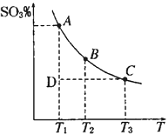 硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g)?2SO3(g),混合體系中SO3的百分含量和溫度的關系如圖所示(曲線上任何一點都表示平衡狀態).根據圖示回答下列問題:
硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g)?2SO3(g),混合體系中SO3的百分含量和溫度的關系如圖所示(曲線上任何一點都表示平衡狀態).根據圖示回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
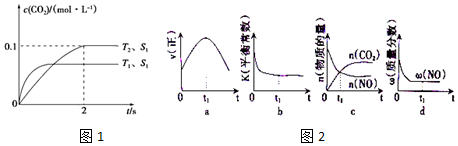
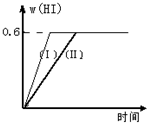 Ⅱ將1mol I2(g)和2mol H2置于2L密閉容器中,在一定溫度下發生反應:I2(g)+H2(g)?2HI(g);△H<0,并達平衡.HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示:
Ⅱ將1mol I2(g)和2mol H2置于2L密閉容器中,在一定溫度下發生反應:I2(g)+H2(g)?2HI(g);△H<0,并達平衡.HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com