
工業上為了處理含有Cr2O72-的酸性工業廢水,采用下列的處理方法: 是綠礬(FeSO4·7H2O),把廢水中的六價鉻離子還原成三價鉻離子,再加入過量的石灰水,使鉻離子轉變為Cr(OH)3沉淀。其主要的化學方程式如下:
H2Cr2O7+6FeSO4+6 H2SO4=Cr2(SO4)3+3Fe 2(SO4)3+7H2O
現用上述方法處理1×104L含鉻(+6價)78mg/L的廢水(Cr相對原子質量為52),請回答下列問題:
⑴處理后,沉淀物中除Cr(OH)3外,還有 . (用化學式表示)。
⑵需用綠礬的質量 。
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
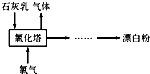 氯氣是重要的化工原料.
氯氣是重要的化工原料.| C(H+)C(Cl-)C(HClO) |
| C(Cl2) |
| C(H+)C(Cl-)C(HClO) |
| C(Cl2) |
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
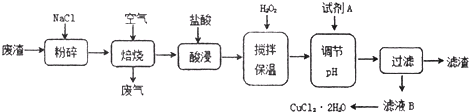
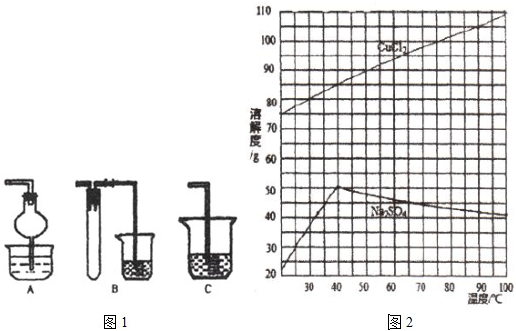
| 氫氧化物開始沉淀時的pH | 氫氧化物沉淀完全時的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化學 來源:2013屆黑龍江省哈三中高三10月月考化學試卷(帶解析) 題型:填空題
(14分) (1) 2009年,長春應用化學研究所在甲醇燃料電池技術上獲得新突破,原理如下圖所示。
①請寫出從C口通入O2發生的電極反應式___________________。
②以石墨電極電解飽和食鹽水,電解開始后在______________的周圍(填“陰極”或“陽極”)先出現紅色。假設電池的理論效率為80%(電池的理論效率是指電池產生的最大電能與電池反應所釋放的全部能量之比),若消耗6.4g甲醇氣體,外電路通過的電子個數為__________________(保留兩位有效數字)。
(2)工業廢水中常含有Cu2+等重金屬離子,直接排放會造成污染,目前在工業廢水處理過程中,依據沉淀轉化的原理,常用FeS等難溶物質作為沉淀劑除去這些離子。已知室溫下Ksp(FeS)=6.3×10-18mol2?L-2,Ksp(CuS)=1.3×10-36mol2?L-2。
請用離子方程式說明上述除雜的原理___________________________________________。
(3)工業上為了處理含有Cr2O72-的酸性工業廢水,用綠礬(FeSO4·7H2O)把廢水中的六價鉻離子還原成三價鉻離子,再加入過量的石灰水,使鉻離子轉變為Cr(OH)3沉淀。
①氧化還原過程的離子方程式為______________________________________________。
②常溫下,Cr(OH)3的溶度積Ksp =1×10—32 mol4?L-4,溶液的pH至少為____,才能使Cr3+沉淀完全。
③現用上述方法處理100m3含鉻(+6價)78mg?L—1的廢水,需用綠礬的質量為 kg。(保留主要計算過程)
查看答案和解析>>
科目:高中化學 來源:2012-2013學年湖北省襄陽市高三調研三月統一測試理綜化學試卷(解析版) 題型:填空題
(14分) 電池的發明和應用是化學家們對人類社會的重要貢獻之一。
Ⅰ.每一次化學電池技術的突破,都帶來了電子設備革命性的發展。最近,我國在甲醇燃料電池的相關技術上獲得了新突破,原理如下圖1所示。
(1)請寫出從C口通入O2發生的電極反應式 。
(2)以石墨做電極電解飽和食鹽水,如下圖2所示。電解開始后在 的周圍(填“陰極”或“陽極”)先出現紅色。假設電池的理論效率為80%(電池的理論效率是指電池產生的最大電能與電池反應所釋放的全部能量之比),若消耗6.4g甲醇氣體,外電路通過的電子個數為 (保留兩位有效數字,NA取6.02×1023)。

Ⅱ.隨著電池使用范圍的日益擴大,廢舊電池潛在的污染已引起社會各界的廣泛關注。
(1)電池生產企業排放的工業廢水中常含有Cu2+等重金屬離子,直接排放會造成污染,目前在工業廢水處理過程中,依據沉淀轉化的原理,常用FeS等難溶物質作為沉淀劑除去這些離子。已知室溫下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。請用離子方程式說明上述除雜的原理 。
(2)工業上為了處理含有Cr2O72-的酸性工業廢水,用綠礬(FeSO4·7H2O)把廢水中的六價鉻離子還原成三價鉻離子,再加入過量的石灰水,使鉻離子轉變為Cr(OH)3沉淀。
①氧化還原過程的離子方程式為 。
②常溫下,Cr(OH)3的溶度積Ksp=1×10-32 mol4·L-4,溶液的pH至少為 ,才能使Cr3+沉淀完全。
③現用上述方法處理100m3含鉻(+6價)78mg•L-1的廢水,需用綠礬的質量為 kg。(寫出主要計算過程)
查看答案和解析>>
科目:高中化學 來源:2012-2013學年黑龍江省高三10月月考化學試卷(解析版) 題型:填空題
(14分) (1) 2009年,長春應用化學研究所在甲醇燃料電池技術上獲得新突破,原理如下圖所示。
①請寫出從C口通入O2發生的電極反應式___________________。
②以石墨電極電解飽和食鹽水,電解開始后在______________的周圍(填“陰極”或“陽極”)先出現紅色。假設電池的理論效率為80%(電池的理論效率是指電池產生的最大電能與電池反應所釋放的全部能量之比),若消耗6.4g甲醇氣體,外電路通過的電子個數為__________________(保留兩位有效數字)。

(2)工業廢水中常含有Cu2+等重金屬離子,直接排放會造成污染,目前在工業廢水處理過程中,依據沉淀轉化的原理,常用FeS等難溶物質作為沉淀劑除去這些離子。已知室溫下Ksp(FeS)=6.3×10-18mol2•L-2,Ksp(CuS)=1.3×10-36mol2•L-2。
請用離子方程式說明上述除雜的原理___________________________________________。
(3)工業上為了處理含有Cr2O72-的酸性工業廢水, 用綠礬(FeSO4·7H2O)把廢水中的六價鉻離子還原成三價鉻離子,再加入過量的石灰水,使鉻離子轉變為Cr(OH)3沉淀。
①氧化還原過程的離子方程式為______________________________________________。
②常溫下,Cr(OH)3的溶度積Ksp =1×10—32 mol4•L-4,溶液的pH至少為____,才能使Cr3+沉淀完全。
③現用上述方法處理100m3含鉻(+6價)78mg•L—1的廢水,需用綠礬的質量為 kg。(保留主要計算過程)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com