
【題目】在一定溫度下的密閉容器中,可逆反應N2 + 3H2![]() 2NH3 達到平衡狀態的標志是
2NH3 達到平衡狀態的標志是
A. N2、H2、NH3在容器中共存
B. 混合氣體的總物質的量不再發生變化
C. 單位時間內生成n mol N2,同時生成3n mol H2
D. 單位時間內消耗n mol N2,同時消耗n mol NH3
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】已知A與![]() 、CO形成B,B能發生銀鏡反應,C分子中只有一種氫,相關物質轉化關系如下
、CO形成B,B能發生銀鏡反應,C分子中只有一種氫,相關物質轉化關系如下![]() 含有相同官能團的有機物通常具有相似的化學性質
含有相同官能團的有機物通常具有相似的化學性質![]() :
:
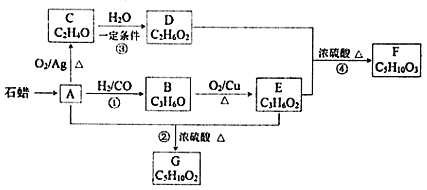
請回答:
![]() 有機物C的結構簡式是______,反應②的反應類型是______。
有機物C的結構簡式是______,反應②的反應類型是______。
![]() 寫出一定條件下發生反應①的化學方程式______。
寫出一定條件下發生反應①的化學方程式______。
![]() 下列說法不正確的是______
下列說法不正確的是______![]() 填字母
填字母![]() 。
。
A.化合物A屬于烴
B.化合物D含有兩種官能團
C.用金屬鈉無法鑒別化合物F、G
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知草酸(H2C2O4)是一種二元弱酸,草酸及其鹽廣泛用于醫藥、印染、塑料等工業。
(1)已知25℃時,幾種常見弱酸的Ka如下表所示:
電解質 | H2C2O4 | CH3COOH | HCN | H2CO3 |
電離常數(mol·L-1) | K1=5.6×10-2 K2=5.4×10-3 | K1=1.7×10-5 | K2=6.2×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
①25℃時,濃度均為0.1mol·L-1的Na2C2O4、CH3COONa、NaCN、Na2CO3的pH由大到小的順序是___。中和等體積、等pH的HCOOH和HCN消耗NaOH的量___(填“前者大”“后者大”或“相等”)。
②下列關于0.1mol·L-1NaHC2O4溶液的說法正確的是___。
a.HC2O4-的電離程度大于水解程度,溶液顯酸性
b.HC2O4-的水解程度大于電離程度程度,溶液顯堿性
c.溶液中c(Na+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
d.溶液中c(H+)=c(OH-)+c(C2O42-)-c(H2C2O4)
(2)在t℃時,MgC2O4在水中的沉淀溶解平衡曲線如圖1所示。又知t℃時Mg(OH)2的Ksp=5.6×10-12,下列說法不正確的是____
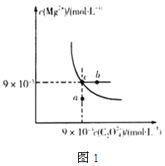
A.在t℃時,MgC2O4的Ksp=8.1×10-5mol2·L-2
B.在MgC2O4飽和溶液中加入Na2CO3固體,可使溶液由c點到b點
C.圖中a點對應的是MgC2O4的不飽和溶液
D.在t℃時,MgC2O4(s)+2OH-(aq)Mg(OH)2(s)+C2O42-(aq)平衡常數K=![]()
(3)草酸亞鐵晶體(FeC2O4·2H2O)是一種淺黃色固體,難溶于水,受熱易分解。某化學興趣小組設計實驗驗證草酸亞鐵晶體熱分解的產物,探究過程如圖2:
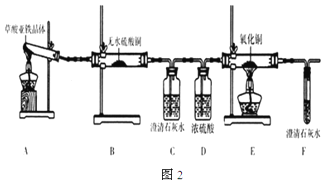
①從環保角度考慮,該套實驗裝置的明顯缺陷是___。
②該興趣小組進行上述實驗時,從實驗安全角度考慮,應先點燃___(填“A”或“E”)處的酒精燈。
③若實驗過程中觀察到B中白色無水CuSO4變成藍色,___(補充實驗現象),則可證明草酸亞鐵晶體熱分解的氣體產物是H2O、CO和
④為探究草酸亞鐵晶體分解的固體產物,興趣小組同學準確稱取3.60g草酸亞鐵晶體(FeC2O4·2H2O),相對分子質量是180),充分加熱,使其完全分解,冷卻后稱得剩余固體的質量為1.60g。若剩余固體只有一種鐵的氧化物,通過計算確定該氧化物的化學式為___。草酸亞鐵晶體分解的化學方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用下列裝置制備Cl2并檢驗其性質,下列說法正確的是( )
A.I圖中:如果MnO2過量,濃鹽酸就可全部消耗完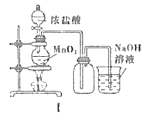
B.II圖中:用排飽和食鹽水收集一試管氯氣,充分光照后,水槽中溶液酸性增強,量筒中液面上升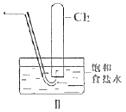
C.III圖中:生成藍色的煙,若向集氣瓶中加入少量水,所得溶液呈黃色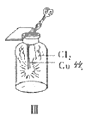
D.IV圖中:干燥的有色布條不褪色,濕潤的有色布條能褪色,說明Cl2有漂白性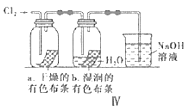
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器中的一定量混合氣體發生反應:xA(g)+yB(g)![]() zC(g),平衡時測得A的濃度為0.50mol/L,保持溫度不變,將容器的容積擴大到原來的兩倍,再達到平衡時,測得A的濃度降低為0.30mol/L.下列有關判斷正確的是
zC(g),平衡時測得A的濃度為0.50mol/L,保持溫度不變,將容器的容積擴大到原來的兩倍,再達到平衡時,測得A的濃度降低為0.30mol/L.下列有關判斷正確的是
A. C的體積分數增大了 B. A的轉化率降低了
C. 平衡向正反應方向移動 D. x+y<z
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒壓、NO和O2的起始濃度一定的條件下,催化反應相同時間,測得不同溫度下NO轉化為NO2的轉化率如圖中實線所示(圖中虛線表示相同條件下NO的平衡轉化率隨溫度的變化)。下列說法正確的是

A. 反應2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B. 圖中X點所示條件下,延長反應時間能提高NO轉化率
C. 圖中Y點所示條件下,增加O2的濃度不能提高NO轉化率
D. 380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡轉化率為50%,則平衡常數K>2000
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究大氣污染物的處理,對緩解和治理環境污染、保護我們賴以生存的地球,具有十分重要的意義。
(1)已知:C(s)+O2(g)═CO2(g)△H=﹣393.5/kJmol
N2(g)+O2(g)═2NO(g)△H=+180kJ/mol
則C(s)+2NO(g)═CO2(g)+N2(g) 的△H=_____kJ/mol。
(2)在一定溫度下,向2L的恒容密閉容器中充入4.0 mol NO2和4.0 mol CO,在催化劑作用下發生反應4CO(g)+2NO2(g)4CO2(g)+N2(g),測得相關數據如表所示:
t/min | 0 | 5 | 10 | 15 | 20 |
n(NO2)/mol | 4.0 | 3.4 | 3.12 | 3.0 | 3.0 |
n(N2)/mol | 0 | 0.30 | 0.44 | 0.50 | 0.50 |
①在0~5 min內,用CO2的濃度變化表示的反應速率為_____。
②此溫度下的化學平衡常數K的表達式為_____。
(3)用活性炭還原法處理氮氧化物,有關反應為C(s)+2NO(g)![]() CO2(g)+N2(g)。某研究小組向2L密閉容器中加入足量的活性炭和一定量的NO,保持溫度和體積不變,發生上述反應。
CO2(g)+N2(g)。某研究小組向2L密閉容器中加入足量的活性炭和一定量的NO,保持溫度和體積不變,發生上述反應。
①下列描述能說明上述反應已達平衡的是_____(填標號)。
A.活性炭的質量不再變化
B.容器中氣體的密度保持不變
C.2v(NO)正 =v(N2)逆
D. 保持不變
保持不變
②壓強為p時,催化劑的催化效率、氮氣的生成速率與溫度的關系如圖所示。當氮氣的生成速率主要取決于溫度時,對應的溫度范圍是_____。
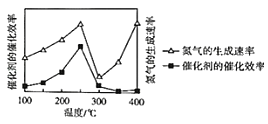
(4)肼(N2H4)是無色液體,具有強還原性。
①肼的水溶液顯弱堿性,其電離過程與NH3H2O類似,則第一步電離方程式為_____。
②新型N2H4燃料電池產物對環境沒有污染,該電池以固體氧化物為電解質(能傳導O2﹣)。寫出負極的電極反應式_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是以苯酚為主要原料制取冬青油和阿司匹林的過程:
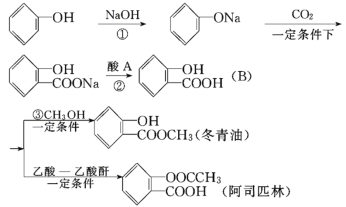
(1) 冬青油含有的官能團名稱為________________
(2)B溶于冬青油致使產品不純,加入下列哪種試劑后再分液即可除去_____
(A) NaOH 溶液 (B) Na2CO3溶液 (C) NaHCO3溶液 (D) Na
(3)寫出第①步反應的化學方程式_________________________________.
(4)寫出反應③的化學方程式_____________________________________
(5)1 mol 阿司匹林最多可與________ mol 氫氧化鈉發生反應.
(6)化合物M是冬青油的同分異構體,與冬青油具有相同的官能團,能與氯化鐵發生顯色反應,苯環上有兩個對位的取代基,寫出兩種M可能的結構簡式____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉍及其化合物在冶金、醫療、化工生產中均有重要作用。鉍在自然界中的含量極少,常以游離金屬和礦物的形式存在。對浮選過的輝鉍礦(主要成分是Bi2S3,還含少量Bi2O3、SiO2、Cu2S、FeS2等雜質)通過浸出、凈化和電沉積法分離回收鉍的流程:
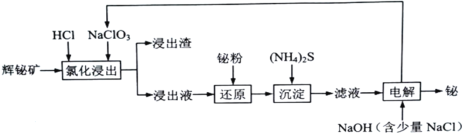
已知:I.“氯化浸出”過程中,需分批多次加入NaClO3,以防生成Cl2;
II.BiCl3極易水解生成不溶性的BiOCl沉淀,但在濃鹽酸中幾乎不水解;
III.氧化性:Fe3+>Cu2+>Bi3+>H+.
請回答以下問題:
(1)“氯化浸出”時,為了提高浸取速率,可采取的措施有________________(任寫一條);加入過量鹽酸的主要目的是______________________.
(2)浸出渣中含有S和____________(寫化學式);
(3)寫出“氯化浸出”中Bi2S3所發生反應的離子方程式__________________________.
(4)“還原”過程中所發生反應的離子方程式為2Bi+3Cu2+=2Bi3++3Cu及____________。
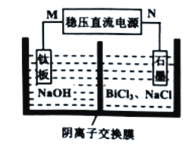
(5)“電解”過程的簡易裝置如圖所示。裝置中N為電源的________(填“正”或“負”)極;陽極上發生的主要電極反應式為__________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com