
【題目】(1)氨氣可作為脫硝劑,在恒溫恒容密閉容器中充入一定量的NO和NH3,在一定條件下發生反應:6NO(g)+4NH3(g)![]() 5N2(g)+6H2O(g)。
5N2(g)+6H2O(g)。
①能說明該反應已達到平衡狀態的標志是___。
a.反應速率v(NH3)=v(N2)
b.容器內壓強不再隨時間而發生變化
c.容器內N2的物質的量分數不再隨時間而發生變化
d.容器內n(NO)∶n(NH3)∶n(N2)∶n(H2O)=6∶4∶5∶6
e.12mol N-H鍵斷裂的同時生成5mol N≡N鍵
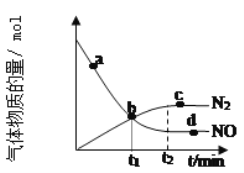
②某次實驗中測得容器內NO及N2的物質的量隨時間變化如圖所示,圖中b點對應的速率關系是v(正)___v(逆);d點對應的速率關系是v(正)___v(逆)。(填﹥、﹤或﹦)。
(2)一定條件下,在2L密閉容器內,反應2NO2(g)![]() N2O4(g),n(NO2)隨時間變化如下表:
N2O4(g),n(NO2)隨時間變化如下表:
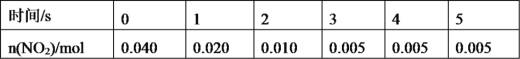
①用N2O4表示0~2s內該反應的平均速率為___。在第5s時,NO2的轉化率為___。
②根據上表可以看出,隨著反應進行,反應速率逐漸減小,其原因是__。
【答案】bc > = 0.00375mol·L-1·s-1(或0.225mol·L-1·min-1) 87.5% 隨著反應的進行,反應物NO2的物質的量濃度減小,因而反應速率減小
【解析】
(1)①a.該反應達到平衡狀態時,5v正(NH3)=4v逆(N2),故a錯誤;
b.該反應是一個反應前后氣體體積增大的可逆反應,容器體積恒定,所以未平衡時壓強會發生改變,當壓強不再變化時說明反應平衡,故b正確;
c.容器內N2的物質的量分數不再隨時間而發生變化說明濃度不在改變,反應達到平衡,故c正確;
d.物質的量之比不能說明正逆反應速率相等或者濃度不變,故d錯誤;
e.只要反應進行12mol N-H 鍵斷裂的同時就會生成5mol N≡N鍵,二者均表示正反應速率,故e錯誤;
故答案為:bc;
②據圖可知b點之后氮氣的濃度增大,NO的濃度減小,說明此時反應正向進行,及v(正)> v(逆);d點時NO的濃度不再變化,說明反應達到平衡,所以v(正)= v(逆);
(2)①0~2s內v(NO2)= =0.0075mol·L-1·s-1,同一反應同一時段內不同物質的反應速率之比等于計量數之比,所以v(N2O4)=0.5v(NO2)=0.00375mol·L-1·s-1;第5s時,二氧化氮的轉化率為
=0.0075mol·L-1·s-1,同一反應同一時段內不同物質的反應速率之比等于計量數之比,所以v(N2O4)=0.5v(NO2)=0.00375mol·L-1·s-1;第5s時,二氧化氮的轉化率為![]() =87.5%;
=87.5%;
②隨著反應的進行,反應物NO2的物質的量濃度減小,因而反應速率減小。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】硫的含量影響鋼鐵性能。一種測定硫含量的方法是將鋼樣中硫轉化為二氧化硫氣體,再用測硫裝置進行測定。某測定硫含量的流程如下:
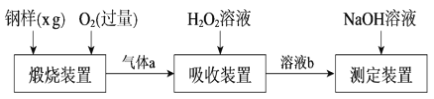
(1)氣體a的主要成分有CO2、______、______。
(2)若鋼樣中硫以FeS的形式存在,煅燒裝置中發生的化學反應為3FeS+5O2 ![]() 1______ +3______。___________
1______ +3______。___________
(3)吸收裝置中,H2O2氧化SO2的化學方程式是_________________。
(4)用NaOH溶液中和生成的溶液b,消耗z mLNaOH溶液,若消耗1 mLNaOH溶液相當于硫的質量為y g,則該鋼樣中硫的質量分數為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中學化學中幾種常見物質的轉化關系如下圖(部分產物未列出),A是一種金屬單質,D是一種非金屬固體單質。
請回答下列問題:

(1)A、C的化學式分別為A_________,C_________;
(2)F的濃溶液與A反應過程中,F體現的性質與下列反應中H2SO4體現的性質完全相同的是_____;
A.C+2H2SO4(濃)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
B.Fe+H2SO4═FeSO4+H2↑
C.Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.FeO+H2SO4═FeSO4+H2O
(3)寫出反應E+H2O2→F的化學方程式:____________;
(4)若反應F+D→E轉移電子數為6.02×1023,則消耗D的質量為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,向10mL 0.1mol·L-1 CuCl2溶液中滴加0.1mol·L-1的Na2S溶液,滴加過程中-lg c(Cu2+)與Na2S溶液體積的關系如圖所示。已知:Ksp(ZnS)=3×10-25,下列有關說法正確的是
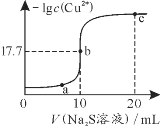
A.Na2S溶液中:c(H+)+c(HS-)+c(H2S)=c(OH-)
B.a、b、c三點對應的溶液中,水的電離程度最小的為b點
C.c點溶液中c(Cu2+)=10-34.4 mol·L-1
D.向100mL Zn2+、Cu2+物質的量濃度均為0.1mol·L-1的混合溶液中逐滴加入10-3 mol·L-1的Na2S溶液,Zn2+先沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯胺![]() 是重要的化工原料。某興趣小組在實驗室里進行苯胺的相關實驗。
是重要的化工原料。某興趣小組在實驗室里進行苯胺的相關實驗。
已知:①![]() 和NH3相似,與鹽酸反應生成易溶于水的鹽
和NH3相似,與鹽酸反應生成易溶于水的鹽![]()
②用硝基苯制取苯胺的反應原理: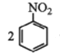 +3Sn+12HCl
+3Sn+12HCl![]()
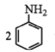 +3SnCl4+4H2O
+3SnCl4+4H2O
③有關物質的部分物理性質見下表:
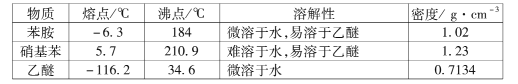
I.比較苯胺與氨氣的性質
(1)將分別蘸有濃氨水和濃鹽酸的玻璃棒靠近,產生白煙,反應的化學方程式為____;用苯胺代替濃氨水重復上述實驗,卻觀察不到白煙,原因是____。
Ⅱ.制備苯胺
往圖1所示裝置(夾持裝置略,下同)的冷凝管口分批加入20mL濃鹽酸(過量),置于熱水浴中回流20min,使硝基苯充分還原;冷卻后,往三頸燒瓶中滴入一定量50% NaOH溶液,至溶液呈堿性。
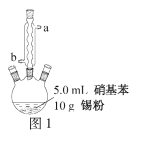
(2)冷凝管的進水口是____(填“a”或“b”);
(3)滴加NaOH溶液的主要目的是析出苯胺,反應的離子方程式為____。
Ⅲ.提取苯胺
i.取出圖1所示裝置中的三頸燒瓶,改裝為圖2所示裝置。加熱裝置A產生水蒸氣,燒瓶C中收集到苯胺與水的混合物;分離混合物得到粗苯胺和水溶液。
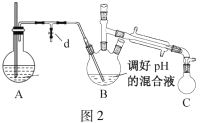
ii.往所得水溶液中加入氯化鈉固體,使溶液達到飽和狀態,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固體干燥,蒸餾后得到苯胺2.79g。
(4)裝置B無需用到溫度計,理由是____。
(5)操作i中,為了分離混合物,取出燒瓶C前,應先打開止水夾d,再停止加熱,理由是____。
(6)該實驗中苯胺的產率為____。
(7)欲在不加熱條件下除去苯胺中的少量硝基苯雜質,簡述實驗方案:____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】前四周期元素X、Y、Z、M、N、O、P,原子序數逐漸增大,其中X、Y、Z、M、N為短周期元素,而X、Y、Z、M處于同周期的P區,且未成對電子數之比為1:2:3:2;N與Z同族。O、P分別位于周期表第2、4列,P的單質被稱為“未來金屬”,具有質量輕、強度大、耐腐蝕性好的優點。
(1)Y、Z、M三種元素的電負性由大到小的順序:________(用元素符號表示)。
(2)M的常見氫化物的氫鍵的鍵能小于HF的氫鍵的鍵能,但Z的常見氫化物常溫下為液態而HF常溫下為氣態的原因是:__________。
(3)XN一種耐磨涂料,可用于金屬表面保護層,該化合物可由X的三溴化物和N的三溴化物于高溫下在氫氣的氛圍中合成。
①寫出合成XN的化學方程式:_________。(各物質用化學式表示)
②XN的晶體的晶胞如圖所示:
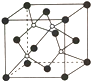
其中實心球為N,在一個晶胞中N原子空間堆積方式為______,N原子的配位數為______;該結構中有一個配位鍵,提供空軌道的原子是________(寫元素符號)。
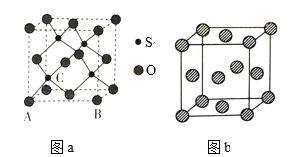
(4)O和硫形成的某種晶體的晶胞如圖a所示:該晶胞原子的坐標參數A為(0,0,0);B為(1,0,0)。則C原子的坐標參數為_______。
(5)圖b為P的一種面心立方晶胞結構,若晶胞的邊長為anm,則P的密度為_____g·cm-3(用含a和NA的代數式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅和鎂的合金4.6 g完全溶于濃硝酸,若反應中硝酸被還原只產生4 480 mL NO2氣體和336 mL的N2O4氣體(氣體的體積已折算到標準狀況),在反應后的溶液中,加入足量的氫氧化鈉溶液,生成沉淀的質量為 ( )
A.9.02 gB.8.51 gC.8.26 gD.7.04 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是部分短周期元素的原子序數與其某種常見化合價的關系圖,若用原子序數代表所對應的元素,則下列說法正確的是

A.31d和33d屬于同種核素
B.氣態氫化物的穩定性:a>d>e
C.工業上常用電解法制備單質b
D.a和b形成的化合物不可能含共價鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煤炭燃燒時產生大量SO2、NO對環境影響極大。
(1)使用清潔能源可有效減少SO2等的排放。煤的液化是現代能源工業中重點推廣的能源綜合利用方案,最常見的液化方法為用煤生產CH3OH。已知制備甲醇的有關化學反應及平衡常數如下:
i:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1=-a kJ/mol
CH3OH(g)+H2O(g) ΔH1=-a kJ/mol
ii:CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH2=+b kJ/mol
CO(g)+H2O(g) ΔH2=+b kJ/mol
iii:CO(g)+2H2(g) ![]() CH3OH(g) ΔH3
CH3OH(g) ΔH3
ΔH3=________。
(2)在密閉容器中進行反應i,改變溫度時,該反應中的所有物質都為氣態,起始溫度、體積相同(T1 ℃、2 L密閉容器)。反應過程中部分數據見下表:
反應時間 | CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
反應Ⅰ恒 溫恒容 | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
反應Ⅱ絕 熱恒容 | 0 min | 0 | 0 | 2 | 2 |
①達到平衡后,反應Ⅰ、Ⅱ對比:平衡常數K(Ⅰ)________K(Ⅱ)(填“>”“<”或“=”下同);平衡時CO2的濃度c(Ⅰ)________c(Ⅱ)。
②對反應Ⅰ,在其他條件不變下,若30 min時只改變溫度為T2 ℃,再次平衡時H2的物質的量為2.5 mol,則T1________T2(填“>”“<”或“=”)。
③若30 min時只向容器中再充入1 mol H2(g)和1 mol H2O(g),則平衡________移動(填“正向”“逆向”或“不”)。
(3)研究人員發現,將煤炭在O2/CO2的氣氛下燃燒,能夠降低燃煤時NO的排放,主要反應為:2NO(g)+2CO(g)=N2(g)+2CO2(g)。在一定溫度下,于2 L的恒容密閉容器中充入0.1 mol NO和0.3 mol CO發生該反應,如圖為容器內的壓強(p)與起始壓強(p0)的比值(p/p0)隨時間的變化曲線。
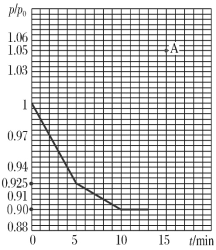
①0~5 min內,該反應的平均反應速率v(NO)=________;平衡時N2的產率為________。
②若13 min時,向該容器中再充入0.06 mol CO2,15 min時再次達到平衡,此時容器內![]() /
/![]() 的比值應在圖中A點的________(填“上方”或“下方”)。
的比值應在圖中A點的________(填“上方”或“下方”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com