

| A. | ⑤③① | B. | ②③④ | C. | ③⑤④ | D. | ③②① |
分析 等物質的量濃度、等體積的MgCl2、BeCl2、AlCl3溶液,即三者的物質的量是相等的,將一定濃度的NaOH溶液,分別滴入三種溶液中至過量,所發生的反應過程如下:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;BeCl2+2NaOH=Be(OH)2↓+2NaCl,Be(OH)2↓+2NaOH=Na2BeO2+2H2O;AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3↓+NaOH=NaAlO2+2H2O,根據溶液物質的量和化學方程式來確定沉淀的量.
解答 解:向氯化鎂中加入氫氧化鈉,開始先中和其中的少量鹽酸,然后生成白色沉淀氫氧化鎂,當氫氧化鈉過量時,沉淀也不會溶解,量保持不變,故對應的是圖象③;
向氯化鈹溶液中加入氫氧化鈉,開始先中和其中的少量鹽酸,然后生成白色沉淀氫氧化鋅,當氫氧化鈉過量時,沉淀會溶解,依次發生反應BeCl2+2NaOH=Be(OH)2↓+2NaCl,Be(OH)2↓+2NaOH=Na2BeO2+2H2O,沉淀量達到最大和沉淀完全消失所消耗的氫氧化鈉是相等的,故圖象⑤是正確的,
向氯化鋁溶液中加入氫氧化鈉,開始先中和其中的少量鹽酸,然后生成白色沉淀氫氧化鋁,當氫氧化鈉過量時,沉淀會溶解,依次發生反應:
AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3↓+NaOH=NaAlO2+2H2O,沉淀量達到最大和沉淀完全消失所消耗的氫氧化鈉的物質的量之比是3:1,故圖象①是正確的.則與BeCl2、MgCl2、AlCl3三種溶液對應的圖象正確的是⑤③①;故A正確;
故選A.
點評 本題考查了金屬鎂、金屬鋁以及金屬鈹的可溶性鹽溶液和強堿氫氧化鈉之間的反應,屬于化學反應知識的考查題,注意方程式的靈活應用是解題關鍵,題目難度中等,側重于考查學生的分析能力和計算能力.


科目:高中化學 來源: 題型:選擇題
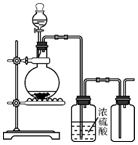
| A. | 銅和稀硝酸制一氧化氮 | B. | 亞硫酸鈉與硫酸制二氧化硫 | ||
| C. | 鋅和稀硫酸制氫氣 | D. | 硫化亞鐵與稀硫酸制硫化氫 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
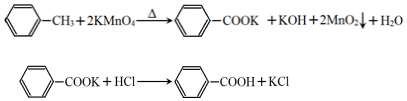
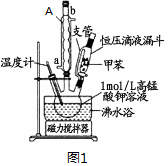
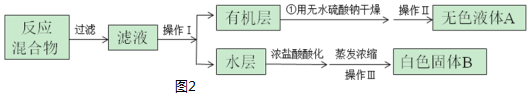
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 體積(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 質量為32g | B. | 含氧原子數為NA | ||
| C. | 含氧分子數為NA | D. | 在標準狀況下,體積約為22.4L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在由水電離產生的氫離子濃度為10-13 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3-四種離子能大量共存 | |
| B. | 已知MgCO3的Ksp=6.82×10-6,則所有含有固體MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 | |
| C. | 常溫下,將0.2 mol?L-1某一元堿(ROH)溶液和0.1 mol?L-1HCl溶液等體積混合,混合后溶液pH<7,則c(ROH)>c(R+) | |
| D. | 對于反應N2H4(l)=N2(g)+2H2(g),△H=-50.6 kJ?mol-1,它只在高溫下自發進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 標準狀況下,22.4 L H2含有的原子數是2NA | |
| B. | 標準狀況下,NA個水分子的體積是22.4 L | |
| C. | 任何情況下,1 mol CO中都含有NA個分子 | |
| D. | 通常狀況下,NA個NH3分子的體積是22.4 L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=11的溶液 | B. | 4 g NaOH溶于水形成1L的水溶液 | ||
| C. | c(OH-)=0.12 mol•L-1 | D. | c(H+)=1×10-10 mol•L-1的溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com