
提純下列物質(括號內的物質是雜質),所選用的除雜試劑和分離方法都正確的是( )
| | 被提純的物質 | 除雜試劑 | 分離方法 |
| A | 乙酸乙酯(乙酸) | CCl4 | 萃取、分液 |
| B | 乙烷(乙烯) | 酸性KMnO4溶液 | 洗氣 |
| C | 溴苯(溴) | 氫氧化鈉溶液 | 分液 |
| D | 苯(苯酚) | 濃溴水 | 過濾 |
科目:高中化學 來源: 題型:實驗題
實驗室制備苯乙酮的化學方程式為:
制備過程中還有CH3COOH+AlCl3―→CH3COOAlCl2+HCl↑等副反應。
主要實驗裝置和步驟如下:
(Ⅰ)合成:在三頸瓶中加入20g無水三氯化鋁和30mL
無水苯。為避免反應液升溫過快,邊攪拌邊慢慢滴加6mL
乙酸酐和10mL無水苯的混合液,控制滴加速率,使反應液
緩緩回流。滴加完畢后加熱回流1小時。
(Ⅱ)分離與提純:①邊攪拌邊慢慢滴加一定量濃鹽酸與冰水混合液,分離得到有機層②水層用苯萃取,分液③將①②所得有機層合并,洗滌、干燥、蒸去苯,得到苯乙酮粗產品④蒸餾粗產品得到苯乙酮
回答下列問題:(1)儀器a的名稱:________;裝置b的作用:________。
(2)合成過程中要求無水操作,理由是_______________________。
(3)若將乙酸酐和苯的混合液一次性倒入三頸瓶,可能導致________。
| A.反應太劇烈 | B.液體太多攪不動 | C.反應變緩慢 | D.副產物增多 |

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
碳酸鎂晶須是一種新型的吸波隱形材料中的增強材料。
(1)合成該物質的步驟如下:
步驟1:配制0.5mol·L-1MgSO4溶液和0.5mol·L-1NH4HCO3溶液。
步驟2:用量筒量取500mL NH4HCO3溶液于1000mL四口燒瓶中,開啟攪拌器。溫度控制在50℃。
步驟3:將250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min內滴加完后,用氨水調節溶液pH到9.5。
步驟4:放置1h后,過濾,洗滌。
步驟5:在40℃的真空干燥箱中干燥10h,得碳酸鎂晶須產品(MgCO3·nH2O n=1~5)。
①步驟2控制溫度在50℃,較好的加熱方法是 。
②步驟3生成MgCO3·nH2O沉淀的離子方程式為 。
③步驟4檢驗是否洗滌干凈的方法是 。
(2)測定合成的MgCO3·nH2O中的n值。
稱量1.000g碳酸鎂晶須,放入如圖所示的廣口瓶中加入水滴入稀硫酸與晶須反應,生成的CO2被NaOH溶液吸收,在室溫下反應4~5h,反應后期將溫度升到30℃,最后的燒杯中的溶液用已知濃度的鹽酸滴定,測得CO2的總量;重復上述操作2次。
①圖中氣球的作用是 。
②上述反應后期要升溫到30℃,主要目的是 。
③設3次實驗測得每1.000g碳酸鎂晶須產生的CO2平均值為a mol,則n值為 (用含a的表達式表示)。
(3)稱取100g上述晶須產品進行熱重分析,熱重曲線如圖。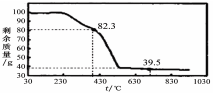
則該條件下合成的晶須中,n= (選填:1、2、3、4、5)。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
純堿(Na2CO3)在生產生活中具有廣泛的用途。以下是實驗室模擬制堿原理制取Na2CO3的流程圖
已知:向飽和食鹽水中通入NH3,CO2后發生和反應為NaCl+NH3+CO2+H2O NaHCO3↓+NH4Cl,請回答以下問題:
NaHCO3↓+NH4Cl,請回答以下問題:
(1)粗鹽中含有的雜質離子有Ca2+,Mg2+,SO42-等。
精制除雜的步驟順序a→_______→________→________→b(填字母編號)。
a.粗鹽溶解,濾去沉渣.b.加入鹽酸調pH;c.加入Ba(OH)2溶液;d.加入Na2CO3溶液;e.過濾
向飽和食鹽水中先通入NH3,后通人CO2,理由是_____________________。
(2)灼燒固體A制Na2CO3在_____填字母序號)中進行。
a.坩堝 b.蒸發皿 c.燒杯 d.錐形瓶
證明濾液A中含有NH4+的方法是__________________________________________________________。
對濾液A進行重結晶能夠獲得NH4HCO3,向pH=13含Na+,K+的溶液中加入少量NH4HCO3。使pH降低,反應的離子方程式____________________________________。
(3)下圖裝置中常用于實驗室制備CO2的是_____(填字母編號);用b示意的裝置制備NH3,分液漏斗中盛放的試劑______(填試劑名稱),燒瓶內可加入的固體試劑__________(填試劑名稱)。
(4)一種天然堿晶體成分是aNa2CO3·bNa2CO3·cH2O,某同學利用下列提供的試劑,設計了如下簡單合理測定Na2CO3的質量分數的實駿方案。(儀器自選)請把實驗方案填全:供選擇的試劑:1.0mol/LH2SO4溶液、1.0mol/L BaCl2溶液、稀氨水、堿石灰、Ca(OH)2溶液、蒸餾水
①稱取m1g一定量天然堿晶體樣品,溶于適量蒸餾水中。
②_________________________________________________________________。
③_________________________________________________________________。
④計算天然堿晶體中含Na2CO3的質量分數。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
制備水楊酸對正辛基苯基酯( )如下:
)如下:
步驟一:將水楊酸晶體投入三頸燒瓶中,再加入氯苯,攪拌溶解后,加入無水三氯化鋁。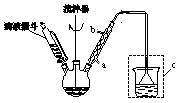
步驟二:按圖所示裝置裝配好儀器,水浴加熱控制溫度在20~40℃之間,在攪拌下滴加SOCl2,反應制得
水楊酰氯。該反應為: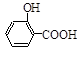 (水楊酸)+SOCl2→
(水楊酸)+SOCl2→ (水楊酰氯)+HCl↑+SO2↑
(水楊酰氯)+HCl↑+SO2↑
步驟三:將三頸燒瓶中的混合液升溫至80℃,再加入對正辛苯酚[ ],溫度控制在100℃左右,不斷攪拌。
],溫度控制在100℃左右,不斷攪拌。
步驟四:過濾、蒸餾、減壓過濾;酒精洗滌、干燥。
(1)步驟一中加入三氯化鋁的作用是 。
(2)實驗時,冷凝管中的水應從 進 出(選填“a”或“b”);裝置c的作用是 。
(3)步驟三中發生反應的化學方程式為 。
(4)步驟四減壓過濾操作中,除燒杯、玻璃棒外,還必須使用的硅酸鹽材料的儀器有 。
(5)步驟四減壓過濾時,有時濾紙會穿孔,避免濾紙穿孔的措施是 。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列實驗操作與預期實驗目的或結論均正確的是( )
| 選項 | 實驗操作 | 預期實驗目的或結論 |
| A | 室溫下,用pH試紙測定濃度為0.1mol·L-1 Na2SiO3溶液和Na2CO3溶液的pH | 比較Si和C的電負性 |
| B | 某溶液中加入硝酸酸化的氯化鋇溶液,有白色沉淀生成 | 該溶液中含有SO42- |
| C | 向某溶液中加入2滴KSCN溶液,溶液不顯紅色。再向溶液中加入幾滴新制的氯水,溶液變為紅色 | 該溶液中一定含有Fe2+ |
| D | 將某氣體通入淀粉和KI的混合溶液,溶液變藍色 | 該氣體一定是Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一條魚蝦絕跡的小河邊,從上游到下游依次有四座工廠:甲、乙、丙、丁.它們排出的廢液里,每廠只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一種.某中學環保小組對河水監測時發現:(1)甲處河水呈乳白色;(2)乙處河水呈褐色;(3)丙處河水由渾變清;(4)丁處河水產生氣泡,河水仍清.下列四廠排出廢液里所含污染物推斷正確的為( )
| A.甲含HCl | B.乙含FeCl3 | C.丙含Na2C03 | D.丁含Ca(OH)2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com