

| A.a電極是負極,OH-移向正極 |
| B.b電極的電極反應為:O2+2H2O+4e-=4OH- |
C.電池總反應式為:2H2+O2 2H2O 2H2O |
| D.電解質溶液的pH保持不變 |
 2NH3(g) ΔH=-92.20 kJ·mol-1。
2NH3(g) ΔH=-92.20 kJ·mol-1。| 時間(h) 物質的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | n2 | 1.00 | 1.00 |


 53隨堂測系列答案
53隨堂測系列答案科目:高中化學 來源:不詳 題型:填空題
| | N2+3H2 2NH3 2NH3 | |||
| 溫度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常數K | 5×108 | 650 | 0.507 | 0.01 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 C(g)+D(g),在不同溫度下,D的物質的量n(D)和時間t的關系如圖。
C(g)+D(g),在不同溫度下,D的物質的量n(D)和時間t的關系如圖。
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 cC(g)(△H<0)在等容條件下進行。改變其他反應條件,在Ⅰ、Ⅱ、Ⅲ階段體系中各物質濃度隨時間變化的曲線如下圖所示:
cC(g)(△H<0)在等容條件下進行。改變其他反應條件,在Ⅰ、Ⅱ、Ⅲ階段體系中各物質濃度隨時間變化的曲線如下圖所示: 

查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
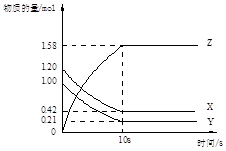
| A.反應開始到10s,用Z表示的反應速率為0.158mol/(Ls) |
| B.反應開始到10s,X的物質的量濃度減少了0.79mol/L |
| C.反應開始到10s時,Y的轉化率為79.0% |
D.反應的化學方程式為: X(g)+Y(g)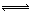 Z(g) Z(g) |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO3(g);ΔH<0。某溫度下,將2 mol SO2和1 mol O2置于10 L密閉容器中,反應達平衡后,SO2的平衡轉化率(α)與體系總壓強(p)的關系如圖甲所示。則下列說法正確的是
2SO3(g);ΔH<0。某溫度下,將2 mol SO2和1 mol O2置于10 L密閉容器中,反應達平衡后,SO2的平衡轉化率(α)與體系總壓強(p)的關系如圖甲所示。則下列說法正確的是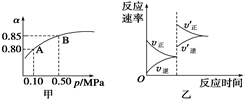
| A.由圖甲知,A點SO2的平衡濃度為0.4 mol/L |
| B.由圖甲知,B點SO2、O2、SO3的平衡濃度之比為2∶1∶2 |
| C.達平衡后,縮小容器容積,則反應速率變化圖象可以用圖乙表示 |
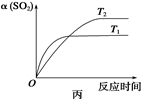
| D.壓強為0.50 MPa時不同溫度下SO2轉化率與溫度關系如丙圖,則T2>T1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 n Z (g) △H > 0,將X和Y以一定比例混合通入密閉容器中進行反應,各物質的濃度隨時間的改變如圖所示。下列說法不正確的是
n Z (g) △H > 0,將X和Y以一定比例混合通入密閉容器中進行反應,各物質的濃度隨時間的改變如圖所示。下列說法不正確的是
| A.反應方程式中n=1 |
| B.10 min時,曲線發生變化的原因是升高溫度 |
| C.10 min時,曲線發生變化的原因是增大壓強 |
| D.0~5 min內,用X表示的反應速率為v(X)="0.08" mol·L-1·min-1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 3F+2G,用傳感器測得該反應在不同pH條件下,物質D的濃度(用每升溶液所含溶質的質量表示,單位為mg/L)變化如圖所示,下列有關說法正確的是
3F+2G,用傳感器測得該反應在不同pH條件下,物質D的濃度(用每升溶液所含溶質的質量表示,單位為mg/L)變化如圖所示,下列有關說法正確的是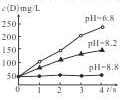
| A.pH=6.8時,D的濃度(mg/L)一定最大 |
| B.在pH相同的條件下,增大壓強,D的濃度(mg/L)增大 |
| C.調節pH到8.8,可使該反應正、逆反應速率都為0 |
| D.溫度相同時,不同pH條件下,該反應的平衡常數相同 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 C(g)
C(g)| 反應時間/min | n(A)/mol | n(B)/ mol |
| 0 | 1.00 | 1.20 |
| 10 | 0.50 | |
| 30 | | 0.20 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com