
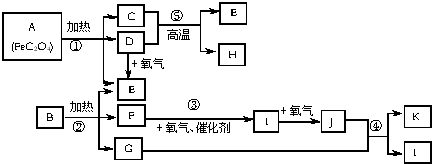
分析 A中[FeC2O4]和C中Fe元素均為+2價,A加熱分解得到C、氣體D與氣體E,且D與氧氣反應得到E,可推知C為FeO,D為CO,E為CO2,由反應⑤可知H為Fe;B是一種常見的化肥,加熱分解得到二氧化碳、氣體F與G,且F能連續與氧氣反應,B為碳酸形成的銨鹽,1molE與含1molF的水溶液恰好反應生成B,B為NH4HCO3,F為NH3,I為NO,J為NO2,G為H2O,K為HNO3,據此解答.
解答 解:A中[FeC2O4]和C中Fe元素均為+2價,A加熱分解得到C、氣體D與氣體E,且D與氧氣反應得到E,可推知C為FeO,D為CO,E為CO2,由反應⑤可知H為Fe;B是一種常見的化肥,加熱分解得到二氧化碳、氣體F與G,且F能連續與氧氣反應,B為碳酸形成的銨鹽,1molE與含1molF的水溶液恰好反應生成B,B為NH4HCO3,F為NH3,I為NO,J為NO2,G為H2O,K為HNO3,
(1)A中[FeC2O4]和C中Fe元素均為+2價,則FeC2O4中碳元素的化合價為+3,E的化學式為CO2,
故答案為:+3;CO2;
(2)反應③的化學方程式為:4NH3+5O2 $\frac{\underline{催化劑}}{△}$4NO+6H2O,
反應④的化學方程式為:3NO2+H2O=2HNO3+NO,
反應⑤的化學方程式為:FeO+CO$\frac{\underline{\;高溫\;}}{\;}$Fe+CO2,
故答案為:4NH3+5O2 $\frac{\underline{催化劑}}{△}$4NO+6H2O;3NO2+H2O=2HNO3+NO;FeO+CO$\frac{\underline{\;高溫\;}}{\;}$Fe+CO2;
(3)少量Fe與HNO3的濃溶液反應生成硝酸鐵與二氧化氮,在一定條件下反應若有1mol HNO3被還原時,轉移的電子總數為1mol×(6-4)×6.02×1023mol-1=6.02×1023,
故答案為:6.02×1023;
(4)過量Fe與HNO3的稀溶液反應的離子方程式:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O,故答案為:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O.
點評 本題考查無機物推斷,側重對化學用語的考查,需要學生熟練掌握元素化合物知識,難度中等.


 開心蛙狀元測試卷系列答案
開心蛙狀元測試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | Na、Al、Fe金屬單質在一定條件下與水反應都生成H2和對應的堿 | |
| B. | 將鐵粉加入FeCl3、CuCl2混合溶液中,充分反應后剩余的固體中必有銅 | |
| C. | 將SO2通入Ca(ClO)2溶液可生成CaSO3沉淀 | |
| D. | 過量的銅與濃硝酸反應,生成的氣體只有NO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸氫鈉溶液中加入鹽酸CO32-+2H+═CO2↑+H2O | |
| B. | 硫化亞鐵與鹽酸反應S2-+2H+═H2S↑ | |
| C. | 苯酚鈉溶于醋酸溶液C6H5O-+CH3COOH→C6H5OH+CH3COO- | |
| D. | 氯化亞鐵溶液中通入少量氯氣Fe2++Cl2═Fe3++2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| c (H+) | c(SO42-) | c (Fe2+、Fe3+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 22.4LCO和CO2的混合氣體中所含的碳原子數一定是NA | |
| B. | 常溫常壓下,22.4L氯氣與足量鎂粉充分反應,轉移的電子數為2NA | |
| C. | 常溫常壓下,32gO2和32gO3所含氧原子數都是2NA | |
| D. | 1L1mol/L的鹽酸溶液中含HCl的分子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 溶液中的陽離子有H+、Mg2+、Al3+、NH4+ | |
| B. | 溶液中n(NH4+)=0.2 mol | |
| C. | 溶液中一定不含CO32-和NO3-,可能含有SO42- | |
| D. | n(H+):n(Al3+):n(Mg2+)=2:2:1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com