
(20分)氯堿工業中電解飽和食鹽水的原理示意圖,如圖所示: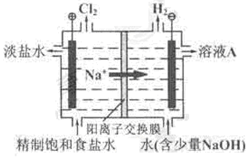
(1)溶液A的溶質是 ;
(2)電解飽和食鹽水的離子方程式是 ;
(3)電解時用鹽酸控制陽極區溶液的pH在2~3,用化學平衡移動原理解釋鹽酸的作用 ;
(4)電解所用的鹽水需精制。
去除有影響的Ca2+、Mg2+、N H4+、SO42-[c(SO42-)>c(Ca2+)]。
H4+、SO42-[c(SO42-)>c(Ca2+)]。
精致流程如下(淡鹽水和溶液A來電解池):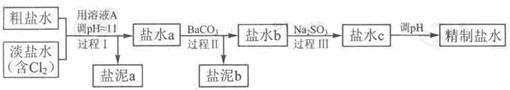
①鹽泥a除泥沙外,還含有的物質是 。
②過程Ⅰ中將NH4+轉化為N2的離子方程式是
③BaSO4的溶解度比BaCO3的小,過程Ⅱ中除去的離子有
④經過程Ⅲ處理,要求鹽水中c 中剩余Na2SO3的含量小于5mg /L,若鹽水b中NaClO的含量是7.45 mg /L ,則處理10m3鹽水b ,至多添加10% Na2SO3溶液 kg(溶液體積變化忽略不計)。
科目:高中化學 來源: 題型:
| A、硫酸生產中常采用高壓條件提高SO2的轉化率 | B、合成氨中采用及時分離氨氣提高反應速率 | C、電解精煉銅時,溶液中c(Cu2+)基本保持不變 | D、氯堿工業電解飽和食鹽水時,陽極得到氫氧化鈉和氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、用電解法精練粗銅時,粗銅作陽極,純銅作陰極 | B、鋅錳干電池工作時,電池的總反應為:Zn+2MnO2+2NH4+?Zn2++Mn2O3+2NH3+H2O | C、鋼鐵電化學腐蝕時,負極反應式為:2H2O+O2+4e-?4OH- | D、氯堿工業中電解飽和食鹽水,陽極反應式為:2Cl--2e-?Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、“氯堿工業”的原料是Cl2和燒堿 | B、“氯堿工業”的主要生產過程是電解飽和食鹽水 | C、“氯堿工業”的主要產品是純堿 | D、“氯堿工業”消耗的能源主要是熱能 |
查看答案和解析>>
科目:高中化學 來源: 題型:
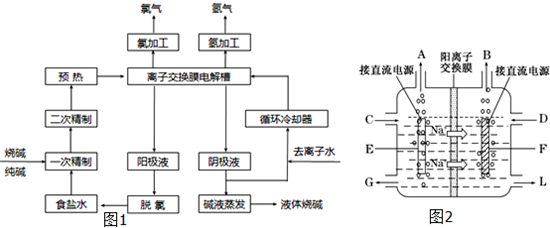
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com