
| A. | 1mol Fe與1mol Cl2反應時轉移的電子數目為3NA | |
| B. | 3g C18O和14CO的混合物中所含電子、中子數目為1.4NA | |
| C. | 0℃、101kPa下,0.1mol 乙炔和甲醛(HCHO)的混合物中含有C-H數目為0.2NA | |
| D. | 50ml 18mo•L-1濃H2SO4與足量的Cu充分反應,能收集到SO2的分子數目為0.45NA |
分析 A、1mol鐵和1mol氯氣反應時,鐵過量,根據氯氣反應后變為-1價來分析;
B、C18O和14CO的摩爾質量均為30g/mol,且均含14個電子和16個中子;
C、乙炔和甲醛(HCHO)中均含2條C-H鍵;
D、銅和濃硫酸反應,和稀硫酸不反應.
解答 解:A、1mol鐵和1mol氯氣反應時,鐵過量,而氯氣反應后變為-1價,故1mol氯氣轉移2NA個電子,故A錯誤;
B、C18O和14CO的摩爾質量均為30g/mol,故3g混合物的物質的量為0.1mol,且均含14個電子和16個中子,故0.1mol混合物中含1.4NA個電子和1.6NA個中子,故B錯誤;
C、乙炔和甲醛(HCHO)中均含2條C-H鍵,故0.1mol乙炔和甲醛的混合物中含0.2NA條C-H鍵,故C正確;
D、銅和濃硫酸反應,和稀硫酸不反應,故濃硫酸不能反應完全,則生成的二氧化硫的分子個數小于0.45NA個,故D錯誤.
故選C.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:實驗題
| 實驗方案 |
| 1.用砂紙打磨后的鎂帶加適量水加熱,再向反應后溶液中滴加酚酞 |
| 2.鈉與滴有酚酞試液的冷水反應 |
| 3.鎂帶與2mol/L的鹽酸反應 |
| 4.鋁條與2mol/L的鹽酸反應 |
| 5.向氯化鋁溶液中滴加氫氧化鈉溶液至過量 |
| 實驗現象 |
| (A) |
| (B)反應不十分強烈,產生氣體 |
| (C)劇烈反應,產生氣體 |
| (D)生成白色膠狀沉淀,然后沉淀消失 |
| (E)產生的氣體可在空氣中燃燒,溶液變成淺紅色 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
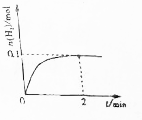 一定溫度下,向2L密閉容器中加入1molNH3(g).發生反應2NH3(g)?3H2(g)+N2(g)△H=+92kJ/mol
一定溫度下,向2L密閉容器中加入1molNH3(g).發生反應2NH3(g)?3H2(g)+N2(g)△H=+92kJ/mol查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
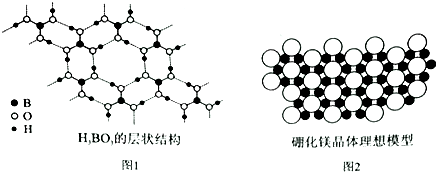 硼元素在化學中有很重要的地位,硼及其化合物廣泛應用于永磁材料、超導材料、復合材料等高新材料領域.
硼元素在化學中有很重要的地位,硼及其化合物廣泛應用于永磁材料、超導材料、復合材料等高新材料領域.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | 實驗目的 | T/K | pH | c/10-3 mol•L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 為以下實驗作參照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究溫度對降解反應速率的影響 | 313 | 3 | 6.0 | 0.30 |
| ③ | 探究溶液的pH對降解反應速率的影響 | 298 | 10 | 6.0 | 0.30 |
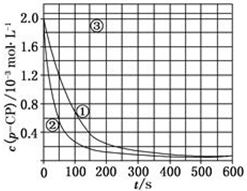 [數據處理]實驗測得p-CP的濃度隨時間變化的關系如圖:
[數據處理]實驗測得p-CP的濃度隨時間變化的關系如圖:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com