
| A. | 10% | B. | 20% | C. | 30% | D. | 40% |
 小學課時作業全通練案系列答案
小學課時作業全通練案系列答案 金版課堂課時訓練系列答案
金版課堂課時訓練系列答案 單元全能練考卷系列答案
單元全能練考卷系列答案科目:高中化學 來源: 題型:解答題

| 物質 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸點/℃ | -57.7 | 12.8 | - | 315 | - |
| 熔點/℃ | -70.0 | -107.2 | - | - | - |
| 升華溫度/℃ | - | - | 180 | 300 | 162 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
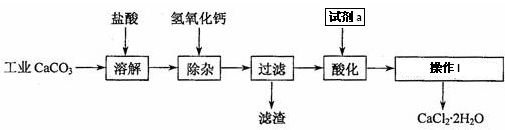
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 在2L密閉容器中,800℃時反應2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:
在2L密閉容器中,800℃時反應2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 高效利用CO2是“低碳經濟”的有效途徑,現有以下兩種利用CO2的方法.
高效利用CO2是“低碳經濟”的有效途徑,現有以下兩種利用CO2的方法.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com