
【題目】下列有關實驗原理、方法和結論都正確的是
A. 向飽和FeCl3溶液中滴加過量氨水,可制取Fe(OH)3膠體
B. 取少量溶液X,向其中加入適量新制氯水,再加幾滴KSCN溶液,溶液變紅,說明X溶液中一定含有Fe2+
C. 某鉀鹽溶于鹽酸,產生能使澄清石灰水變渾濁的無色無味氣體,說明該鉀鹽是![]()
D. 向久置的Na2SO3溶液中加入足量BaCl2溶液,出現白色沉淀;再加入足量稀鹽酸,部分沉淀溶解,部分Na2SO3被氧化
【答案】D
【解析】A. 向飽和FeCl3溶液中滴加過量氨水,不能用于制取Fe(OH)3膠體,得到的是氫氧化鐵膠體;B. 取少量溶液X,向其中加入適量新制氯水,再加幾滴KSCN溶液,溶液變紅,不能證明X溶液中一定含有Fe2+,這樣操作不能排除原溶液含有Fe3+的可能;C. 某鉀鹽溶于鹽酸,產生能使澄清石灰水變渾濁的無色無味氣體,不能證明該鉀鹽是![]() ,這樣操作不能排除該鉀鹽是碳酸氫鉀的可能;D. 向久置的Na2SO3溶液中加入足量BaCl2溶液,出現白色沉淀;再加入足量稀鹽酸,部分沉淀溶解,說明還有一部分沉淀不溶于稀鹽酸,從而說明有部分Na2SO3被氧化為硫酸鈉,D正確。本題選D.
,這樣操作不能排除該鉀鹽是碳酸氫鉀的可能;D. 向久置的Na2SO3溶液中加入足量BaCl2溶液,出現白色沉淀;再加入足量稀鹽酸,部分沉淀溶解,說明還有一部分沉淀不溶于稀鹽酸,從而說明有部分Na2SO3被氧化為硫酸鈉,D正確。本題選D.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】鉻、鐵、鎳、銅等金屬及其化合物在工業上有重要用途。
(l)基態鉻原子的價電子排布式為___________。
(2)CrO2C12和NaClO均可作化工生產的氧化劑或氯化劑。制備CrO2C12的反應為:
K2Cr2O7 + 3CCl4 = 2KCl+ 2 CrO2C12+ 3COCl2↑
① 上述反應式中非金屬元素電負性由大到小的順序是_______(用元素符號表示)。
② 常溫下CrO2C12是一種易溶于CCl4的液體,則固態CrO2C12屬于______晶體。
③ COCl2分子中所有原子均滿足8電子結構,則COCl2分子中σ鍵和π鍵的個數比為_______。
(3)NiO、FeO的晶體結構均與氯化鈉的晶體結構相同,其中Ni2+和Fe2+的半徑分別為6.9×10-2 nm 和7.8×10-2 nm,則熔點:NiO______(填“< ”、“= ”或“>” ) FeO。
④CuCl的鹽酸溶液能吸收CO生成復合物氯化羰基亞銅[Cu2Cl2(CO)2·2H2O] ,其結構如圖所示。下列說法不正確的是_____(填字母序號)。

A.該復合物中只含有離子鍵和配位鍵 B.該復合物中Cl原子的雜化類型為sp3
C.該復合物中只有CO和H2O作為配位體 D.CO與N2的價電子總數相同,其結構為C≡O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,有0.01 molL-1的醋酸溶液,試回答下列問題:
(1)寫出醋酸的電離平衡常數表達式_____________
(2)達平衡時,溶液中c(H+)=______________(25℃時,醋酸的K=1.75×10 -5)
(3)當向該溶液中加入一定量的鹽酸時,溶液中的c(H+)_____,c (CH3COO-)_________(填增大、減小、不變)。
(4)當向該溶液中加入一定量的鹽酸時,電離常數________ (填增大、減小、不變)。原因________________________________________________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知高鐵酸鈉(Na2FeO4)是一種綠色消毒凈水劑,只在堿性環境中穩定存在。下列是通過次氧酸鈉氧化法制備高鐵酸鈉并探究其性質的實驗,步驟如下:
I.制備高鐵酸鈉(Na2FeO4)
(1)制備NaClO溶液
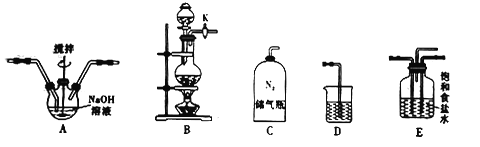
已知:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
①如何檢查裝置B的氣密性?____________________________________________。
②實驗室制取Cl2的化學方程式是_______________________,利用如圖所給的裝置組裝成制備NaClO的正確連接順序是![]() ________(填字母),其中裝置E的作用是________(填序號)。
________(填字母),其中裝置E的作用是________(填序號)。
a.混合氣體 b.除去氯氣中的氯化氫 c.干燥氣體 d.觀察氣體的通入速率
③為了防止產生NaClO3,除攪拌和混入N2稀釋外,還應采取的操作是__________________。
(2)制備Na2FeO4:將Fe(NO3)2溶液加入到NaOH與NaClO的混合溶液中,其反應的離子方程式是___________________________________。
II.高鐵酸鈉(Na2FeO4)具有強氧化性,某實驗小組的同學對于高鐵酸鈉消毒后鐵元素的存在形式展開如下探究:
【提出猜想】:猜想1:全部為Fe2+ 猜想2:全部為Fe3+ 猜想3: Fe2+和Fe3+都有
【設計實驗】:
(1)證明溶液中只含有Fe2+的實驗操作是_________________________________。
(2)某實驗小組將消毒后的溶液分在兩支試管中,進行如下實驗:
步驟一:向試管1中加入K3[Fe(CN)6]溶液,現象是__________,所以溶液中不存在Fe2+;
步驟二:向試管2中滴入KSCN溶液,溶液變成血紅色,所以溶液中存在Fe3+。
【實驗結論】:高鐵酸鈉消毒后溶液中只存在Fe3+。
(3)小明同學認為上述實驗結論不夠嚴謹,原因是___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】巧妙的實驗設計有助于更好地解決問題。下列裝置不能達到實驗目的的是

A. 用裝置甲驗證HCl氣體易溶于水
B. 用裝置乙驗證SO2具有漂白性
C. 用裝置丙采集到的壓強數據判斷鐵釘發生析氫腐蝕還是吸氧腐蝕
D. 用裝置丁檢驗NH4Cl分解產生的氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)將下列物質進行分類:
①![]() H與
H與![]() H ②O2與O3 ③乙醇(C2H5OH) 與甲醚 (CH3—O—CH3) ④正丁烷與異丁烷 ⑤C60與金剛石;互為同分異構體的是__________________;
H ②O2與O3 ③乙醇(C2H5OH) 與甲醚 (CH3—O—CH3) ④正丁烷與異丁烷 ⑤C60與金剛石;互為同分異構體的是__________________;
(2)若將反應Fe+H2SO4===FeSO4+H2↑設計成原電池銅為原電池某一極材料,則銅為______(填“正”或“負”)極。該極上發生的電極反應為_____________________,外電路中電子由______極(填“正”或“負”,下同)向______極移動。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子在指定溶液中一定能大量共存的是
A.能使甲基橙變紅的溶液中:Fe2+、Al3+、NO![]() 、Cl-
、Cl-
B.在pH=12的溶液中:Na+、AlO![]() 、NO
、NO![]() 、S2-
、S2-
C.室溫下,由水電離的c(H+)=10-10mol/L的溶液中:Cl-、HCO![]() 、NO
、NO![]() 、NH
、NH![]()
D.加入Mg能放出H2的溶液中:Mg2+、NH![]() 、ClO-、K+
、ClO-、K+
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com