
(1)(3分)有反應:2NO2![]() N2O4 △H<0,根據圖像判斷后填空:
N2O4 △H<0,根據圖像判斷后填空:
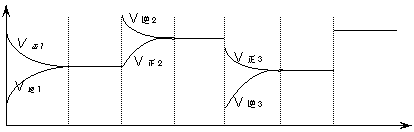
t1 t2 t3 t4 t5 t6 t
t1至t3采取的措施是_____________;t4至t5采取的措施是______________t6采取的措施是_________________。
(2)(3分)蓋斯定律在生產和科學研究中有很重要的意義。有些反應的反應熱雖然無法直接測得,但可通過間接的方法測定。現根據下列3個熱化學反應方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2 △H=-25kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
 請寫出FeO(s)被CO(g)還原成Fe和CO2(g)的熱化學方程式 。
請寫出FeO(s)被CO(g)還原成Fe和CO2(g)的熱化學方程式 。
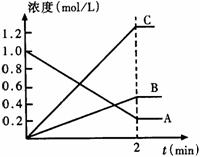
(3)(2分)右圖表示800℃時,A、B、C三種氣體物質的濃度隨時間變化的情況,t是達到平衡狀態的時間。則該反應的化學方程式為________________________。
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:閱讀理解
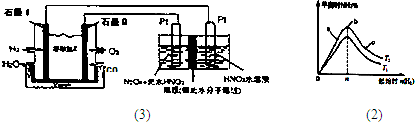
 (2011?黃山模擬)如圖是各種不同密度的硝酸與鐵反應(相同溫度)時主要還原產物的分布圖.請認真讀圖分析,回答有關問題.
(2011?黃山模擬)如圖是各種不同密度的硝酸與鐵反應(相同溫度)時主要還原產物的分布圖.請認真讀圖分析,回答有關問題.
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| c(N2)?c2(CO2) |
| c2(CO)?c2(NO) |
| c(N2)?c2(CO2) |
| c2(CO)?c2(NO) |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
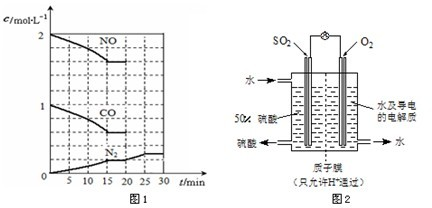
 CO2、SO2、NOx是重要的非金屬氧化物,與我們的生存環境息息相關.
CO2、SO2、NOx是重要的非金屬氧化物,與我們的生存環境息息相關.| C(HCO3-)C(OH-) |
| C(CO32-) |
| C(HCO3-)C(OH-) |
| C(CO32-) |
| 5 |
| 144 |
| 5 |
| 144 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| n |
| 3 |
| n |
| 3 |
| V/s | 0 | 50 | 100 |
| c(N2O3)/mol?L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 1 |
| 2 |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com