
A、合金中的物質的量為
| ||
| B、d=a+17b | ||
C、c1=
| ||
| D、與金屬反應后剩余鹽酸的物質的量濃度為(c1V1-b)mol/L |
| n |
| V |
|
|
| a-3b |
| 18 |
| bg |
| 2g/mol |
| c2V2 |
| V1 |
| c1V1-b |
| V1 |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、限制化學工業發展,關停所有化工企業,消除污染源頭 |
| B、積極推廣太陽能、風能等新能源的使用,減少化石燃料的使用 |
| C、加強城市生活污水脫氮除磷處理,遏制水體富營養化 |
| D、禁止農村燃燒秸桿,積極推廣沼氣、秸稈發電、秸稈制乙醇等實用技術的使用 |
查看答案和解析>>
科目:高中化學 來源: 題型:
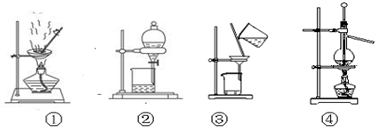
| A、用圖①裝置蒸發稀鹽酸制濃鹽酸 |
| B、用圖②裝置分液時,下層液體從分液漏斗下口放出,關閉活塞再將上層液體從上口倒出 |
| C、用圖③洗滌沉淀時,漏斗中加入適量蒸餾水,攪拌并濾干 |
| D、用圖④裝置,分離四氯化碳與苯的混合溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 編號 | H2C2O4溶液 | KMnO4溶液 | 硫酸溶液 | 溫度/℃ | ||
| 濃度 (mol/L) | 體積 (mL) | 濃度 (mol/L) | 體積 (mL) | |||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 50 |
查看答案和解析>>
科目:高中化學 來源: 題型:

| A、圖Ⅰ中a的取值范圍為0≤a<50 | ||
B、圖Ⅰ中
| ||
| C、圖Ⅱ中a的取值范圍為80<a<90 | ||
| D、圖Ⅲ中a的取值范圍為75<a<90 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、2 | B、3 | C、6 | D、9 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 可逆反應mA(g)+nB(g)?pC(g)+gD(g)的v-t圖象如圖Ⅰ所示,若其他條件都不變,只是在反應前加入合適的催化劑,則其v-t圖象如圖Ⅱ所示.
可逆反應mA(g)+nB(g)?pC(g)+gD(g)的v-t圖象如圖Ⅰ所示,若其他條件都不變,只是在反應前加入合適的催化劑,則其v-t圖象如圖Ⅱ所示. | A、②④⑤⑦ | B、②④⑤⑧ |
| C、②③⑤⑦ | D、②③⑤⑧ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com